
科目: 来源: 题型:
【题目】化合物PH4I是一种白色晶体,受热不稳定,易分解产生PH3。PH3是无色剧毒气体, 广泛用于半导体器件和集成电路生产的外延、离子注入和掺杂。
(1)在2L真空密闭容器中加入一定量PH4I固体,T1℃ 时发生如下反应: PH4I(s) PH3(g) + HI(g)
①下列可以作为反应达到平衡的判据是_____。
A.容器内气体的压强不变
B.容器内 HI 的气体体积分数不变
C.容器内 PH4I 质量不变
D.容器内气体的密度不变
E.容器内气体的平均相对分子质量不变
②t1时刻反应达到平衡后,在t2时刻维持温度不变瞬间缩小容器体积至1L,t3时刻反应重新达到 平衡。在下图中画出t2~t4 时段的υ正、υ逆随时间变化图______。
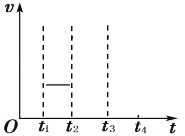
(2)PH4I固体分解产生的PH3和HI均不稳定,在一定温度下也开始分解。在2L真空密闭容器中加 入一定量PH4I固体,已知在T2℃ 时存在如下反应:
Ⅰ PH4I(s) PH3(g) + HI(g) ΔH1
Ⅱ 4 PH3(g) P4(g) + 6 H2(g) ΔH2
Ⅲ 2 HI(g) H2 (g) + I2(g) ΔH3
①已知:298K,101kPa,H-P键、P-P键、H-H键的键能分别为322 kJ·mol-1、200 kJ·mol-1、436 kJ·mol-1试计算ΔH2 =______________。
②各反应均达平衡时,测得体系中 n(PH3)=a mol ,n(P4)=b mol ,n(H2)=c mol ,则 T2℃时 反应I的平衡常数K值为___________________。(用a、b、c表示)
③维持温度不变,缩小体积增大压强,达到新的平衡后,发现其它各成分的物质的量均发生变化,而n(I2)基本不变,试解释可能原因_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气还原 NO 的反应为![]() 。
。
(1)![]() 的电子式为________。
的电子式为________。
(2)已知几种共价键的键能如下:
共价键 | H-H |
| N-O | H-O |
键能/( | 436 | 946 |
| 464 |
根据上述数据计算,NO的键能![]() =___________。
=___________。
(3)![]() 的反应速率表达式为
的反应速率表达式为![]() (
(![]() 为正反应速率常数,只与温度有关。
为正反应速率常数,只与温度有关。![]() 和
和![]() 为反应级数,取最简正整数)。
为反应级数,取最简正整数)。
为了探究一定温度下 NO、![]() 的浓度对反应速率的影响,测得实验数据如下:
的浓度对反应速率的影响,测得实验数据如下:
序号 |
|
|
|
Ⅰ | 0.10 | 0.10 | 0.414 |
Ⅱ | 0.10 | 0.20 | 0.828 |
Ⅲ | 0.30 | 0.10 | 3.726 |
①![]() 中,
中,![]() =____,
=____,![]() =______。
=______。
②经研究,有人提出上述反应分两步进行:![]() ;
;![]() 。
。
化学总反应由较慢的一步反应决定。
上述反应中,(a)反应较慢,(a)正反应活化能________(填“大于”“小于”或“等于”)(b)正反应活化能。
③1889年,瑞典化学家阿伦尼乌斯根据实验结果,提出了温度与反应速率常数关系的经验公式:![]() [
[![]() 为反应速率常数,
为反应速率常数,![]() 为比例常数,
为比例常数,![]() 为自然对数的底数,
为自然对数的底数,![]() 为气体摩尔常数,
为气体摩尔常数,![]() 为开尔文温度,
为开尔文温度,![]() 为活化能
为活化能![]() ]。
]。![]() 反应达到平衡后,升高温度,正反应速率常数增大的倍数_____(填“大于”“小于”或“等于”)逆反应速率常数增大的倍数。
反应达到平衡后,升高温度,正反应速率常数增大的倍数_____(填“大于”“小于”或“等于”)逆反应速率常数增大的倍数。
(4)一定温度下,在2 L恒容密闭容器中充入2 mol NO(g)、![]() 发生上述反应,混合气体压强随着时间变化关系如图所示。
发生上述反应,混合气体压强随着时间变化关系如图所示。
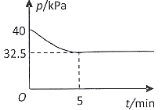
①05 min 内![]() 的平均速率
的平均速率 ![]() =___________________
=___________________![]() 。
。
②该温度下,上述反应的平衡常数![]() =________________
=________________![]() 。
。
③其他条件不变,在10min时向反应体系中再充入1mol NO、![]() ,达到新平衡时NO的平衡转化率 ________________(填“增大”“减小”或“不变”)。
,达到新平衡时NO的平衡转化率 ________________(填“增大”“减小”或“不变”)。
(5)工业上,可以采用电化学方法处理NO。以惰性材料为电极,以硝酸铵溶液为电解质溶液并补充![]() ,电解反应为
,电解反应为![]() 。电解过程中,阳极的电极反应式为_______________________。
。电解过程中,阳极的电极反应式为_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】烷、烯、炔都是常见的碳氢化合物。
(1)写出下列有机物的系统命名法名称:
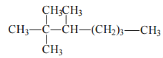 名称是______________________________
名称是______________________________
(2)有下列有机物:①CH3CH3②CH2=CH2③CH3-CH2-C≡CH④CH3-C≡C-CH3⑤C2H6⑥CH3-CH=CH2,其中互为同系物的是__________,互为同分异构体的是_________(填编号)
(3)实验室常用浓硫酸和乙醇混合加热制取乙烯。
①实验室制乙烯的化学方程式为_____________________________________。
②关于该实验的说法中正确的是(________)
a.浓硫酸只有催化剂的作用 b.可用向下排空气法收集乙烯
c.在反应容器中放入几片碎瓷片防止混合液暴沸 d.温度计应插入反应溶液液面下,以便控制温度
③实验后期制得的乙烯气体中常含有杂质气体![]() 和
和![]() ,将此混合气体直接通入溴水中,若观察到溴水褪色,能否证明乙烯发生了加成反应?__________(填“能”或“否”),原因是_________________________________________________________。
,将此混合气体直接通入溴水中,若观察到溴水褪色,能否证明乙烯发生了加成反应?__________(填“能”或“否”),原因是_________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
![]()
A.金属性:甲>乙>丁
B.原子半径:辛>己>戊
C.丙与庚的原子核外电子数相差3
D.乙的单质在空气中燃烧生成只含离子键的化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、C原子序数依次递增,它们的原子的最外层电子数之和为10。A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数。下列叙述正确的是( )
A. 原子半径A<B<C
B. A的氢化物的稳定性小于C的氢化物的稳定性
C. C的氧化物的熔点比A的氧化物的低
D. A与C可形成原子晶体
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是( )
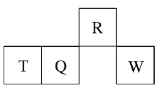
A. 最简单气态氢化物的热稳定性:R>Q
B. 最高价氧化物对应水化物的酸性:Q<W
C. 原子半径:T>Q>R
D. 单质T与NaOH溶液不反应
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.由三种常见元素组成的化合物A,按如下流程进行实验。气体B、C、D均无色、无臭,B、D是纯净物;浓硫酸增重3.60g,碱石灰增重17.60g;溶液F焰色反应呈黄色。
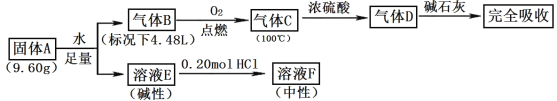
请回答:
(1)组成A的非金属元素是_____,气体B的结构简式_____。
(2)固体A与足量水反应的化学方程式是_____。
(3)一定条件下,气体D可能和FeO发生氧化还原反应,试写出一个可能的化学方程式_____。
Ⅱ.某兴趣小组为验证卤素单质的氧化性强弱,向NaBr溶液中通入一定量Cl2,将少量分液漏斗中溶液滴入试管中,取试管振荡,静止后观察现象。实验装置如图:
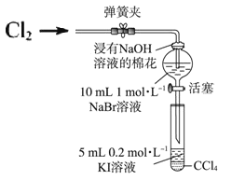
(4)说明氧化性 Br2>I2 的实验现象是_____。
(5)为了排除Cl2对溴置换碘实验的干扰,需确认分液漏斗中通入Cl2 未过量。试设计简单实验方案检____。
查看答案和解析>>
科目: 来源: 题型:
【题目】W、Q、X、Y、Z为短周期元素且原子序数依次增大,X原子的K层电子数与M层电子数相等,Y是常用的灰黑色半导体材料,通常状态下YW4呈气态。下图是晶体Y的一种制备路线图。有关说法正确的是
![]()
A. 标准状况下,WZ为液态B. 原子半径大小为W<X<Y
C. YQ2和YW4均只含极性共价键D. 氢化物的稳定性为Q>Y>Z
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 == 2Na2CO3 + O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和过氧化钠为原料,制取O2,设计出如下实验装置:

(1)A中制取CO2 的装置,应从下列图①、② 中选哪个图:________。

A装置中发生反应的离子方程式为 ______________________________。
(2)B装置的作用是________________,C装置内可能出现的现象是__________ 。为了检验E中收集到的气体,在取出集气瓶后,__________________________(简要表述操作过程及结论)。
(3)若E中的石灰水出现轻微白色浑浊,请说明原因:_______________ (用离子方程式及简要文字描述)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com