
科目: 来源: 题型:
【题目】25℃时,向25ml氢氧化钠标准溶液中逐滴加入0.2mol·L1的一元酸HA溶液,PH变化曲线如下图所示:
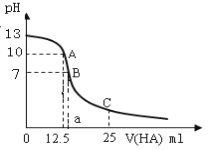
(1)该氢氧化钠溶液的物质的量浓度为__________mol·L1。
(2)A点对应酸的体积为12.5ml,则所得混合溶液中由水电离出的c(OH)= _______mol·L1。
(3)HA是____酸(选填“强”、“弱”)。
(4) 在B点所得混合溶液中,c(Na+)、c(A)、c(H+)、c(OH) 的大小的顺序是_____________。
(5)在C点所得混合溶液中,下列说正确的是________。
A.HA的电离程度小于NaA的水解程度
B.离子浓度由大到小的顺序是c(Na+)>c(A)>c(H+)>c(OH)
C.c(Na+) + c(H+) = c(A-) + c(OH)
D.c(HA) + c(A) = 0.2mol·L1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列4组物质,能起反应的写出化学方程式;属于离子反应的,还要写出离子方程式;不能起反应的,说明不能起反应的原因。
(1)硫酸溶液与氯化钡溶液:_______________________________________;
(2)稀硫酸与碳酸钠溶液:_______________________________________;
(3)硝酸钠溶液与氯化钾溶液:_______________________________________;
(4)碳酸钙和盐酸:_______________________________________________________;
(5)氢氧化钾溶液和醋酸(CH3COOH)溶液:___________________________________;
(6)三氯化铁溶液和氢氧化钾溶液:__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组利用如图装置探究SO2和Fe(NO3)3溶液的反应原理。下列说法错误的是( )
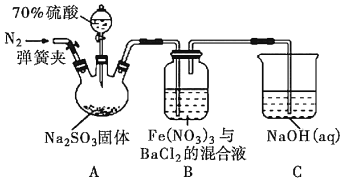
A.装置B中若产生白色沉淀,说明Fe3+能将SO2氧化成SO![]()
B.实验室中配制加70%的硫酸需要的玻璃仪器有量筒、烧杯、玻璃棒
C.三颈烧瓶中通入N2的操作应在滴加浓硫酸之前,目的是排尽装置内的空气
D.装置C可能发生倒吸,同时还不能完全吸收反应产生的尾气
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)参加反应的HNO3和作为氧化剂的HNO3的个数比为________。
(2)若有64 g Cu被氧化,则被还原的HNO3的质量是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.中和滴定
(1)用酸式滴定管量取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加1~2滴酚酞作指示剂,用0.20 mol·L-1NaOH标准溶液进行滴定。为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00 mL,三次实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗NaOH溶液体积/mL | 19.00 | 23.00 | 23.02 |
该盐酸的浓度约为_____________(保留两位有效数字)。滴定达到终点的标志是_____________。
(2)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。
A. 滴定终点读数时俯视读数
B. 酸式滴定管使用前,水洗后未用待测盐酸润洗
C. 锥形瓶水洗后未干燥
D. 配制NaOH标准溶液时,没有等溶解液降至室温就转移至容量瓶中
E. 配制NaOH标准溶液时,定容时仰视容量瓶的刻度线
F. 碱式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.(1)在粗制CuSO4·5H2O晶体中常含有杂质Fe2+。在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质可采用的是________
A. KMnO4 B. H2O2 C. 氯水 D. HNO3
(2)然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3,可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的_______。
A. NaOH B. NH3·H2O C. CuO D. Cu(OH)2
(3)常温下Fe(OH)3的溶度积Ksp=8.0×10-38,Cu(OH)2的溶度积Ksp=3.0×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0 mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为_______,Fe3+完全沉淀时溶液的pH为________(已知 lg5 = 0.7 )
查看答案和解析>>
科目: 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用千冶金染料、皮革等工业。硫化钠的一种制备方法是Na2SO4+2C![]() Na2S+2CO2↑。下列有关说法正确的是( )
Na2S+2CO2↑。下列有关说法正确的是( )
A.12g石墨晶体中含有碳碳键的数目为3NA
B.1L0.1molL-1Na2S溶液中含阴离子的数目小于0.lNA
C.生成1mol氧化产物时转移电子数为4NA
D.常温常压下,11.2LCO2中含质子的数目为11NA
查看答案和解析>>
科目: 来源: 题型:
【题目】多巴胺是一种神经传导物质,会传递兴奋及开心的信息。其部分合成路线如下,下列说法正确的是
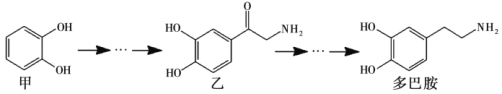
A. 甲在苯环上的溴代产物有2种
B. lmol乙与H2发生加成,最多消耗3molH2
C. 多巴胺分子中所有碳原子可能处在同一平面
D. 甲、乙、多巴胺3种物质均属于芳香烃
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达平衡后,降低温度,A的体积分数将减小。
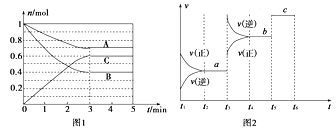
(1)该反应的化学方程式为____________________________。
(2)该反应的反应速率v随时间t的关系如上图2所示:
①根据上图判断,在t3时刻改变的外界条件是______________。
②a、b、c三点中,C的体积分数最大的是________。
③各阶段的平衡常数如下表所示:
t2~t3 | t4~t5 | t5~t6 |
K1 | K2 | K3 |
K1、K2、K3之间的大小关系为________(用“>”、“<”或“=”连接)。
Ⅱ.在密闭容器中充入一定量的H2S,发生反应2H2S(g) ![]() 2H2(g)+S2(g) ΔH,如图所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
2H2(g)+S2(g) ΔH,如图所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
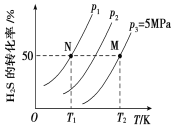
(1)△H_________ (填“>”“<”或“ = ”)0。
(2)图中压强(p1、p2、p3)的大小顺序为________________。
(3)图中M点的平衡常数Kp =_______MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)如果想进一步提高H2S的转化率,除改变温度、压强外,还可以采取的措施有___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以含锂电解铝废渣(主要成分为LiF、AlF3、NaF,少量CaO等)为原料,生产高纯度LiOH的工艺流程如图:(已知:常温下,LiOH可溶于水,Li2CO3微溶于水)

(1)含锂电解铝废渣与浓硫酸在200~400℃条件下反应2h。“滤渣1”主要成分是___(填化学式)。
(2)“过滤2”需要趁热在恒温装置中进行,否则会导致Li2SO4的收率下降,原因是___。
(已知部分物质的溶解度数据见下表)
温度/℃ | Li2SO4/g | Al2(SO4)3/g | Na2SO4/g |
0 | 36.1 | 31.2 | 4.9 |
10 | 35.4 | 33.5 | 9.1 |
20 | 34.8 | 36.5 | 19.5 |
30 | 34.3 | 40.4 | 40.8 |
40 | 33.9 | 45.7 | 48.8 |
(3)40°C下进行“碱解”,得到粗碳酸锂与氢氧化铝的混合滤渣,生成氢氧化铝的离子方程式为___;若碱解前滤液中c(Li+)=4molL-1,加入等体积的Na2CO3溶液后,Li+的沉降率到99%,则“滤液2”中c(CO32-)=___molL-1。[Ksp(Li2CO3)=1.6×10-3]
(4)“苛化”过程,若氧化钙过量,则可能会造成___。
(5)整个工艺流程中可以循环利用的物质有___。
(6)“电解”原理如图所示。“碳化”后的电解液应从(填“a”或“b”)___口注入。阴极的电极反应式为___。
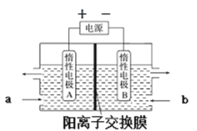
(7)高纯度LiOH可转化为电池级Li2CO3。将电池级Li2CO3和C、FePO4高温下反应,生成LiFePO4和一种可燃性气体,该反应的化学方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某废催化剂含SiO2、ZnO、ZnS和CuS。实验室从该废催化剂中回收锌和铜的一种流程如下图所示。
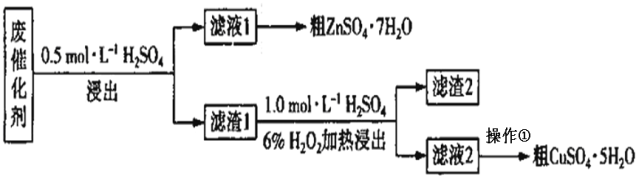
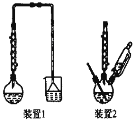
浸出使用的装置如图所示。回答下列问题:
 蒸发浓缩、冷却结晶蒸发浓缩、冷却结晶
蒸发浓缩、冷却结晶蒸发浓缩、冷却结晶
(1)第一次浸出必须选用装置 _______(填“1”或“2”),原因是 ________。滤渣1的主要成分有_______。
(2)第二次浸出时生成单质硫,写出反应的离子方程式:_______________。该步骤即使加热温度不高也可能会有副反应发生,产物之一是空气的主要成分,分析可能原因是_____________________ 。
(3)从滤液2中得到CuSO4·5H2O的操作是 __________ 、过滤、洗涤。
(4)下列叙述中涉及到与该流程中的“操作①”相同操作的是_____________ 。
A.《肘后备急方》中治疟疾:“青蒿一握,以水升渍,绞取汁,尽服之”
B.《本草衍义》中精制砒霜:“将生砒就置火上,以器覆之,令砒烟上飞着覆器”
C.《开宝本草》中获取硝酸钾:“冬月地上有霜,扫取以水淋汁后,乃煎炼而成”
D. 《本草纲目》中烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”
(5)若该废催化剂中含12.8%的CuS,实验中称取15.0g废催化剂最终得到3.0gCuSO4·5H2O,则铜的回收率为 __________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com