
科目: 来源: 题型:
【题目】工业制硝酸中的一步重要反应是NH3在加热条件下催化氧化:4NH3+5O2![]() 4NO+6H2O这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下列说法中错误的是
4NO+6H2O这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下列说法中错误的是
A.使用催化剂可以加快反应速率,提高生产效率
B.适当提高O2的浓度可以提高NH3的转化率
C.升高温度,正反应速率增大、逆反应速率减小
D.NH3的转化率为最大值时,该反应达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A.无色透明的溶液中:OH-、Na+、CrO![]() 、SO
、SO![]()
B.c(S2O![]() )=0.1mol·L-1的溶液中:Na+、K+、CO
)=0.1mol·L-1的溶液中:Na+、K+、CO![]() 、SO
、SO![]()
C.水电离出的c(H+)=1.0×10-13mol·L-1的溶液中:Na+、Mg2+、HSO![]() 、NO
、NO![]()
D.能使蓝色石蕊试纸变红的溶液中:Na+、NH![]() 、
、 、Cl-
、Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】新型冠状病毒爆发时刻,更能体现化学知识的重要性。下列有关消毒剂的说法中正确的是( )
A.各类消毒剂浓度越大,消毒效果越好
B.为了增强消毒效果,可以将医用酒精、“84”消毒液混用
C.过氧乙酸的结构简式为CH3COOOH,含有-1价氧元素,具有氧化性
D.各类消毒剂均能使病毒蛋白质变性,但是对人体蛋白质无影响
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化铍(BeO)常温下为不溶于水、易溶于强酸和强碱的固体,除用作耐火材料外,还可以用于制霓虹灯和铍合金。工业上以硅铍石(主要含有BeO、SiO2、MgO,还含有少量Al2O3和Fe2O3)制备高纯度BeO的流程如图所示:
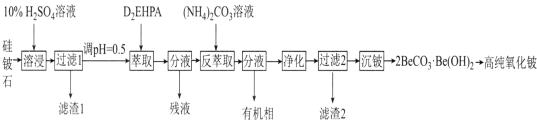
已知:①BeO为离子化合物,熔点为2350℃,BeC12和NaC1等比例混合的固体混合物在350℃即可熔化;
②不同金属阳离子在D2EHPA中的溶解性如下表所示:
Be2+ | Mg2+ | Fe3+ | Al3+ | |
D2EHPA中的溶解性 | 易溶 | 难溶 | 微溶 | 微溶 |
请回答下列问题:
(1)“滤渣1”的主要成分为__(填化学式)。“残液”中含量最多的金属元素为__(填名称)。
(2)“萃取”后铍元素以Be(HX2)2的形式存在于有机相中,“反萃取”后以(NH4)2Be(CO3)2的形式存在于水相中,则“反萃取”时含铍微粒发生反应的化学方程式为___。
(3)“净化”时需将反萃取液加热到70℃,加热到70℃的目的为__。
(4)由2BeCO3·Be(OH)2制备高纯BeO的方法是__。
(5)BeO的电子式为__。工业上常采用电解熔融BeC12与NaC1等比例混合物的方法制备金属Be,不采用电解熔融BeO制备的主要原因为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸钠![]() 是一种工业盐,外观与食盐相似。下面是某学习小组设计的
是一种工业盐,外观与食盐相似。下面是某学习小组设计的![]() 制取实验和纯度检验实验。该小组收集了相关资料:
制取实验和纯度检验实验。该小组收集了相关资料:
![]() 和
和![]() 溶液反应生成
溶液反应生成![]() 和
和![]() 为淡黄色接近白色固体,在水中形成沉淀
为淡黄色接近白色固体,在水中形成沉淀![]()
Ⅰ![]() 亚硝酸钠的制取实验
亚硝酸钠的制取实验
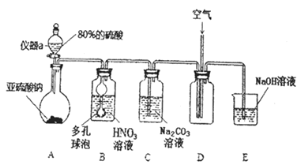
![]() 仪器a的名称为___________,A装置中发生的化学反应方程式为________________。
仪器a的名称为___________,A装置中发生的化学反应方程式为________________。
![]() 装置中多孔球泡的作用_________________________。
装置中多孔球泡的作用_________________________。
![]() 若装置B中逸出的NO与
若装置B中逸出的NO与![]() 气体物质的量之比为
气体物质的量之比为![]() ,则装置B中发生反应的化学方程式为_______。
,则装置B中发生反应的化学方程式为_______。
![]() 实验过程中需控制C装置中溶液
实验过程中需控制C装置中溶液![]() ,否则C中生成的
,否则C中生成的![]() 的产量会下降,理由是_______________。
的产量会下降,理由是_______________。
![]() 请根据题干所给信息设计实验证明C装置中有
请根据题干所给信息设计实验证明C装置中有![]() 产生:__________。
产生:__________。 ![]() 限选用的试剂:稀硝酸、硝酸银溶液、NaOH溶液
限选用的试剂:稀硝酸、硝酸银溶液、NaOH溶液![]()
Ⅱ![]() 亚硝酸钠的纯度检验
亚硝酸钠的纯度检验
已知:![]()
![]()
![]()
![]()
![]()
![]() 反应结束后C中溶液通过结晶获得
反应结束后C中溶液通过结晶获得![]() 粗产品mg,溶解后稀释至250mL,分别取
粗产品mg,溶解后稀释至250mL,分别取![]() 用
用![]() 的酸性
的酸性![]() 溶液平行滴定三次,平均每次消耗酸性
溶液平行滴定三次,平均每次消耗酸性![]() 溶液的体积为VmL。则粗产品中
溶液的体积为VmL。则粗产品中![]() 的质量分数为_______
的质量分数为_______![]() 用含c、V、m的式子表示
用含c、V、m的式子表示![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】阿伏伽德罗常数的值为NA,下列说法正确的是( )
A.在常温常压下, lmol 氦气含有的原子数目为2NA
B.7. 1克氯气通入足量的氢氧化钠溶液中,转移的电子数为0.2NA
C.标准状况下,2.24L N2和O2的混合气体中原子数为0.2NA
D.标准状况下,2.24LHCl溶于500mL水中所得溶液浓度为2mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】把6.5gZn放入足量的盐酸中,锌完全反应。计算:
(1)6.5gZn的物质的量?_________。
(2)参加反应的HCl的物质的量?_________。
(3)生成氢气的体积(标准状况)?__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“套管实验”是将一个较小的玻璃仪器装入另外一个玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验。因其具有许多优点,近年被广泛开发并应用于化学实验中。下述实验为“套管实验”,请观察如图所示实验装置,分析实验原理,回答下列问题:
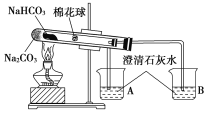
(小试管内塞有沾有无水硫酸铜粉末的棉花球)
(1)从点燃酒精灯开始,试管及烧杯B中能观察到的现象有____________________。
(2)通过该实验可得出的结论是_________________________________。
(3)本装置的优点是_______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面科普信息,回答问题:
一个体重50kg的健康人含铁2g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是_________
A.Fe B.Fe2+ C.Fe3+
(2)工业盐中毒后,可以服用维生素C来缓解中毒状况,这说明维生素C具有______性。
(3)在Fe+4HNO3(稀)═Fe(NO3)3+NO+H2O↑的反应中,用双线桥法表示电子的转移____________,反应中HNO3表现出了______性和______性,则1molFe参加反应时,被还原的HNO3为_________mol,转移电子数为________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】石油裂解气主要含有丙烯、1,3-丁二烯等不饱和烃,以它们为原料可合成CR橡胶和医药中间体G,合成路线如下:
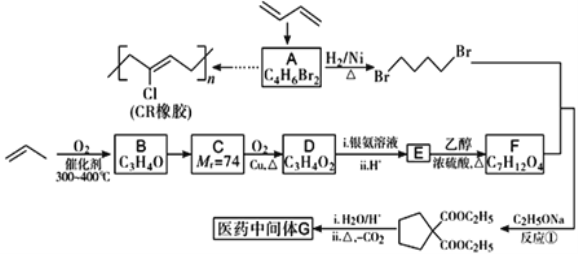
已知:①B、C、D 均能发生银镜反应;
②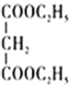
![]()
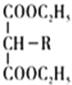
![]() RCH2COOH
RCH2COOH
(1)A的顺式异构体的结构简式为_______。
(2)C中含氧官能团的名称是________,反应①的反应类型为_______。
(3)写出E→F反应的化学方程式:_________。
(4)写出同时满足下列条件的医药中间体G的同分异构体的结构简式: _______。
①与D 互为同系物; ②核磁共振氢谱有三组峰。
(5)用简要语言表述检验B中所含官能团的实验方法:_______。
(6)以A为起始原料合成CR橡胶的线路为______(其它试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com