
科目: 来源: 题型:
【题目】美托洛尔可用于治疗高血压及心绞痛,某合成路线如下:

已知:R1OH+R2-Cl![]() R1OR2+HCl
R1OR2+HCl
(1)写出化合物C中的含氧官能团名称___________。
(2)下列说法正确的是___________。
A.C→D的反应类型是氧化反应
B.G的分子式为C12H14O3
C.试剂X在NaOH溶液中能水解
D.美托洛尔既能与盐酸反应又能与Na2CO3溶液反应
(3)写出E→F的化学方程式_______。
(4)写出化合物B的相邻同系物(C9H10O2)的同分异构体结构简式,且必须符合下列条件:_。
①含有苯环,能发生银镜反应 ②1H—NMR表明,分子中共有4种H原子
(5)结合题中信息,请设计以苯甲酸和苯酚为原料制备![]() 的合成路线(用流程图表示,无机试剂任选)_____________。
的合成路线(用流程图表示,无机试剂任选)_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,CH3COOH溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,下列说法正确的是( )
CH3COO-+H+,下列说法正确的是( )
A. 向10mLpH=5的CH3COOH溶液中加水至10L,最后溶液pH在7和8之间
B. 加入少量CH3COONa固体,平衡向左移动,c(CH3COO-)下降
C. 加入少量NaOH固体(忽略溶解热效应),平衡向右移动,水的电离程度也随之增大
D. 向10mLpH=5的CH3COOH溶液中加入等体积,等浓度的盐酸,混合溶液的c(H+)不变
查看答案和解析>>
科目: 来源: 题型:
【题目】次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性。回答下列问题:
(1)①H3PO2属于一元中强酸,酸性略强于亚硫酸,写出其电离方程式_________
②下列说法正确的是_________
A.NaH2PO2溶液显弱碱性
B.向NaH2PO2溶液中滴加硝酸可以制得H3PO2
C.1molH3PO2最多可以和3molNaOH发生反应
D.NaH2PO2溶液中:c(Na+)=c(H3PO2)+c(H2PO2-)
(2)H3PO2可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过):

①写出阳极反应式_________
②A、B、C分别是_________离子交换膜、_________离子交换膜、_________离子交换膜(填“阴”或“阳”)
③阳极室中溶液pH _________(填变大、变小或不变)
查看答案和解析>>
科目: 来源: 题型:
【题目】4-乙氧基乙酰乙酰苯胺(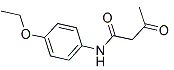 ),简称AAPP,常用作染料、有机颜料中间体。其合成路线如下:
),简称AAPP,常用作染料、有机颜料中间体。其合成路线如下:
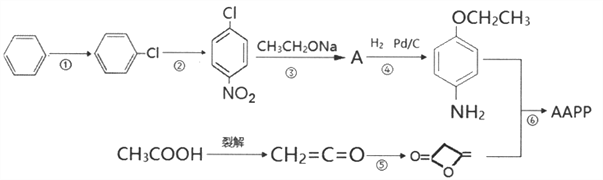
已知: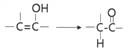
回答下列问题:
(1)下列有关说法正确的是_________
A.反应③是取代反应,反应⑤是加成反应
B.1mol苯完全燃烧需要6molO2
C.CH3COOH不能与新制Cu(OH)2浊液反应
D.CH2=C=O在一定条件下能生成乙醇
(2)反应②的反应条件是_________
(3)A的结构简式_________
(4)反应⑥的化学方程式_________
(5)![]() 有多种同分异构体,写出三种符合下列要求的同分异构体_________
有多种同分异构体,写出三种符合下列要求的同分异构体_________
a.链状化合物 b.能发生银镜反应,但不能在稀硫酸中水解 c.不能与Na反应
查看答案和解析>>
科目: 来源: 题型:
【题目】次硫酸氢钠甲醛(NaHSO2·HCHO·2H2O,M=154.0g·mol-1)俗称吊白块,易溶于水,微溶于乙醇,在120℃以上易分解。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
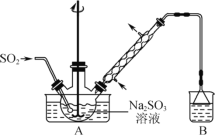
步骤1:在三颈烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH 约为4,制得NaHSO3溶液。
步骤2:向三颈烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80℃~90℃下,反应约3h,冷却至室温,抽滤。
步骤3:将滤液经结晶、抽滤、洗涤等操作后制得粗产品。
(1)步骤2中加入锌粉反应时会有Zn(OH)2生成,写出发生反应的化学方程式_____________;为防止生成的Zn(OH)2覆盖在锌粉表面阻止反应进行,可采取的措施是_____________。
(2)下列说法中不正确的是_____________。
A.装置B的作用是吸收尾气
B.该实验的加热方式最好选用水浴加热
C.步骤2抽滤的滤渣成分只有Zn(OH)2固体
D.步骤3得到的产品可以在烘箱中高温烘干
(3)如图装置,经过一系列操作完成步骤3中的结晶和洗涤操作。请选择合适的字母,按正确的操作顺序补充完整(洗涤操作只需考虑一次):_____→固液转移至布氏漏斗→开抽气泵→c→f→________→_________→_________→________→d→关抽气泵。_____________
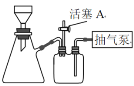
a.将滤液蒸发至大量晶体出现
b.将滤液真空浓缩,冷却结晶
c.关闭活塞A
d.打开活塞A
e.加乙醇洗涤
f.确认抽干
(4)将0.5000g样品充分加热分解,释放出的HCHO用36.00mL0.1000mol·L-1KMnO4溶液吸收(不考虑SO2的影响,5HCHO+4![]() +12H+=5CO2↑+4Mn2++11H2O),再用0.1000mol·L-1H2C2O4溶液滴定KMnO4溶液,重复实验3次,平均消耗H2C2O4溶液的体积为30.00mL,则样品的纯度为_____________。
+12H+=5CO2↑+4Mn2++11H2O),再用0.1000mol·L-1H2C2O4溶液滴定KMnO4溶液,重复实验3次,平均消耗H2C2O4溶液的体积为30.00mL,则样品的纯度为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.无机盐A由4种常见的元素组成,为探究A的组成,设计并完成如下实验:
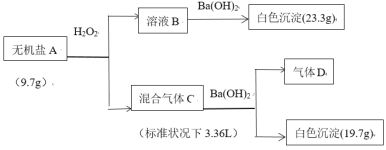
已知:D为单质,在标准状况下的密度为1.25g/L;溶液B显酸性。
(1)写出组成A的金属元素在周期表中的位置______________。
(2)气体D的电子式为______________。
(3)写出A与H2O2反应的离子方程式______________。
Ⅱ.某小组设计实验探究在适当温度和催化剂条件下SO2与O2反应后混合气体的成分:
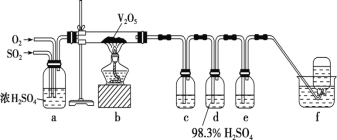
(1)c中盛放的试剂是______________;e中盛放的试剂是______________。
(2)某同学提出用饱和的Na2SO3溶液代替98.3%的浓H2SO4,请评价该方案是否可行______________,若可行不必说明理由;若不可行,简述其理由______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组的同学取一定量的Al和Fe2O3的混合物进行铝热反应,并探究熔落物的成分。已知:Al、Fe的熔、沸点数据如下。
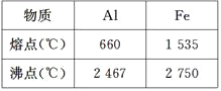
请回答下列问题:
(1)某同学猜测,铝热反应所得到的熔落物是铁铝合金。理由:该反应放热能使铁熔化,而铝的熔点比铁低,所以铁和铝能形成合金。你认为他的解释是否合理?__(选填“合理”或“不合理”)。设计一个简单的实验方案,证明上述所得的熔落物中含有金属铝:__。
(2)另外一名同学观察到熔落物呈黑色,他认为铝热反应中有少量Fe3O4生成,该同学设计如下实验验证他的结论:取少量熔落物,用稀硫酸溶解,加水稀释后滴加3~4滴KSCN溶液。若溶液变为红色,则有Fe3O4生成;否则没有Fe3O4生成。该同学的实验方案是否合理?____说明你的理由____。
查看答案和解析>>
科目: 来源: 题型:
【题目】检测血液中的Ca2+能够帮助判断多种疾病。某研究小组测定血液样品中Ca2+的含量(l00mL血液中含Ca2+的质量),实验步骤如下:
①准确量取5.00mL血液样品,处理后配制成50.00mL溶液;
②准确量取溶液10.00mL,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀;
③过滤并洗净所得CaC2O4沉淀,用过量稀硫酸溶解,生成H2C2O4和CaSO4稀溶液;
④加入12.00mL0.0010mol·L-1的KMnO4溶液,使H2C2O4完全被氧化,离子方程式为:2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;
⑤用0.0020mol·L-1 (NH4)2Fe(SO4)2溶液滴定过量的KMnO4溶液,消耗(NH4)2Fe(SO4)2溶液的体积如图所示,离子方程式为:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O
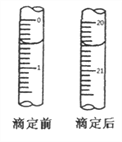
回答下列问题:
(1)已知H2C2O4属于二元弱酸,下列说法正确的是_________
A.H2C2O4 溶液中:c(H+)=c(HC2O4-)+ c(C2O42-)+ c(H2C2O4)
B.相同温度下,等物质的量浓度的(NH4)2C2O4和(NH4)2Fe(SO4)2溶液,c(NH4+)前者小于后者
C.(NH4)2C2O4 溶液中:c(NH4+)+c(NH3·H2O)=2c(HC2O4-)+2c(C2O42-)+ 2c(H2C2O4)
D.(NH4)2Fe(SO4)2溶液:c(SO42-)>c(NH4+)>c(Fe2+)>c(OH-)>c(H+)
(2)实验中发现向草酸溶液中逐滴加入酸性高锰酸钾溶液,溶液褪色开始时缓慢,一段时间后迅速加快,利用水浴使反应液保持恒温时也是如此,出现该现象的可能原因是_________
(3)12.00mL0.0010mol·L-1的KMnO4溶液应用_________量取(填“酸式”或“碱式”滴定管)
(4)到达滴定终点时的现象是_________
(5)若步骤⑤滴定管在使用前未用标准(NH4)2Fe(SO4)2溶液洗涤,测得血液中Ca2+的含量将_________ (填“偏高”、“偏低”或“无影响”)。
(6)计算血样中Ca2+的含量_________ g/100mL
查看答案和解析>>
科目: 来源: 题型:
【题目】0.05mol某有机物A和0.125molO2在一密闭容器中充分燃烧,所得产物通过浓H2SO4时使其增重2.7g;再通过足量灼热的CuO粉末,固体质量减小了0.8g;最后通过足量碱石灰,固体质量增加了6.6g。
(1)该化合物A的分子式______________。(写出计算过程)
(2)若0.05mol含有醛基的有机物B与有机物A的最简式相同,且在0.125molO2中能完全燃烧,写出B所有可能的结构简式______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】海带中含有丰富的碘。为了从海中提取碘,某研究性学习小姐设计并进行了以下实验,请填写下列空白:

(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是___(用标号字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是___,步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是__。
(3)步骤④反应的离子方程式是___。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是__、___。
(5)请设计一种检验提取碘后的水溶液中是否还有单质碘的简单方法:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com