
科目: 来源: 题型:
【题目】(1)某学习小组用0.80 mol/L标准浓度的烧碱溶液测定未知浓度的盐酸。
①用滴定的方法来测定盐酸的浓度,实验数据如下所示:
实验编号 | 待测HCl溶液的体积/mL | 滴入NaOH溶液的体积/mL |
1 | 20.00 | 22.00 |
2 | 20.00 | 22.10 |
3 | 20.00 | 21.90 |
该未知盐酸的浓度为_____________(保留两位有效数字)
②滴定管如下图所示,用___________滴定管盛装标准浓度的氢氧化钠溶液 (填“甲”或“乙”)。
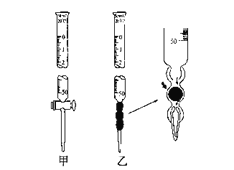
③下列操作会使所测得的盐酸的浓度偏低的是______________。
A.盛装待测液的锥形瓶用水洗后未干燥
B.滴定前,碱式滴定管尖端有气泡,滴定后气泡消失
C.碱式滴定管用蒸馏水洗净后,未用标准氢氧化钠溶液润洗
D.读碱式滴定管的刻度时,滴定前仰视凹液面最低处,滴定后俯视读数
(2)某课外活动小组为了测定某氯化锶(SrCl2)样品的纯度,设计了如下方案:
称取1.0 g样品溶解于适量水中,向其中加入含AgNO32.38 g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2 mol·L-1的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定氯化锶样品的纯度。
请回答下列问题:
①判断滴定达到终点的现象是___________________。
②考虑Ag+和Fe3+在酸或碱性溶液中的存在形式,在实施滴定的溶液以呈_____________(选填“酸性”“中性”或“碱性”)为宜。
③在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果_____________(选填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在托盘天平两盘上分别放有盛有等质量的足量稀盐酸的烧杯,调整天平至平衡。向左边烧杯中加入10.8 g镁条,向右边烧杯中加入10.8 g铝条(两金属外形相同,表面均经过砂纸打磨处理)。反应过程中指针偏转情况正确的是( )
A.先偏左,最后偏右B.先偏右,最后偏左
C.先偏左,最后平衡D.先偏右,最后平衡
查看答案和解析>>
科目: 来源: 题型:
【题目】下列五种物质中,①Ar ②CO2 ③SiO2 ④Ba(OH)2 ⑤K2S,含有共价键的物质有________(填序号)。分别写出CO2、Ba(OH)2的电子式________、________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某元素的一种同位素X的原子质量数为A,含N个中子,它与![]() 原子组成HmX分子.在a克HmX中所含质子的物质的量是( )
原子组成HmX分子.在a克HmX中所含质子的物质的量是( )
A. ![]() (A-N+m)molB.
(A-N+m)molB. ![]() (A-N)molC.
(A-N)molC. ![]() (A-N)molD.
(A-N)molD. ![]() (A-N+m)mol
(A-N+m)mol
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质与其用途不完全符合的有( )
①干冰—人工降雨;②Na2CO3—制玻璃;③Fe2O3—红色油漆或涂料;④Al2O3—耐火材料;⑤NaClO—净水剂⑥NaHCO3—制食品发泡剂;⑦KAl(SO4)2—消毒、净水。
A.⑤⑦B.②④⑥⑧C.③④D.①③⑤⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】俗名为“臭碱”的硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化钠的一种制备方法是Na2SO4+2C![]() Na2S+2CO2↑。下列有关说法正确的是( )(设NA表示阿伏加德罗常数的值)
Na2S+2CO2↑。下列有关说法正确的是( )(设NA表示阿伏加德罗常数的值)
A.Na2SO4和Na2S均为离子晶体,晶体中每个SO![]() 或S2-周围均有2个Na+
或S2-周围均有2个Na+
B.C(金刚石)属于共价晶体,1mol该晶体中含的σ键数目为4NA
C.生成1mol氧化产物时转移电子数为4NA
D.标准状况下22.4LCO2中含π键的数目为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z均为短周期元素且原子序数依次增大,它们的原子最外层电子数为互不相等的奇数,Y与W形成的阴离子(如图所示)中W不满足8电子稳定结构,W与Z的最高价之和为8。下列说法中正确的是( )

A.W、X、Z可形成离子化合物
B.Z2O是某种弱酸的酸酐,且为直线型分子
C.W与X形成的二元化合物只能含极性键
D.X、Z形成氧化物对应水化物的酸性:Z>X
查看答案和解析>>
科目: 来源: 题型:
【题目】氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气放出,下列叙述不正确的是( )
A.NH4H是离子化合物,含有离子键和共价键
B.NH4H与水反应时,NH4H是还原剂
C.NH4H投入少量的水中,有两种气体产生
D.NH4H溶于水,所形成的溶液成酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A.不是所有的共价键都具有方向性
B.N≡N键能大于C≡C的键能,所以N≡N不易发生加成反应
C.根据价层电子对互斥理论可知,OF2分子的构型和H2O分子的构型相同
D.Na原子基态核外电子占有3个能层,4种能级,6个原子轨道,有6种电子运动状态
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)①常温下,pH=3的盐酸和pH=11的氢氧化钡等体积混合,溶液的pH=____。
②常温下pH=3的盐酸和pH=6的盐酸等体积混合(不考虑混合时溶液的体积变化),溶液的pH=____。(lg2=0.3)
(2)在某温度下,H2O的离子积常数为1×10-13,则该温度下:
①某溶液中的H+浓度为1×10-7mol/L,则该溶液呈___性。
②99mLpH=1的H2SO4溶液与101mLpH=12的KOH溶液混合后(不考虑混合时溶液的体积变化),溶液的pH=___。
(3)今有①CH3COOH、②HCl、③H2SO4三种溶液,用序号回答下列问题:
a.当它们pH相同时,其物质的量浓度由大到小排列是___。
b.当它们的物质的量浓度相同时,其pH由大到小排列是___。
c.中和同一烧碱溶液,需同浓度的三种酸溶液的体积关系为___。(用等式表示)
d.体积和浓度均相同的①、②、③三溶液,分别与同浓度的烧碱溶液恰好完全反应,反应需烧碱溶液的体积关系为___。(用等式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com