
科目: 来源: 题型:
【题目】氮气是制备含氮化合物的一种重要物质,而含氮化合物的用途广泛,如图表示两个常见固氮反应的平衡常数对数值(lg K)与温度的关系:①N2+3H2![]() 2NH3,②N2+O2
2NH3,②N2+O2![]() 2NO。
2NO。

根据图中的数据判断下列说法正确的是( )
A.反应①和②均为放热反应
B.升高温度,反应①的反应速率减小
C.在常温下,利用反应①固氮和利用反应②固氮反应程度相差很大
D.在1 000 ℃时,反应①和反应②体系中N2的浓度一定相等
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如图1:
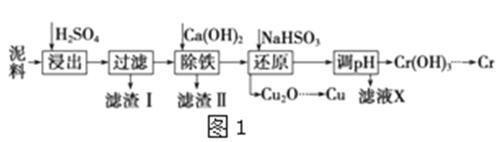
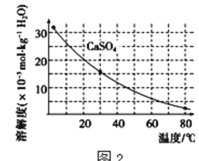
已知部分物质沉淀的pH及CaSO4的溶解度曲线如图2:
Fe3+ | Cu2+ | Cr3+ | |
开始沉淀pH | 2.1 | 4.7 | 4.3 |
完全沉淀pH | 3.2 | 6.7 | a |
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有__;
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:①加入石灰乳调节pH到约__,检验Fe3+已经除尽的操作是__;②将浊液加到80℃,__;
(3)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式__,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是__;
(4)在FeS饱和溶液中存在:FeS(s)![]() Fe2+(aq)+S2-(aq),常温下FeS的Ksp=6.25×10-18。又知FeS饱和溶液中c(H+)与c(S2-)之间存在以下限量关系:c2(H+)c(S2-)=1.0×10-22,为了使溶液中c(Fe2+)达到1molL-1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)为___。
Fe2+(aq)+S2-(aq),常温下FeS的Ksp=6.25×10-18。又知FeS饱和溶液中c(H+)与c(S2-)之间存在以下限量关系:c2(H+)c(S2-)=1.0×10-22,为了使溶液中c(Fe2+)达到1molL-1,现将适量FeS投入其饱和溶液中,应调节溶液中的c(H+)为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】由合成气制备二甲醚的主要原理如下。下列有关说法正确的是
① CO(g)+2H2(g)![]() CH3OH(g) ΔH1=-90.7 kJ·mol-1
CH3OH(g) ΔH1=-90.7 kJ·mol-1
② 2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ·mol-1
③ CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH3=-41.2 kJ·mol-1
A.将1mol CO(g)和2 mol H2(g)充分反应,反应会放出90.7 kJ能量
B.反应①的ΔS>0
C.反应③使用催化剂,ΔH3减少
D.反应3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g)的ΔH=-246.1 kJ·mol-1
CH3OCH3(g)+CO2(g)的ΔH=-246.1 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】相同温度下,分别在起始体积均为1L的两个密闭容器中发生反应:X2(g)+3Y2(g)![]() 2XY3(g) △H=-akJ/mol 实验测得反应的有关数据如下表。
2XY3(g) △H=-akJ/mol 实验测得反应的有关数据如下表。
容器 | 反应条件 | 起始物质的量/mol | 达到平衡所用时间 /min | 达到平衡过程中的能量变化 | ||
X2 | Y2 | XY3 | ||||
① | 恒容 | 1 | 3 | 0 | 10 | 放热0.1akJ |
② | 恒压 | 1 | 3 | 0 | t | 放热bkJ |
下列叙述正确的是
A. 对于上述反应,①、②中反应的平衡常数K的数值不同
B. ①中:从开始至10min内的平均反应速率υ(X2)=0.1mol/(L·min)
C. ②中:X2的平衡转化率小于10%
D. b>0.1a
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1 mol·L-1,加入等体积0.3 mol·L-1的BaCl2溶液恰好使![]() 完全沉淀,则混合溶液中Na+的浓度为________。
完全沉淀,则混合溶液中Na+的浓度为________。
(2)将0.1 mol·L-1的K2SO4溶液、0.2 mol·L-1的Al2(SO4)3溶液和纯水混合,要使混合液中K+、Al3+、![]() 的浓度分别为0.1 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,则K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比________(忽略体积的变化)。
的浓度分别为0.1 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,则K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比________(忽略体积的变化)。
(3)在标准状况下,将一个充满HCl气体和氧气的集气瓶倒放于盛水的水槽中,水面上升至集气瓶容积的![]() ,把集气瓶从水中取出(假设HCl全部留在集气瓶中),若溶液密度的变化忽略不计,则HCl的物质的量浓度为________ mol·L-1。
,把集气瓶从水中取出(假设HCl全部留在集气瓶中),若溶液密度的变化忽略不计,则HCl的物质的量浓度为________ mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家提出如下光分解法制备氢气:
①2Ce4+(aq)+H2O(l)===2Ce3+(aq)+![]() O2(g)+2H+(aq) ΔH1
O2(g)+2H+(aq) ΔH1
②Ce3+(aq)+H2O(l)===Ce4+(aq)+![]() H2(g)+OH-(aq) ΔH2
H2(g)+OH-(aq) ΔH2
③H2O(l)===H+(aq)+OH-(aq) ΔH3
④2H2O(l)===2H2(g)+O2(g) ΔH4
下列说法正确的是( )
A. Ce4+能够增大水分解反应的活化能,提高反应速率
B. Ce3+是反应②和反应③的催化剂
C. 上述反应中,ΔH4=2ΔH1+4ΔH2-4ΔH3
D. 通常条件下,反应④中生成H2、O2的速率之比为1∶2
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年诺贝尔化学奖授予锂离子电池领域。LiFePO4(磷酸亚铁锂) 是锂离子电池的一种电极材料,可通过下列方法制备:
方法一:2FePO4(s)+Li2 CO3(s)+2C(s)2LiFePO4(s)+3CO(g)
(1)该反应的平衡常数表达式为_____。若在容积不变的容器中,上述反应达到平衡时,一氧化碳的浓度为amolL﹣1,再充入bmol一氧化碳,则平衡向_____方向移动,达到新平衡时,一氧化碳的浓度为_____。
(2)一定温度下,在2L密闭容器中发生上述反应。反应进行到20min时,容器内固体的质量减少了5.6g,则0~20min内一氧化碳的平均反应速率是_____。
方法二:LiFePO4可以通过(NH4)2Fe(SO4)2、H3PO4与Li OH溶液发生共沉淀反应,所得沉淀经80℃真空干燥、高温成型而制得。
(3)氢氧化钠碱性比氢氧化锂碱性强,请用元素周期律知识说明理由_____。
(4)共沉淀反应投料时,不将(NH4)2Fe(SO4)2和LiOH溶液直接混合,其原因是_____。
(5)磷酸亚铁锂电池总反应为:FePO4+Li![]() LiFePO4,放电时,负极为_____(填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为_____。
LiFePO4,放电时,负极为_____(填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述与图象对应符合的是( )

A. 对于达到平衡状态的N2(g)+3H2(g)![]() 2NH3(g)在t0时刻充入了一定的NH3,平衡逆向移动
2NH3(g)在t0时刻充入了一定的NH3,平衡逆向移动
B. P2>P1,T1>T2
C. 该图象表示的方程式为:2A===B+3C
D. 对于反应2X(g)+3Y(g)![]() 2Z(g) ΔH<0,y可以表示Y的百分含量
2Z(g) ΔH<0,y可以表示Y的百分含量
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列填空:硼氧化钠(NaBH4)是合成中常用的还原剂。采用NaBO2为主要原料制备NaBH4(B元素化合价为+3)的反应为:NaBO2+SiO2+Na+H2![]() NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
NaBH4+Na2SiO3(未配平);硅酸钠俗称泡花碱,又名水玻璃,在工业生产中也有广泛应用(已知硅酸为难溶性弱酸)
完成下列填空:
(1)上述反应中,原子最外层有两个未成对电子的元素是_____(填元素符号)。SiO2熔点高的原因是_____。
(2)上述反应中H2与Na的物质的量之比为_____。
(3)硅酸钠水溶液产生硅酸(H2SiO3),硬化粘结,且有碱性,其原因是_____(用离子方程式表示)。铸造工艺中可用氯化铵作为水玻璃的硬化剂。试用平衡原理加以解释_____。
(4)NaBH4可使许多金属离子还原成金属单质。例如它从含金离子(Au3+)的废液中提取Au.配平该反应的离子方程式:_____Au3++_____BH4﹣+_____OH-→_____Au+_____BO2﹣+_____H2O。
(5)最新研究发现以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,则每消耗1L6mol/L H2O2溶液,理论上流过电路中的电子数为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1。某温度下的平衡常数为400。此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如下表。下列说法中不正确的是( )
CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1。某温度下的平衡常数为400。此温度下,在1 L体积不变的密闭容器中加入CH3OH,某时刻测得各组分的物质的量浓度如下表。下列说法中不正确的是( )
物质 | CH3OH | CH3OCH3 | H2O |
c/mol·L-1 | 0.08 | 1.6 | 1.6 |
A. 此时刻反应达到平衡状态
B. 容器内压强不变时,说明反应达平衡状态
C. 平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率不变
D. 平衡时,反应混合物的总能量降低40 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com