
科目: 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法正确的是
A.32 g S8与S6(![]() )的混合物中所含共价键数目为NA
)的混合物中所含共价键数目为NA
B.1 L 0.1 mol·L-1 H2C2O4溶液中含C2O![]() 离子数为0.1NA
离子数为0.1NA
C.2 mol NO与2 mol O2在密闭容器中充分反应,转移的电子数为8NA
D.56g铁片投入足量浓H2SO4中生成NA个SO2分子
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米微晶![]() (碱式碳酸锌)属于高端精细化工产品,晶粒粒度在
(碱式碳酸锌)属于高端精细化工产品,晶粒粒度在![]() ,不溶于水和醇。某高校实验室用工业级硫酸锌(主要成分为
,不溶于水和醇。某高校实验室用工业级硫酸锌(主要成分为![]() ,含少量
,含少量![]() )制备纳米微晶碱式碳酸锌样品的流程如图所示:
)制备纳米微晶碱式碳酸锌样品的流程如图所示:
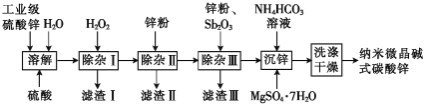
已知:a.![]() 的
的![]() 分别是37.4、15.4、16.2。
分别是37.4、15.4、16.2。
b.残留在溶液中的离子浓度小于![]() 时可认为沉淀完全。
时可认为沉淀完全。
c.滤渣Ⅲ所含主要金属元素是![]() 。
。
(1)“除杂Ⅰ”的目的是除去溶液中的铁元素,则![]() 的作用是________________;若溶液中
的作用是________________;若溶液中![]() ,此过程中还应调节溶液的
,此过程中还应调节溶液的![]() 在____范围(不考虑离子间的相互影响)。
在____范围(不考虑离子间的相互影响)。
(2)“除杂Ⅱ”与“除杂Ⅲ”均为还原除杂。
①滤渣Ⅱ的主要金属元素是_________________________
②“除杂Ⅲ”中加入的![]() 在溶液中主要以
在溶液中主要以![]() 形式存在。请写出锌与
形式存在。请写出锌与![]() 反应生成“金属间化合物”
反应生成“金属间化合物”![]() (
(![]() 中各元素化合价视为0价)的离子方程式:___________________________
中各元素化合价视为0价)的离子方程式:___________________________
(3)“沉锌”后得到的固体先用去离子水洗涤,再用乙醇洗涤。用乙醇洗涤的目的是_______________________
(4)加入![]() 的主要目的是降低样品晶粒粒度,但主元素
的主要目的是降低样品晶粒粒度,但主元素![]() 的质量分数必须在56%以上。若镁、锌的质量比值过高,
的质量分数必须在56%以上。若镁、锌的质量比值过高,![]() 还可能会生成_________(填化学式),从而对样品造成影响。
还可能会生成_________(填化学式),从而对样品造成影响。
(5)样品中锌的含量可用![]() (可表示为
(可表示为![]() )滴定测定,反应的离子方程式为
)滴定测定,反应的离子方程式为![]() 。取
。取![]() 纳米微晶碱式碳酸锌样品,酸溶后得到pH为5~6的溶液,以二甲酚橙作指示剂,用
纳米微晶碱式碳酸锌样品,酸溶后得到pH为5~6的溶液,以二甲酚橙作指示剂,用![]() 标准溶液滴定,消耗
标准溶液滴定,消耗![]() 溶液
溶液![]() ,则样品中锌的质量分数是_______(用代数式表示)。
,则样品中锌的质量分数是_______(用代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有A、B、C、D四种烃,其球棍模型或比例模型如图:
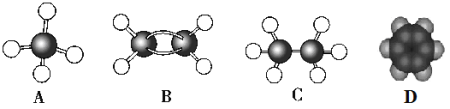
(1)可以用来鉴别A和B的试剂是__________
A、水B、稀硫酸C、溴的四氯化碳溶液D、酸性高锰酸钾溶液
(2)上述四种物质互为同系物的是__________。(填字母)
(3)在一定条件下,B能发生聚合反应,写出该反应的方程式__________。
(4)上述四种物质中有一种可以在一定条件下与浓硝酸反应,请写出反应的化学方程式:__________
(5)E是一种新合成的烃,其碳架呈三棱柱体(如图所示);
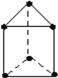
①上述物质中与E互为同分异构体的是__________。(填分子式)
②E的二氯取代物有__________种。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属有机催化体系的发现和发展对有机合成策略的革新起到关键的决定性作用。最近,中国科学家采用新型锰催化体系,选择性实现了简单酮与亚胺的芳环惰性C-H的活化反应。利用该反应制备化合物W的合成路线如下:
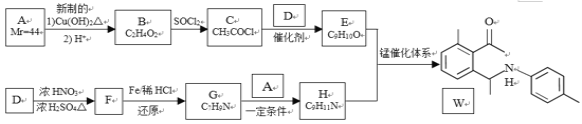
已知:①A为常见的有机物;D为苯的同系物,分子式为C7H8
②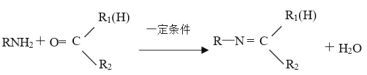
回答下列问题:
(1)B中官能团的名称是__________,F的化学名称是____________。
(2)W的分子式为__________。
(3)D→F,E+H→W的反应类型分别是___________、_____________。
(4)A与银氨溶液加热反应的化学方程式为__________。C和D生成E的化学方程式为_________。
(5)芳香化合物L是E的同分异构体。若L能发生银镜反应,则L可能的结构有______种,其中核磁共振氢谱有四组峰的结构简式为__________(任写一种)。
(6)请以甲苯、丙酮(CH3COCH3)等为原料制备 ![]() ,写出相应的合成路线流程图(无机试剂任用)_________。
,写出相应的合成路线流程图(无机试剂任用)_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“结晶玫瑰”具有强烈的玫瑰香气,属于结晶型固体香料,在香料和日用化工产品中具有广阔的应用价值。“结晶玫瑰”的化学名称为乙酸三氯甲基苯甲酯,通常用三氯甲基苯基甲醇和醋酸酐为原料制备。
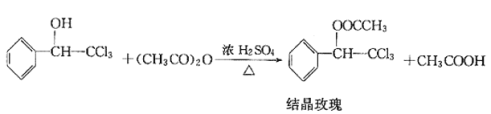
已知:
物质 | 在乙醇中的溶解性 | 在水中的溶解性 | 熔点℃ |
三氯甲基苯基甲醇 | 溶 | 不溶 | — |
醋酸酐 | 溶 | 溶 | -73 |
结晶玫瑰 | 溶 | 不溶 | 88 |
醋酸 | 易溶 | 易溶 | 16.6 |
部分实验装置以及操作步骤如下:
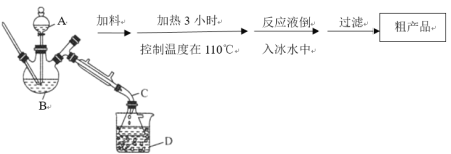
请根据以上信息,回答下列问题:
(1)装置中仪器B的名称是___________。
(2)加料时,应先加入三氯甲基苯基甲醇和醋酸酐,然后慢慢加入浓硫酸并搅拌。待混合均匀后,最适宜的加热方式为油浴加热,用油浴加热的理由是_______________。有同学认为装置中A仪器也可改为另一种漏斗,该漏斗的名称是___________,它的作用是____________。
现有同学设计如下方案把粗产品进行提纯。
(3)①将粗产品溶解在________(填“水”、“乙醇”或“粗产品滤液”)中均匀混合,用水浴加热到70℃,回流溶剂使粗产品充分溶解,得到无色溶液。然后将所得溶液经过__________(填操作方法)析出白色晶体,整个过程中不需要用到的仪器是_______(选择相应字母填空)。
A.冷凝管 B.烧杯 C.蒸发皿 D.玻璃棒
②将步骤①所得混合物过滤、洗涤、干燥得到白色晶体,请列举一种常见的实验室干燥的方法_______。可通过测定晶体的熔点判断所得晶体是否是结晶玫瑰,具体做法为:加热使其熔化测其熔点,实验现象为__________。
(4)ag的三氯甲基苯基甲醇与足量乙酸酐充分反应得到结晶玫瑰bg,则产率是_________。(用含a、b的式子表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯二氧化碳主要用于医学研究及临床诊断及电子工业;含碳的有机物醇、醛在生产生活中有广泛运用。
I.(1)工业上用CO2和H2在一定条件下反应可合成二甲醚,已知:
2CO2(g)+6H2(g)=2CH3OH(g)+2H2O(g) △H1=-107.4kJ/mol
2CH3OH(g)=CH3OCH3(g)+H2O(g) △H2=-23.4kJ/mol
则2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3=________kJ/mol
CH3OCH3(g)+3H2O(g) △H3=________kJ/mol
(2)在一定条件下将CO2和H2充入一固定容积的密闭容器中,在两种不同温度下发生反应:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g),测得CH3OCH3(g)的物质的量随时间的变化如图所示。
CH3OCH3(g)+3H2O(g),测得CH3OCH3(g)的物质的量随时间的变化如图所示。
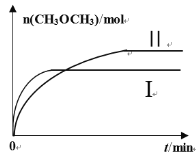
①曲线I、Ⅱ对应的平衡常数大小关系为KI_______KⅡ(填“>”“=”或“<”)。
②一定温度下,下列能判断该反应达到化学平衡状态的是________(填序号)。
a.混合气体密度不变
b.二甲醚和水蒸气的反应速率之比保持不变
c.v正(H2)=2v逆(H2O)
d.2个C=O断裂的同时有3个H-O断裂
(3)合成气CO和H2在一定条件下能发生如下反应:CO(g)+2H2(g)![]() CH3OH(g) △H。在某压强下,合成甲醇的反应在不同温度、不同投料比时,CO的转化率如图所示。
CH3OH(g) △H。在某压强下,合成甲醇的反应在不同温度、不同投料比时,CO的转化率如图所示。
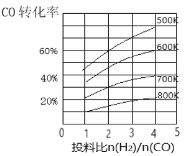
①600K温度下,将1molCO和4molH2充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(H2)=___________。
②若投料比保持不变,升高温度,该反应平衡向_______方向移动(填“正反应”或“逆反应”)。
③上述合成甲醇的过程中提高CO的转化率可采取的措施有______。(列举一种即可)。
Ⅱ.用隔膜电解法处理高浓度乙醛废水的原理为:
使用惰性电极电解,乙醛分别在阴、阳极转化为乙醇和乙酸,总反应为:2CH3CHO+H2O![]() CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程。
CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程。
①电解过程中,两极除分别生成乙酸和乙醇外,均产生无色气体,阳极产生气体的电极反应为:______。
②在实际工艺处理过程中,阴极区乙醛的去除率可达80%。若在两极区分别注入1m3乙醛含量为400mg/L的废水,可得到乙醇________kg(计算结果保留2位小数)。
查看答案和解析>>
科目: 来源: 题型:
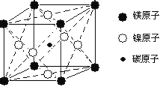
【题目】最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。
(1)该新型超导晶体的一个晶胞如图所示,则该晶体的化学式是__________。镍在元素周期表中的位置是______,Ni2+的价电子有_________种不同运动状态。
(2)500-600℃时,BeCl2以双聚分子存在的BeCl2的结构式为________________________。
(3)橙红色晶体羰基钴的熔点为52℃,分子式为Co2(CO)8,是一种重要的无机金属配合物,可溶于多数有机溶剂。该晶体属于______晶体,配体是______该配合物中存在的作用力类型有___________(填标号)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键 F.范德华力
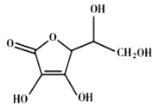
(4)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为_______;推测抗坏血酸在水中的溶解性:________(填“难溶于水”或“易溶于水”)。
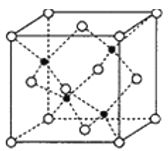
(5)副族元素Zn和元素Se形成的某化合物属于立方晶系,其晶胞结构如图所示,其中为( ![]() 为Se,
为Se,![]() 为Zn),Zn的配位数为______,该晶体的密度为
为Zn),Zn的配位数为______,该晶体的密度为![]() g/cm3,则Zn—Se键的键长为______nm。
g/cm3,则Zn—Se键的键长为______nm。
查看答案和解析>>
科目: 来源: 题型:
【题目】一同学设计了两种由CuO→Cu的实验方案:
方案一:Zn![]() H2
H2![]() Cu;
Cu;
方案二:CuO![]() CuSO4
CuSO4![]() Cu。
Cu。
大家认为方案二优于方案一,理由是:①节约能源;②Cu产率高;③产品纯净;④操作安全。其中,评价正确的是( )
A.①②③B.①②④C.①③④D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com