
【题目】一同学设计了两种由CuO→Cu的实验方案:
方案一:Zn![]() H2
H2![]() Cu;
Cu;
方案二:CuO![]() CuSO4
CuSO4![]() Cu。
Cu。
大家认为方案二优于方案一,理由是:①节约能源;②Cu产率高;③产品纯净;④操作安全。其中,评价正确的是( )
A.①②③B.①②④C.①③④D.②③
【答案】B
【解析】
方案一:Zn+H2SO4═ZnSO4+H2↑,H2+CuO =Cu+H2O,反应需加热,且H2还原CuO时需先通H2排出空气,否则易爆炸,反应结束后还需通入H2至生成的Cu冷却,否则Cu又易被氧化;
方案二:CuO +H2SO4= CuSO4+H2O,Zn+ CuSO4=ZnSO4+Cu;耗原料少,操作安全,产率高,但Cu中易混有Zn,以此来解答。
方案一中发生Zn+H2SO4═ZnSO4+H2↑、H2+CuO =Cu+H2O,反应需加热,且H2还原CuO时需先通H2排出空气,否则易爆炸,反应结束后还需通入H2至生成的Cu冷却,否则Cu又易被氧化,而方案二消耗原料少,操作安全,产率高,则方案二优于方案一,理由是:①节约能源、②Cu产率高、④操作安全;
故选:B。


科目:高中化学 来源: 题型:
【题目】根据相应的图像,判断下列相关说法错误的是
A.图①中,密闭容器中反应达到平衡,t0时改变某一条件,则改变的条件可能是加压(a+b=c)或使用催化剂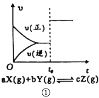
B.图②是达到平衡时外界条件对平衡的影响关系,则正反应为放热反应,p2>p1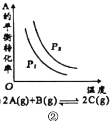
C.图③是物质的百分含量和温度T关系,则反应为放热反应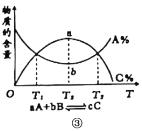
D.图④是反应速率和反应条件变化关系,则该反应的正反应为吸热反应,且A、B、C、D一定均为气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电解NaHSO4溶液制备Na2S2O8(过二硫酸钠)。电解时,阴极材料为Pb;阳极(铂电极)电极反应式为2![]() -2e-=
-2e-=![]() +2H+。下列说法正确的是
+2H+。下列说法正确的是
A.Na2S2O8水溶液呈弱碱性
B.Na2S2O8可水解生成H2O2,同时生成NaHSO4可循环利用
C.H2S2O8可完全电离,故稳定性与硫酸相当
D.Na2S2O8具有强氧化性,故不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H)。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
①比较下列两组物质的熔点高低(填“>”或“<”=)
SiC_____________Si;SiCl4_____________SiO2
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)该反应的反应热△H=_____________kJ/mol.
Si(s)+4HCl(g)该反应的反应热△H=_____________kJ/mol.
(2)已知化合物Na2O的晶胞如图。
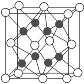
①其中O2-离子的配位数为________,
②该化合物与MgO相比,熔点较高的是________。(填化学式)
③已知该化合物的晶胞边长为apm,则该化合物的密度为___g·cm-3(只要求列出算式,不必计算出数值,阿伏加德罗常数的数值为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.向氨水中加入少量的硫酸氢钠,溶液碱性减弱
B.每升pH=3的H2C2O4 溶液中H+数目为0.003NA
C.常温下,CH3COONa溶液中加水,水电离产生的c(H+)、c(OH-)保持不变
D.0.1molFeCl3溶于水形成的Fe(OH)3胶体粒子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属有机催化体系的发现和发展对有机合成策略的革新起到关键的决定性作用。最近,中国科学家采用新型锰催化体系,选择性实现了简单酮与亚胺的芳环惰性C-H的活化反应。利用该反应制备化合物W的合成路线如下:
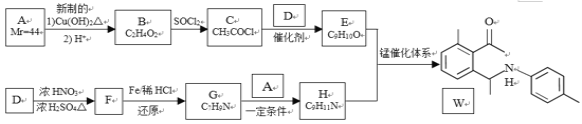
已知:①A为常见的有机物;D为苯的同系物,分子式为C7H8
②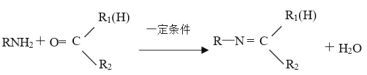
回答下列问题:
(1)B中官能团的名称是__________,F的化学名称是____________。
(2)W的分子式为__________。
(3)D→F,E+H→W的反应类型分别是___________、_____________。
(4)A与银氨溶液加热反应的化学方程式为__________。C和D生成E的化学方程式为_________。
(5)芳香化合物L是E的同分异构体。若L能发生银镜反应,则L可能的结构有______种,其中核磁共振氢谱有四组峰的结构简式为__________(任写一种)。
(6)请以甲苯、丙酮(CH3COCH3)等为原料制备 ![]() ,写出相应的合成路线流程图(无机试剂任用)_________。
,写出相应的合成路线流程图(无机试剂任用)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D1、D2、E、F、G、H均为有机化合物,请根据下列图示回答问题。
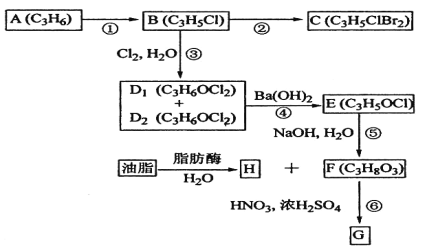
(1)直链有机化合物A的结构简式是__________________;
(2)B中官能团的名称为___________;
(3)①的反应试剂和反应条件是__________;
(4)D1或D2生成E的化学方程式是___________________________________;
(5)G可应用于医疗、爆破等,由F生成G的化学方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:
a. 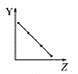 b.
b. 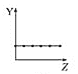 c.
c. 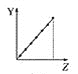 d.
d. 
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为___________(名称),Y为____________(元素符号),Z原子结构示意图为________________。
②N的最高价氧化物的水化物的化学式为________________。
③M的最高价氧化物的化学式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题。每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》
⑴材料是人类赖以生存和发展的重要物质基础。
①水泥是最常用的建筑材料,它属于______________(填字母)。
a.金属材料b.无机非金属材料c.有机高分子材料
②下列硅酸盐产品的生产原料中不需要石灰石的是_______________(填字母)。
a.陶瓷b.水泥c.玻璃
③高岭土是烧制瓷器的重要原料,其组成可以表示为Al2Si2Ox(OH)y,其中x,y的数值分别是_______________(填字母)。
a.5、4b.6、3c.7、2
④下列物品的构成材料中主要是合成高分子材料的是_______________(填字母)。
a.宣纸b.羊毛衫c.保鲜膜
⑤橡胶是制造轮胎的主要原料,天然橡胶是________________结构(填“线型”或“体型”),需经过硫化处理改变其结构,增强其机械强度。
⑵良好的生态环境可以提升生活质量。
①汽车尾气(含有烃类、CO、NOx、SO2等)是城市空气的主要污染源,治理方法之一是在汽车排气管上加装“催化转化器”使CO、NOx转化为无害物质,下列说法不正确的是________________。
a.CO和NOx反应的化学方程式为:2xCO + 2NOx=2xCO2 + N2
b.上述方法增加了空气中CO2的含量,加重了酸雨污染
c.在日光照射下,汽车尾气还会产生光化学烟雾
②家庭装修中使用的装潢材料缓慢释放出来的污染物达一定浓度时会影响人体健康,下列属于常见装修污染物的是_______________(填字母)。
a.NO、NO2b.甲醛、苯c.SO2、CO
③通过水质检测确定水体中污染物的种类和浓度后,可采取不同的方法对污水进行处理。例如向废水中通入臭氧,运用_______________(填字母)除去其中含有的油类、氰化物。
a.中和法b.沉淀法c.氧化法
④天然水中含有细小悬浮颗粒物可以用明矾进行处理,明矾溶于水后电离出的铝离子与水反应生成氢氧化铝胶体能吸附悬浮颗粒物,写出铝离子与水反应的离子方程式___________________________。
⑶均衡营养、合理用药是保证人体健康的重要途径。
①葡萄糖可作为营养剂供给人体能量,其在人体内发生的主要反应是_______________(填字母)。
a.加成反应
②维生素C能防治坏血病,可通过食用富含它的食物进行补充,碱性条件下维生素C易被空气氧化,为减少维生素C的损失,烹调食物时可加入少许 _______________(填字母)。
a.白糖b.食醋c.苏打
③人体内有8种氨基酸必须通过食物摄入,某品牌蛋糕中含有下列物质,其中水解生成氨基酸的是 _______________(填字母)。
a.纤维素b.蛋白质c.油脂
④“胃舒平”又名复方氢氧化铝,除主要成分氢氧化铝外,还含有一定量的三硅酸镁(2MgO·3SiO2·nH2O),三硅酸镁与胃酸发生反应生成MgCl2和H2SiO3,其反应方程式是______________。
B.《有机化学基础》
⑴根据分子中所含官能团可预测有机化合物的性质。
①分子中所有碳原子位于同一条直线上的是________________(填字母)。
a.丙烷b.丙烯c.丙炔
②能发生加成反应的有机物是______________(填字母)。
a.CH3CH2Brb.CH3CH2OHc.葡萄糖
③能鉴别乙烯与乙烷的试剂是______________(填字母)。
a.水b.酸性KMnO4溶液c.NaOH溶液
④下列化合物中,能发生酯化反应的是_______________。(填字母)
a.CH3CHOb.HCOOCH3c.CH3COOH
⑤与![]() 和
和![]() 都能反应的是______________。(填字母)
都能反应的是______________。(填字母)
a.FeCl3溶液b.金属钠c.饱和Na2CO3溶液
⑵非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
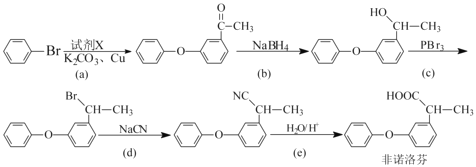
①反应中加入的试剂X的分子式为C8H8O2,X的结构简式为 ________________。
②上述反应中是取代反应的有 ________________(填字母),是还原反应的有 _______________(填字母)。
③非诺洛芬的一种同分异构体满足下列条件,写出该异构体的结构简式: ________________。
Ⅰ不能与FeCl3发生显色反应,但其一种水解产物能与FeCl3发生显色反应。
Ⅱ分子中有3种不同化学环境的氢,且分子中含有两个苯环。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com