
科目: 来源: 题型:
【题目】现有73 g HCl气体,若阿伏加德罗常数用NA表示,则:
(1)HCl气体的物质的量为_______mol。
(2)HCl气体所含原子总数为_______个。
(3)HCl气体在标准状况下的体积为________L。
(4)HCl气体溶于水后形成2 L溶液,其溶液的物质的量浓度为_________mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为3∶1)直接作燃料,其工作原理如图所示,并以此电源用于工业生产。
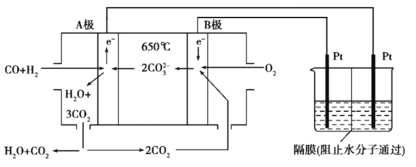
(1)H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0kJ·mol-1,1g液态水变为水蒸气时吸热2.44kJ,则电池总反应3CO(g)+H2(g)+2O2(g)=3CO2(g)+H2O(g)的ΔH=___________kJ·mol-1,B电极上发生反应的电极反应式为___________。
(2)若以此电源生产新型硝化剂N2O5,装置如上图所示。已知两室加入的试剂分别是a.硝酸溶液b.N2O4+无水硝酸,则左室加入的试剂应为___________(填“a”或“b”),其电极反应式为___________。
(3)若以此电源用惰性电极电解足量的硝酸银溶液,阴极产物的质量为5.4g,则阳极产生的气体在标准状况下的体积为___________L。电解后溶液体积为500mL,溶液的pH约为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】温度T℃时,在3个体积相同的恒容密闭容器中发生反应CO(g)+H2O(g)![]() CO2(g)+H2(g)ΔH=-41kJ·mol-1,其起始时投料、各物质的量及其达平衡过程体系热量的变化如表所示:
CO2(g)+H2(g)ΔH=-41kJ·mol-1,其起始时投料、各物质的量及其达平衡过程体系热量的变化如表所示:
容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系热量的变化(均为正值) | |||
CO | H2O(g) | CO2 | H2 | ||
① | 1 | 4 | 0 | 0 | 32.8kJ |
② | 8 | 2 | 0 | 0 | Q1 |
③ | 0 | 0 | 1 | 4 | Q2 |
下列说法中不正确的是
A.容器②中热量变化:Q1=65.6kJ
B.平衡后容器①②中各组分体积分数相同
C.三个容器达平衡时,①中的CO、②中的H2O(g)、③中的CO2的转化率相等
D.保持相同条件,向平衡后的容器①中再加入0.1molCO和0.4molCO2(g),平衡不移动
查看答案和解析>>
科目: 来源: 题型:
【题目】磷酸铁锂电池是新型的绿色能源电池,其简化的生产工艺流程如下。
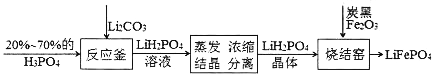
(1)反应釜中反应的化学方程式为_______,该反应体现出非金属性关系:P_____C(填“>”或“<”)。
(2)室温下,LiH2PO4溶液的pH随c(H2PO4-)的变化如图1所示,H3PO4溶液中H2PO4-的分布分数![]() 随pH的变化如图2所示[
随pH的变化如图2所示[![]() (含P元素的粒子)]。
(含P元素的粒子)]。
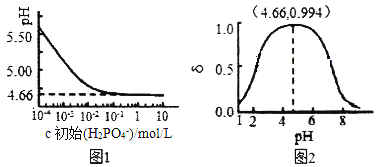
①由图1知,低浓度时LiH2PO4溶液的pH小于7,且随着c初始(H2PO4-)的增大而减小,其合理的解释为__________________。
②综合上图分析,若用浓度大于1mol/L的H3PO4溶液溶解Li2CO3,要使反应釜中的H3PO4几乎全部转化成LiH2PO4,反应釜中需要控制溶液的pH=________。
(3)磷酸铁锂电池总反应为:LiFePO4+6C![]() Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向______(填“阳极”或“阴极”);放电时,正极反应式为__________________。
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向______(填“阳极”或“阴极”);放电时,正极反应式为__________________。
(4)磷酸铁锂电池中铁的含量可通过如下方法测定:称取1.60g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.030mol/L重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液50.00mL。
已知:2Fe3++Sn2++6Cl-=SnCl62-+2Fe2+
4Cl-+Sn2++2HgCl2=SnCl62-+Hg2Cl2
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
①实验中加入HgCl2饱和溶液的目的是____________。
②铁的百分含量Fe(%)=_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中物质的量浓度为1mol/L的是( )
A.将40g NaOH溶解在1L水中
B.将22.4L HCl气体溶于水配成1L溶液
C.将1L 10 mol/L浓盐酸加入9L水中
D.将10g NaOH溶于少量水,在稀释到溶液为250ml
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是某温度下,将足量的BaSO4固体溶于一定量水中达到溶解平衡后,假定溶液体积不变的情况下,加入Na2CO3使c(CO32-)增大过程中,溶液中c(Ba2+)和c(SO42-)的变化曲线。根据图中的数据分析,下列说法正确的是:
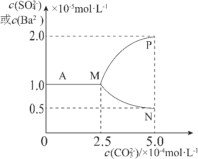
A.该温度下BaSO4的Ksp=2.5×10-9mol2·L-2
B.图中表示c(Ba2+)的曲线是MP
C.反应BaSO4(s)+CO32-(aq)![]() BaCO3(s)+SO42-(aq)的平衡常数K=0.04
BaCO3(s)+SO42-(aq)的平衡常数K=0.04
D.如用1LNa2CO3溶液将0.1molBaSO4固体完全转化为BaCO3,则原Na2CO3溶液浓度至少为2.5mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】在标况下,m克气体A和n克气体B的分子数相等,下列说法正确的是
A.同体积的气体A和气体B的质量比为m:n
B.25℃时,1kg气体A和1kg气体B的分子数比为m:n
C.同温同压下,气体A和气体B的密度比为n:m
D.标准状况下,等质量的气体A和气体B的体积比为n:m
查看答案和解析>>
科目: 来源: 题型:
【题目】某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离:H2A![]() H++HA-、HA-
H++HA-、HA-![]() H++A2-。已知相同浓度时的电离度α(H2A)>>α(HA-),现有下列四种溶液:
H++A2-。已知相同浓度时的电离度α(H2A)>>α(HA-),现有下列四种溶液:
①0.01mol·L-1的H2A溶液
②0.01mol·L-1的NaHA溶液
③0.02mol·L-1的HCl与0.04mol·L-1的NaHA溶液等体积混合液
④0.02mol·L-1的NaOH与0.02mol·L-1的NaHA溶液等体积混合液
下列说法中不正确的是
A.溶液④一定显碱性B.c(H2A)最大的是③
C.c(A2-)最小的是①D.c(H+)最大的是③
查看答案和解析>>
科目: 来源: 题型:
【题目】生态工业园区的建设,不仅仅是体现环保理念,重要依据循环经济理论和充分考虑经济的可持续发展,如图是某企业设计的硫酸-磷铵-水泥联产,海水-淡水多用,盐-热-电联产生三大生态产业链流程图。根据上述产业流程回答下列问题:
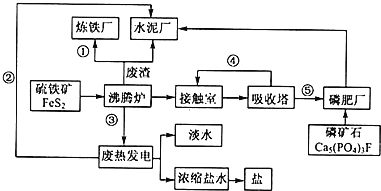
(1)从原料、能源、交通角度考虑该企业应建在______
A西部山区 B沿海地区 C发达城市 D东北内陆
(2)该流程①、②、③、④、⑤为能量或物质的输送,请分别写出输送的主要物质的化学式或能量形式:①______、②______、③______、④______、⑤______。
(3)沸腾炉发生反应的化学方程式:______;磷肥厂的主要产品是普钙,其主要成分是______(填化学式)。
(4)热电厂的冷却水是______,该流程中浓缩盐水除提取盐以外还可提取的物质有______(写出一种即可)。
(5)根据现代化工厂没计理念请提出高炉炼铁厂废气、废渣及多余热能的利用设想。______,______(写出两点即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中:
a. 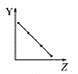 b.
b. 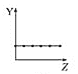 c.
c. 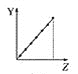 d.
d. 
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为___________(名称),Y为____________(元素符号),Z原子结构示意图为________________。
②N的最高价氧化物的水化物的化学式为________________。
③M的最高价氧化物的化学式为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com