
科目: 来源: 题型:
【题目】如图为某化学反应的速率与时间的关系示意图。有关t1时刻改变条件的说法正确的是
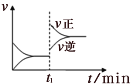
A.C(s)+H2O(g)![]() CO(g)+H2(g) ΔH>0,t1时刻升高温度
CO(g)+H2(g) ΔH>0,t1时刻升高温度
B.H2O(g)+CO(g) ![]() H2(g)+CO2(g) ΔH>0,t1时刻增大压强
H2(g)+CO2(g) ΔH>0,t1时刻增大压强
C.2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0,t1时刻升高温度
2SO3(g) ΔH<0,t1时刻升高温度
D.4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2 浓度
4NO(g)+6H2O(g) ΔH<0,t1时刻增大O2 浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】如图中,两电极上发生的电极反应为a极:Cu2++2e-=Cu;b极:Fe-2e-=Fe2+。下列说法不正确的是
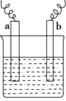
A.电解质溶液含有Cu2+
B.该装置是化学能转化为电能
C.a、b可能是同种电极材料
D.a极上发生还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】已知可分别通过如下两个反应制取氢气: ( )
a.CH3CH2OH(g)+H2O(g) ![]() 4H2(g)+2CO(g) ΔH=+256.6 kJ·mol-1
4H2(g)+2CO(g) ΔH=+256.6 kJ·mol-1
b.2CH3CH2OH(g)+O2(g) ![]() 6H2(g)+4CO(g) ΔH=+27.6 kJ·mol-1
6H2(g)+4CO(g) ΔH=+27.6 kJ·mol-1
则下列说法正确的是( )
A.乙醇的燃烧热ΔH=-13.8 kJ·mol-1
B.升高反应a的反应温度,乙醇的转化率减小
C.2H2(g)+O2(g)=2H2O(g) ΔH=-229 kJ·mol-1
D.制取等量的氢气,反应b吸收的能量更少
查看答案和解析>>
科目: 来源: 题型:
【题目】R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应,X2++Z=X+Z2+,Y+Z2+=Y2++Z。这四种离子被还原成0价时,表现的氧化性强弱顺序为( )
A.R2+>X2+>Z2+>Y2+B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+D.Z2+>X2+>R2+>Y2+
查看答案和解析>>
科目: 来源: 题型:
【题目】曲酸和脱氧曲酸是一种非常有潜力的食品添加剂,结构如图所示。下列有关叙述不正确的是
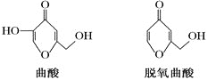
A.曲酸分子中所有原子不可能共平面
B.脱氧曲酸能发生酯化反应、氧化反应、还原反应
C.曲酸与脱氧曲酸所含的官能团相同
D.与脱氧曲酸互为同分异构体的芳香族化合物有4种![]() 不考虑
不考虑![]() 键
键![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四种有机化合物的结构简式如下所示,均含有多个官能团,下列有关说法中正确的是( )
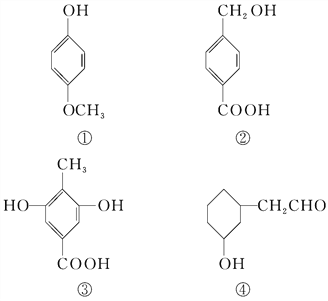
A.①属于酚类,可与NaHCO3溶液反应产生CO2
B.②属于酚类,能使FeCl3溶液显紫色
C.1 mol ③最多能与3 mol Br2发生反应
D.④属于醇类,可以发生消去反应
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铜(CuCl)常用于催化剂、颜料、防腐等工业。某兴趣小组设计实验制备氯化亚铜。回答下列问题:

制法一:将铜粉加入B反应器中,与一定浓度的食盐—盐酸溶液相互作用,在60~70℃通入氧气,充分反应(部分仪器略去)。
①仪器X的名称___,X中盛有二氧化锰,分液漏斗中盛放双氧水,则A装置中发生反应的化学方程式是___。

②反应结束后,打开瓶塞 a,倾出反应液于大烧杯中,为防止外溅,通常采用的操作方法是___。
制法二:将氯化铜与氯化钠加水溶解,并调节酸度,加入铜粉一起加热,Cu2+被单质铜还原,生成可溶性的配合物Na[CuCl2],再经水解后产生白色沉淀。抽滤,沉淀依次用水、无水乙醇洗涤多次,得白色固体产品
①写出该法生成Na[CuCl2]的化学反应方程式___。
②用水洗涤CuCl沉淀的具体操作为___,沉淀水洗后再用无水乙醇洗涤的原因是___。
③判断CuCl是共价化合物还是离子化合物的实验方法是___。
制法三:以铜为电极,电解饱和食盐水也可制得CuCl。阳极的电极反应式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】(题文)有机物M的合成路线如下图:
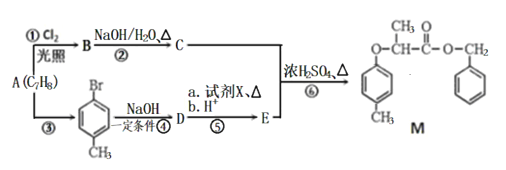
已知:i: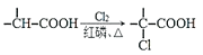 ii:
ii: 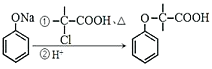
(1)M中含氧官能团的名称有醚键和___________,C的名称为___________,步骤⑥的反应类型为___________。
(2)步骤④反应的化学方程式为_________________________________。
(3)试剂X的结构简式为___________。
(4)同时满足下列条件,E的同分异构体有__________种。
I.能与FeCl3溶液发生显色反应;II.能发生水解反应和银镜反应;III.苯环上只有两个取代基。
其中核磁共振氢谱峰面积比为1:1:2:2:6的分子的结构简式为: ______________________。
(5)根据以上信息,写出以![]() 为原料制取
为原料制取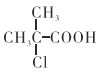 的合成路线图 (无机试剂一定要选银氨溶液,其它无机试剂任选)____________________________________________。合成路线图示例:CH2=CH2
的合成路线图 (无机试剂一定要选银氨溶液,其它无机试剂任选)____________________________________________。合成路线图示例:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组,拟探究和比较SO2和C12的漂白性, 设计如下图所示的实验装置二套。请你参与探究并回答下列问题。
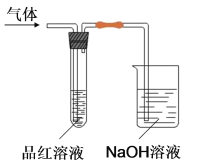
(1)向第一套装置中通入一段时间的SO2,观察到试管中的品红溶液褪色,然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(2)向第二套装置中通入一段时间的C12,观察到试管中的品红溶液也褪色,然后再加热试管,溶液________(填“恢复”或“不恢复”)红色;
(3)由以上两个实验可以说明SO2和C12的漂白原理____(填“相同”或“不相同”);
(4) C12通入品红溶液中,生成的具有漂白性的物质是_____(填“HC1”或“HClO”)。
(5)烧杯中NaOH溶液的作用是______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列框图涉及的物质所含元素中,除一种元素外,其余均为1~18号元素。
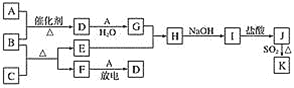
已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为___________。
(2)E与G的稀溶液反应的离子方程式为_________。
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为________ mol·L-1。(已知25 ℃、101 kPa条件下气体摩尔体积为24.5 L·mol-1,不必化简)
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是_________。
(5)B和C反应的化学方程式为__________。
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com