
科目: 来源: 题型:
【题目】(1).FeCl3是中学实验室常用的试剂,可以用来制备氢氧化铁胶体。
下列制备氢氧化铁胶体的操作方法正确的是____________(填字母);
A.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
B.加热煮沸氯化铁饱和溶液
C.在氨水中滴加氯化铁浓溶液
D.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色。
(2)写出Ba(OH)2溶液与少量NaHCO3溶液反应的离子方程式:___________________。
(3)写出次氯酸的电子式:________________;写出过氧化钠中存在的所有化学键类型:____________________。
(4)铁粉中含有铝粉,可加______除去杂质,发生的化学方程式为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备光敏材料KaFeb(C2O4)c·xH2O的工艺流程如下:
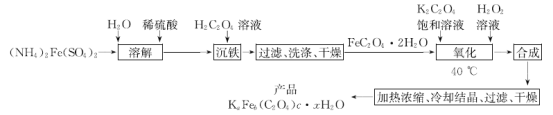
回答下列问题:
(1)“溶解”时,为使所用的水中不含O2,采用的操作方法是_________________。
(2)用H2C2O4(弱酸)“沉铁”时,反应的离子方程式为______________。
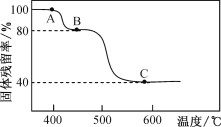
(3)FeC2O4·2H2O热分解与气氛及温度有关,在N2气氛中热分解时,固体的残留率(固体样品的剩余质量/固体样品的起始质量×100%)与温度的关系如图所示,则B→C的变化中,发生反应的化学方程式为___________________。
(4)“氧化”时,温度不宜超过40℃,其原因是_______。
(5)为测定产品KaFeb(C2O4)c·xH2O(铁元素为+3价)的组成,称取产品0.2455g用硫酸溶解后,用0.02000 mol·L-1的KMnO4标准溶液滴定至终点,消耗标准溶液30.00 mL。在上述滴定过C2O42-的保留液中加入足量锌粉,加热至黄色消失,过滤洗涤,滤液及洗涤液再用0.02000 mol·L-1的KMnO4标准溶液滴定至终点,消耗标准溶液5.00 mL。则该产品的化学式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应![]() ,为研究影响该反应速率的因素,在不同条件下进行4组实验,Y、Z的起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。下列说法不正确的是( )
,为研究影响该反应速率的因素,在不同条件下进行4组实验,Y、Z的起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。下列说法不正确的是( )

A.若实验②、④只改变一个条件,则由实验②、④得出结论:升高温度,化学反应速率加快
B.若实验①、②只改变一个条件,则由实验①、②得出结论:增大反应物浓度,化学反应速率加快
C.若实验②、③只改变一个条件,则实验③使用了催化剂
D.0~10min内,实验③的平均速率v(Y)=0.04 mol/(L·min)
查看答案和解析>>
科目: 来源: 题型:
【题目】用废易拉罐制备明矾的实验步骤如下:
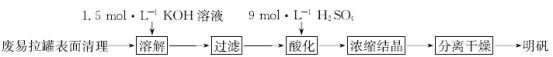
回答下列问题:
(1)清除已剪成片状的废易拉罐表面颜料及塑料内膜的方法是_________________。
(2)实验需用100 mL 1.5 mol·L-1 KOH溶液,配制时需称取KOH固体质量为_________;配制过程中需要的玻璃仪器有烧杯、量筒、玻璃棒及_____________和_____________。
(3)“溶解”时发生反应的化学方程式为________________。
(4)“酸化”时,为使硫酸滴加量不过量太多,正确的操作依据是_________。
(5)鉴定明矾中含有K+的操作方法及现象是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2和CH4催化重整可制备合成气,对减缓燃料危机具有重要意义,其反应历程示意图如图:

下列说法不正确的是( )
A.合成气的主要成分为CO和H2
B.①→②过程可表示为CO2+NiC=2CO+Ni
C.①→②过程吸收能量
D.Ni在该反应中做催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】写出铝丝与硫酸铜溶液的化学方程式,并用双线桥标出电子的转移。化学方程式: _______________;氧化剂:__________ ,还原剂: __________,氧化产物:___________ ,还原产物:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组制备草酸晶体(H2C2O4·2H2O)的实验装置如下:
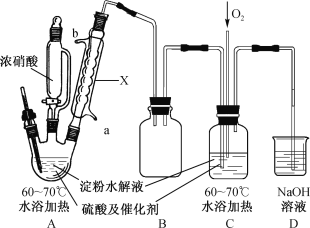
已知:I.草酸(H2C2O4)是二元弱酸,熔点101~102℃;
II.草酸的溶解度如下表所示:
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 |
溶解度/g·(100g水)-1 | 9.5 | 14.3 | 21.2 | 31.4 | 46.0 | 84.5 |
III.在催化剂和硫酸存在下,用浓硝酸氧化淀粉水解液可制备草酸,发生的主要反应为:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O。
回答下列问题:
(1)装置A中仪器X名称为___________,水从接口___________(填“a”或“b”)进入。
(2)装置B的作用是___________;设计装置C的目的是_________________________。
(3)反应C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O中,每生成1 mol H2C2O4转移电子的物质的量为____________。
(4)将装置A和C中反应液浓缩、静置结晶并过滤得粗草酸晶体,提纯H2C2O4·2H2O的方法是_________________________。
(5)探究草酸的性质:
①向Na2CO3溶液中滴加H2C2O4溶液,产生大量气体,说明草酸的酸性比碳酸________(填“强”或“弱”)。
②向NaClO溶液中加入过量H2C2O4溶液,有气泡产生,能解释这一现象的离子方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化铝(AlN)是一种灰白色固体,能与水缓慢反应。利用NH3和Al在800℃以上反应可制备AlN,实验装置如下:

回答下列问题:
(1)装置②中盛放的药品为__________;装置④的作用是吸收氨气和__________。
(2)实验时先点燃①处酒精灯,其目的是______________________________________。
(3)为使实验安全,装置④的尾气处理方法是_____________________。
(4)装置①中发生反应的化学方程式为_____________________;装置③中发生反应的化学方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化学方程式或电离方程式中,不能正确表达反应颜色变化的是
A.将氨气通入滴有酚酞试液的水中,溶液变红:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-
NH4++OH-
B.少量FeCl3溶液滴入沸水中变为红褐色液体:FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
C.向CuCl2溶液中加入足量的铁粉,溶液由蓝色变为浅绿色:Fe+CuCl2=Cu+FeCl2
D.呼吸面具使用后,Na2O2由淡黄色逐渐变为白色:2Na2O2=2Na2O+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】从有机含碘(含I2、ICl等)废水中回收碘并制备KI溶液的一种工艺流程如下:
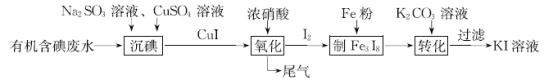
下列说法错误的是
A.“沉碘”时,Na2SO3作还原剂
B.“氧化”时,尾气可用NaOH溶液吸收处理
C.“制Fe3I8”时,每生成1 mol Fe3I8转移8mole-
D.“转化”时,K2CO3溶液可用K2SO4溶液代替
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com