
科目: 来源: 题型:
【题目】将一定量的Fe、Fe2O3、CuO的混合物放入体积为l00mL、浓度为2.2mol·L-1的H2SO4溶液中,充分反应后,生成气体 896mL(标况),得到不溶固体1.28 g,过滤后,滤液中的金属离子只有Fe2+(假设滤液体积仍为 100mL)。向滤液中滴加 2mol·L-1的 NaOH溶液至40mL时开始出现沉淀。则未滴加 NaOH溶液前,滤液中 FeSO4的物质的量浓度为
A.2 mol·L-1B.l.8 mol·L-1C.1.9 mol·L-1D.无法计算
查看答案和解析>>
科目: 来源: 题型:
【题目】一种气态烷烃和气态烯烃组成的混合物共10g,混合气体的密度是相同状况下H2密度的12.5倍,该混合气体通过装有溴水的试剂瓶时,试剂瓶总质量增加8.4g,该混合气体是
A.乙烯和乙烷B.甲烷和乙烯
C.丙烯和甲烷D.丙烯和乙烷
查看答案和解析>>
科目: 来源: 题型:
【题目】向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol·L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示。下列判断正确的是( )
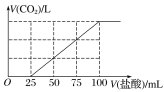
A. 原NaOH溶液的浓度为0.2 mol·L-1
B. 通入CO2在标准状况下的体积为448 mL
C. 所得溶液的溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶3
D. 所得溶液的溶质成分的物质的量之比为n(NaHCO3)∶n(Na2CO3)=1∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】格氏试剂在有机合成方面用途广泛,可用卤代烃和镁在醚类溶剂中反应制得。
设R为烃基,已知RX +Mg![]() R-MgX(格氏试剂)
R-MgX(格氏试剂)
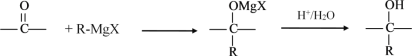
阅读以下合成路线图,回答有关问题:

(1)反应I的类型是____________,反应II的条件是____________。
(2)反应III的化学方程式为____________。
(3)E的同分异构体中,含有苯环且能发生银镜反应的有机物共有____________种。
(4)有机物![]() 是合成药物中的一种原料,实验室可用下列合成路线合成该有机物:
是合成药物中的一种原料,实验室可用下列合成路线合成该有机物:
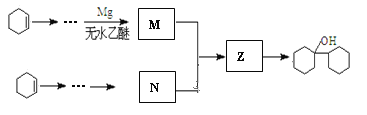
其中Z的结构简式为____________,用反应流程图表示以环己烯(![]() )为有机原料合成有机物N。____________
)为有机原料合成有机物N。____________
查看答案和解析>>
科目: 来源: 题型:
【题目】氢能的存储是氢能应用的主要瓶颈,开发新型储氢材料是氢能利用的重要研究方向。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。
①基态Ti2+中含有的电子数为______,电子占据的最高能级是______,该能级具有的原子轨道数为______。
②BH4-中B原子的杂化方式是______。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+______ H-(填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物,M的部分电离能如下表所示:
I1/kJmol-1 | I2/kJmol-1 | I3/kJmol-1 | I4/kJmol-1 | I5/kJmol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
该氢化物的化学式为______。
(3)液氨是富氢物质,是氢能的理想载体。
①NH3的相对分子质量小于PH3,但NH3的沸点却远高于PH3,其原因是 ______。
②NH3容易和分子中有空轨道的BF3反应形成新的化合物,该化合物的结构式为 ______。
(4)2008年,Yoon等人发现Ca与C60(分子结构如图1)生成的Ca32C60能大量吸附H2分子。
①C60晶体易溶于苯、CS2,C60是 ______ 分子(填“极性”或“非极性”)。
②1mol C60分子中,含有σ 键数目为 ______ 个(阿伏加德罗常数用NA表示)。

(5)某金属氢化物储氢材料的晶胞结构如图2所示,该金属氢化物的化学式为 ______,已知该晶体的密度为agcm-3,金属元素R的相对原子质量为M,阿伏加德罗常数为NA,则该晶胞的体积为 ______ cm3。
查看答案和解析>>
科目: 来源: 题型:
【题目】分子式为C8H8O3的芳香族化合物有多种不同的结构,这些物质在食品、化妆品等行业有广泛用途。
(1)C8H8O3的某一同分异构体尼泊金酯的结构简式如图。
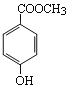
①下列对尼泊金酯的判断不正确的是______。
a.能发生水解反应
b.能与FeCl3溶液发生显色反应
c.分子中所有原子都在同一平面上
d.与浓溴水反应时,1 mol尼泊金酯消耗1 mol Br2
②尼泊金酯与NaOH溶液在一定条件下反应的化学方程式是________________________,其中包含的反应类型有________________、_______________。
(2)C8H8O3的另一种同分异构体甲满足以下条件:
①与足量的NaOH溶液完全反应时,1 mol甲消耗3 molNaOH
②遇FeCl3溶液显色③ 苯环上的一氯取代物只有一种,甲可能的结构简式是_______、________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硼是新型无机材料中的明星元素。

(1)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为 ______,图为磷化硼晶体结构中最小的重复单元,磷化硼的晶体类型是 ______,一个晶胞中含 ______个P原子,每个B或P均形成4个共价键,其中有一个配位键,提供空轨道的是 ______原子。
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是 ______(填元素符号),其基态原子的电子排布式为 ______,氮化硼中B元素的化合价为 ______。
(3)环硼氮烷与苯是等电子体,其一氯代物有两种结构、二氯代物有四种结构,写出环硼氮烷分子结构式 ______。
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料。在BF3分子中,F-B-F的键角是 ______ 度,B原子采用 ______ 杂化;BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为 ______。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍,B在D的单质中充分燃烧能生成其最高价化合物BD2,E+与D2-具有相同的电子数。A在F是单质中燃烧,产物溶于水得到一种强酸。下列有关说法正确的是( )
A.工业上F单质用MnO2和AF来制备
B.B元素所形成的单质的晶体类型都是相同的
C.F所形成的氢化物的酸性强于BD2的水化物的酸性,说明F的非金属性强于B
D.由化学键角度推断,能形成BDF2这种化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】向含0.2molAlCl3的溶液中加入了一定量的1mol/L的NaOH溶液后,生成了7.8g的沉淀,则加入的NaOH溶液的体积可能为( )
A.150mLB.200mLC.700mLD.400mL
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素中:A是地壳中含量最高的元素;B比Ne的质子数多1个;C最外层电子数与其电子层数相等;D单质是半导体材料;E非金属性在同周期元素中最强。下列说法中正确的是
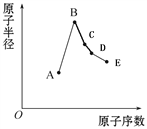
A. B离子的半径比C离子的半径小
B. C单质与A或E单质形成的化合物均为离子化合物
C. A、B两单质反应可得到两种不同的离子化合物
D. B最高价氧化物对应的水化物与0.1mol D单质充分反应放出4.48L气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com