
科目: 来源: 题型:
【题目】氯胺是一种长效缓释水消毒剂,主要包括一氯胺、二氯胺和三氯胺(NH2Cl,NHCl2和NCl3)。工业上可利用NH3(g)+Cl2(g) ![]() NH2Cl(g)+HCl(g)制备一氯胺。回答下列问题:
NH2Cl(g)+HCl(g)制备一氯胺。回答下列问题:
(1)氯胺作饮用水消毒剂是因为水解生成具有强烈杀菌作用的物质,该物质是___,二氯胺与水反应的化学方程式为___。
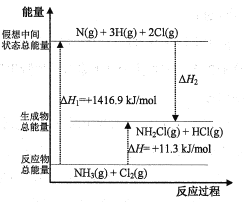
(2)已知部分化学键的键能和化学反应的能量变化如表和如图所示(忽略不同物质中同种化学键键能的细微差别)。
化学键 | N-H | N-Cl | H-Cl |
键能(kJ/mol) | 391.3 | x | 431.8 |
则ΔH2=___kJ/mol,x=___。
(3)在密闭容器中反应NH3(g)+Cl2(g) ![]() NH2Cl(g)+HCl(g)达到平衡,据此反应通过热力学定律计算理论上NH2Cl的体积分数随
NH2Cl(g)+HCl(g)达到平衡,据此反应通过热力学定律计算理论上NH2Cl的体积分数随![]() (氨氯比)的变化曲线如图所示。
(氨氯比)的变化曲线如图所示。
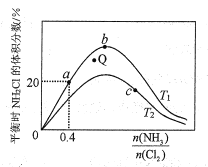
①a、b、c三点对应平衡常数的大小关系是___。T1温度下该反应的平衡常数为___(列出算式即可)。
②在T2温度下,Q点对应的速率:v正___v逆(填“大于”“小于”或“等于”)。
③在氨氯比一定时,提高NH3的转化率的方法是___(任写1种)
④若产物都是气体,实验测得NH2Cl的体积分数始终比理论值低,原因可能是___。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知在常温常压下,A是固体,B、C、D、E是非金属单质且都是气体,C呈黄绿色;化合物F是淡黄色固体,化合物G的焰色反应为黄色,化合物Ⅰ和J通常状况下呈气态;D和E反应生成一种刺激性气味的气体。
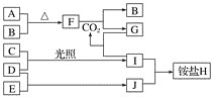
请回答下列问题:
(1)E和J的化学式分别是________和________。
(2)写出F和CO2反应的化学方程式并用单线桥法表示电子转移的情况:_________。
(3)将少量单质C通入盛有淀粉碘化钾溶液的试管中,溶液变蓝色,该反应的离子方程式为_________。
(4)标况下3.36 L气体B与A完全反应,转移电子的数目为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外活动小组的同学在网上查询资料时得知,干燥的CO2与Na2O2不能反应,只有在水蒸气存在下二者才能发生反应。他们设计了如图所示实验装置,用于验证上述结论。
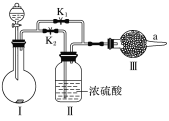
(1)装置Ⅰ中的试剂的最佳组合是________(填字母)。
a.稀盐酸 b.稀硫酸
c.小苏打 d.石灰石
(2)实验时,甲同学认为关闭K1、打开K2,通过观察________判断此时Ⅲ中是否发生了化学反应。
(3)乙同学认为可以分别按“先关闭K1、打开K2,再关闭K2、打开K1”的方式进行操作,并在a处收集所得气体,然后用带火星的木条检验收集到的气体,但他发现两种情况下木条均没有复燃。
①丙同学经过观察分析,建议在Ⅲ后安装一个盛有碱石灰的干燥管,目的是________________
②丁同学认为即使采纳丙同学的建议且最终观察到木条复燃,也不能证明CO2参与了反应,原因是________________________
(4)为进一步达到实验目的,应补充的实验操作是:取最终反应后Ⅲ中所得固体,____________
查看答案和解析>>
科目: 来源: 题型:
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题(Cl2易溶于CCl4)。
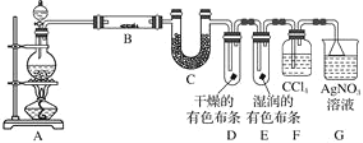
(1)若用含有7.3 g HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2质量总是小于3.55 g的原因是________________________________。
(2)①装置B中盛放的试剂名称为________________,作用是________________________________,现象是_____________________________。
②装置D和E中出现的不同现象说明的问题是___________________。
③装置F的作用是__________________________________________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应放入________(填写试剂或用品名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】设阿伏加德罗常数值用NA表示,下列说法正确的是( )
A.常温下1LpH=3的亚硫酸溶液中,含H+数目为0.3NA
B.A1与NaOH溶液反应产生11.2L气体,转移的电子数为0.5NA
C.NO2与N2O4混合气体的质量共ag,其中含质子数为0.5aNA
D.1mo1KHCO3晶体中,阴阳离子数之和为3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米级TiO2具有独特的光催化性与紫外线屏蔽等功能、具有广阔的工业应用前景。实验室用钛铁精矿(FeTiO3)提炼TiO2的流程如下。下列说法错误的是( )

A.酸浸的化学方程式是:FeTiO3+2H2SO4=FeSO4+TiOSO4+2H2O
B.X稀释所得分散系含纳米级H2TiO3,可用于观察丁达尔效应
C.②用水蒸气是为了促进水解,所得稀硫酸可循环使用
D.①③反应中至少有一个是氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】科研工作者利用Li4Ti5O12纳米材料与LiFePO4作电极组成可充放电电池,其工作原理如图所示。下列说法正确的是( )
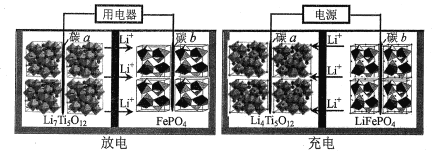
A.放电时,碳a电极为正极,电子从b极流向a极
B.电池总反应为Li7Ti5O12+FePO4=Li4Ti5O12+LiFePO4
C.充电时,a极反应为Li4Ti5O12 +3Li++3e-=Li7Ti5O12
D.充电时,b电极连接电源负极,发生还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物A是近年来采用的锅炉水添加剂,其结构式如图,A能除去锅炉水中溶解的氧气,下列说法正确的是( )
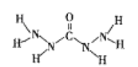
A. A分子中所有原子都在同一平面内
B. A分子中所含的σ键与π键个数之比为10:1
C. 所含C、N均为sp2杂化
D. A与O2反应生成CO2、N2、H2O的物质的量之比为1:2:3
查看答案和解析>>
科目: 来源: 题型:
【题目】通过加入适量乙酸钠,设计成微生物电池可以将废水中的氯苯转化为苯而除去,其原理如图所示。下列叙述正确的是
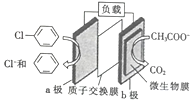
A. b极为正极,发生还原反应
B. 一段时间后b极区电解液的pH减小
C. H+由a极穿过质子交换膜到达b极
D. a极的电极反应式为![]() -e-=Cl-+
-e-=Cl-+![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】氮及其化合物的转化过程如图所示。下列分析合理的是

A. 催化剂a表面发生了极性共价键的断裂和形成
B. N2与H2反应生成NH3的原子利用率为100%
C. 在催化剂b表面形成氮氧键时,不涉及电子转移
D. 催化剂a、b能提高反应的平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com