
科目: 来源: 题型:
【题目】以高纯H2为燃料的质子交换膜燃料电池具有能量效率高、无污染等优点,但燃料中若混有CO将显著缩短电池寿命。
以甲醇为原料制取高纯H2是重要研究方向。甲醇水蒸气重整制氢主要发生以下两个反应:主反应:
CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49kJmol-1
副反应:H2(g)+CO2(g)=CO(g)+H2O(g) △H=+41kJmol-1
①甲醇蒸气在催化剂作用下裂解可得到H2和CO,则该反应的热化学方程式为__,既能加快反应速率又能提高CH3OH平衡转化率的一种措施是__。
②分析适当增大水醇比![]() 对甲醇水蒸气重整制氢的好处是___。
对甲醇水蒸气重整制氢的好处是___。
③某温度下,将![]() =1∶1的原料气充入恒容密闭容器中,初始压强为P1,反应达平衡时总压强为P2,则平衡时甲醇的转化率为___(忽略副反应)。
=1∶1的原料气充入恒容密闭容器中,初始压强为P1,反应达平衡时总压强为P2,则平衡时甲醇的转化率为___(忽略副反应)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组拟合成西他沙星的中间体X。其流程如下:

已知:①![]() +CH3CH2Br
+CH3CH2Br![]()
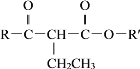
②R-CH2Br+![]()
![]()
![]() +HBr
+HBr
③![]() +H-CH2-COOR″
+H-CH2-COOR″![]() RCOCH2COOR″+R′-OH
RCOCH2COOR″+R′-OH
请回答:
(1)下列说法正确的是___。
A.化合物A不能与H2发生加成反应
B.化合物D→E,发生了取代反应
C.化合物F的水解产物具有两性
D.化合物G分子式为C13H15ON2
(2)化合物C的结构简式___。
(3)写出E→F的化学方程式___。
(4)中间体X有多种同分异构体,写出3种同时满足下列条件的X的同分异构体结构简式___。
①分子中含有一个六元碳环;②含有![]() 结构。
结构。
(5)以乙醇为原料,设计合成A的路线(无机试剂任选,用流程图表示)__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,属于同分异构体的是( )
A.![]() 和
和![]()
B.H2N-CH2-COOH 和 H3C-CH2-NO2
C.CH3-CH2-CH2-COOH 和 H3C-CH2-CH2-CH2-COOH
D.H3C-CH2-O-CH2-CH3 和![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】甲酸钠是一种重要的化工原料。在0.5L真空密闭耐压容器中,将预先用95%乙醇水溶液配制的0.2LNaOH溶液加到容器,加热并搅拌,达到60℃恒温时,通入CO到一定压力,开始反应后记录容器压力随时间变化,直到压力不再变化,冷却,泄压,取出反应物,抽滤、烘干并称量。其反应如下:
Ⅰ:CO(g)+H2O(g)![]() HCOOH(aq) ΔH1 K1
HCOOH(aq) ΔH1 K1
Ⅱ:HCOOH(aq)+NaOH(aq)![]() HCOONa(s)+H2O(l) ΔH2 K2
HCOONa(s)+H2O(l) ΔH2 K2
Ⅲ:CO(g)+NaOH(aq)![]() HCOONa(s) ΔH K
HCOONa(s) ΔH K
请回答:
(1)K=___(用K1、K2表示),ΔH=___(用ΔH1、ΔH2表示)。
(2)若需加快反应Ⅲ的速率,下列措施可行的是___。
A.增大CO的初始压力 B.适当升高温度
C.减少乙醇浓度 D.降低搅拌转速
(3)CO的压力转化率可以反映羰基化进程。CO的压力转化率可以表示为:x(CO)=1-![]() ×100%,P0为CO初始压力,P1为CO某时刻分压。HCOONa收率可表示为:Y(HCOONa)=
×100%,P0为CO初始压力,P1为CO某时刻分压。HCOONa收率可表示为:Y(HCOONa)=![]() ×100%,n0(NaOH)表示投料NaOH的物质的量,n(HCOONa)表示生成HCOONa的物质的量。投料比r=
×100%,n0(NaOH)表示投料NaOH的物质的量,n(HCOONa)表示生成HCOONa的物质的量。投料比r=![]() 。
。
保持60℃恒温,以投料比r=0.7时,CO初始压力分别为0.5Mpa、1.5Mpa和2.0Mpa,测得x(CO)与t的关系如图所示。
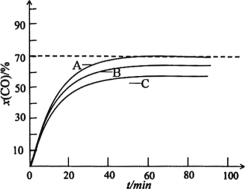
①表示1.5Mpa的曲线为___(用A、B、C表示)。
②若1.5Mpa时,Y(HCOONa)=87%,则NaOH的转化率为___。
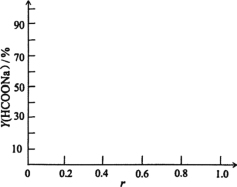
③当CO初始压力为1.5Mpa,保持60℃恒温,不计HCOONa在乙醇中溶解。画出Y(HCOONa)与r示意图___。
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体样品可能含有Fe3+、NH4+、Ag+、NO3-、Cl中的若干种离子,为确定该样品的组成,将样品用蒸馏水配成100mL分散系A,进行了如下实验(假设气体全部逸出):
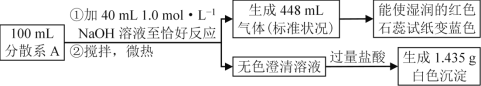
下列说法正确的是( )
A.该样品中肯定含有NH4NO3、AgNO3
B.溶液A中肯定没有Fe3+、Cl
C.溶液A可能含有Cl
D.溶液A中NO物质的量浓度是0.5mol·L1
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,已知有机物A的相对分子质量是28,它的产量是衡量一个国家石油化工水平的标志,B和D都是日常生活食品中常见的有机物,E是具有浓郁香味、不易溶于水的油状液体,F是一种高聚物,生活中用于制造食物保鲜膜。
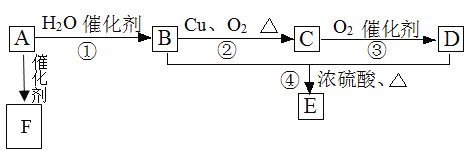
(1)请写出A的结构简式___、C的结构式___;
(2)请写出:B中官能团的电子式___、D中官能团的名称___;
(3)请写出下列反应的类型:①___,②___,④___。
(4)请写出下列物质转化的化学方程式:
A→F:___;
B→C:___;
B+D→E:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:2H2(g)+O2(g)═2H2O(g)△H1
3H2(g)+Fe2O3(s)═2Fe(s)+3H2O(g)△H2
2Fe(s)+![]() O2(g)═Fe2O3(s)△H3
O2(g)═Fe2O3(s)△H3
2Al(s)+![]() O2(g)═Al2O3(s)△H4
O2(g)═Al2O3(s)△H4
2Al(s)+Fe2O3(s)═Al2O3(s)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
A.△H1<0,△H3>0B.△H5<0,△H4<△H3
C.△H1=△H2+△H3D.△H3=△H4+△H5
查看答案和解析>>
科目: 来源: 题型:
【题目】某烷烃的结构简式是CH3CH2CH(CH2CH3)CH3,它的正确命名是
A. 2-乙基丁烷 B. 3-乙基丁烷
C. 3-甲基戊烷 D. 2,2-二甲基丁烷
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,将1 mol A(g)和1 mol B(g)充入2 L密闭容器中发生反应A(g)+B(g)xC(g)+D(s),在t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中C(g)的浓度随时间变化如图所示。下列有关说法正确的是

A. 反应方程式中x=2
B. t2时刻改变的条件是使用催化剂
C. t3时刻改变的条件是移去少量D
D. t1~t3间该反应的平衡常数不相同
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂用NaCl为原料制备高氯酸,实验按流程如下所示:
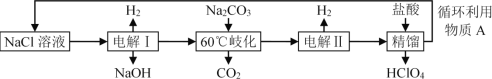
下列说法不正确的是( )
A.电解Ⅰ分别用不锈钢网和石墨作电极,石墨电极上有黄绿色气体生成
B.“60℃歧化”的反应为:3Cl2+3CO32-=5Cl+ClO3-+3CO2
C.电解Ⅱ中阳极反应式为:ClO3-+2OH-2e=ClO4-+H2O
D.循环利用物质A的成分是NaCl、NaClO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com