
科目: 来源: 题型:
【题目】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为:CH4(g)+ CO2(g)=2CO(g)+2H2(g) △H=+247kJ/mol;
①有利于提高CH4平衡转化率的条件是____
A. 高温低压 B.低温高压 C.高温高压 D.低温低压
②某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_______mol2·L2。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
积碳反应CH4(g)= C(s)+2H2(g) | 消碳反应CO2(g)+ C(s)= 2CO(g) | ||
ΔH/(kJ·mol1) | 75 | 172 | |
活化能/(kJ·mol1) | 催化剂X | 33 | 91 |
催化剂Y | 43 | 72 | |
①由上表判断,催化剂X____Y(填“优于”或“劣于”),理由是_________________。在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是________
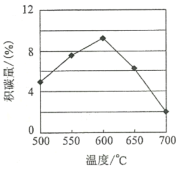
A.K积、K消均增加
B.v积减小,v消增加
C.K积减小,K消增加
D.v消增加的倍数比v积增加的倍数‘
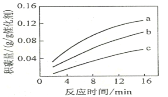
②在一定温度下,测得某催化剂上沉积碳的生成速率方v=k·p(CH4)·![]() (k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为________________。
(k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.常温下,加水稀释氨水,稀释过程中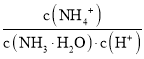 的值不变
的值不变
B.反应NH3(g)+HCl(g)=NH4Cl(s) △H<0在任何条件下均能自发进行
C.常温下电解CuSO4溶液,产生22.4LO2,反应中转移的电子数为4×6.02×1023个
D.为防止浸泡在海水中的闸门腐蚀,可以在闸门上焊接铜块
查看答案和解析>>
科目: 来源: 题型:
【题目】我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:

相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_______________________。
(2)滤渣1的主要成分除SiO2外还有___________;氧化除杂工序中ZnO的作用是____________,若不通入氧气,其后果是________________。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_________________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________;沉积锌后的电解液可返回_______工序继续使用。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为元素周期表的一部分,已知D为金属元素且其原子核外内层电子数为最外层电子数的5倍
A | B | C | ||||
D | E | X | ||||
G | ||||||
Y |
请回答下列问题:
(1)元素B在元素周期表中的位置为________
(2)元素A和元素E的最简单氢化物中沸点较高的是_____(填化学式)
(3)已知BC2中所有原子的最外层均满足8电子稳定结构,则BC2的电子式为_____其中B元素的化合价为______价。
(4)D3A2与H2O反应可生成两种碱,请写出该反应的化学方程式____________
(5)Y与X的原子序数之差为____________.
查看答案和解析>>
科目: 来源: 题型:
【题目】某制药有限公司生产有多种型号的钙尔奇D片剂,为测定某型号片剂中碳酸钙含量,进行如下实验:取10片该片剂碾碎后放入足量的盐酸中充分反应(假设盐酸只与碳酸钙反应)后过滤,取滤液加(NH4)2C2O4使Ca2+生成CaC2O4沉淀,沉淀过滤洗涤后溶解于强酸中并稀释成1L溶液,取20.00mL,然后用0.0500mol·L-1KMnO4溶液滴定,反应中用去12.00mLKMnO4溶液,发生反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
请回答:
(1)该型号片剂中每片含碳酸钙的质量为_____克
(2)该公司一种“钙尔奇D600片剂”(其主要成分与题中某型号的片剂相同,仅仅是碳酸钙的含量不同)的部分文字说明如下:“本品每片含主要成分碳酸钙1.5g(相当于钙元素600mg),成人每天服用1片”。则某型号的片剂应称为“钙尔奇D_____(填数字)片剂。”
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,当过量的Mg(OH)2固体在水溶液中达到平衡时:Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq),要使Mg(OH)2固体增加,c(OH-)增加,可采取的措施是
Mg2+(aq)+2OH-(aq),要使Mg(OH)2固体增加,c(OH-)增加,可采取的措施是
A.加适量的水B.通入少量HCl气体
C.加少量NaOH固体D.加少量MgSO4固体
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)量取12.00mL溶液所用玻璃仪器的名称是______。
(2)按系统命名法命法,有机物![]() 的名称是______。
的名称是______。
(3)CaH2是离子化合物,写出CaH2的电子式______。。
(4)乙醇沸点高于二甲醚的主要原因是______。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)熔融盐燃料电池具有高的发电效率,因而受到重视。可用熔融的碳酸盐作为电解质,向负极充入燃料气CH4,用空气与CO2的混合气作为正极的助燃气,以石墨为电极材料,制得燃料电池。工作过程中,CO![]() 移向________极(填“正”或“负”),已知CH4发生反应的电极反应式为_____________________________,则另一极的电极反应式为___________________________ 。
移向________极(填“正”或“负”),已知CH4发生反应的电极反应式为_____________________________,则另一极的电极反应式为___________________________ 。
(2)某实验小组同学对电化学原理进行了一系列探究活动。
1)如图为某实验小组设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________mol电子。
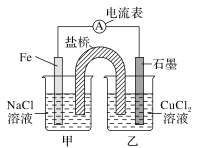
2)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示,
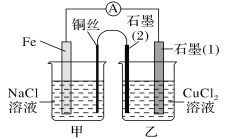
一段时间后,在甲装置铜丝附近滴加酚酞试液,现象是________________,电极反应为________________________;乙装置中石墨(1)为________极(填“正”“负”“阴”或“阳”),乙装置中与铜丝相连石墨(2)电极上发生的反应式为________________,产物常用________检验。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E五种物质是含钠元素的单质或化合物,其中B为淡黄色固体,它们有如图所示的转化关系:
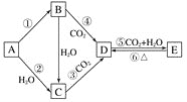
(1)推断各符号所代表的物质的化学式:A__,B__,C__,D__,E__。
(2)写出反应②的化学方程式:___。
(3)向D的饱和溶液中通入CO2时,反应的化学方程式为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上采用CO和H2合成再生能源甲醇,反应为:2H2(g)+CO(g)![]() CH3OH(g) ΔH<0
CH3OH(g) ΔH<0
(1)一定温度下,将1molCO与1molH2通入VL恒容密闭容器中发生反应。
①该反应能自发进行的条件是______(填“高温”、“低温”或“任意温度”)
②下列说法正确的是______。
A.v正(H2)=2v逆(CO)时,反应达到化学平衡状态
B.达到平衡时CO与H2的转化率相等
C.恒温恒压,往原料气中通入少量稀有气体,CO的转化率会降低
D.该反应的正反应活化能大于逆反应活化能
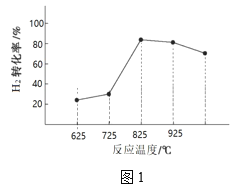
③图1为温度对H2合成甲醇反应的影响,请从反应速率和平衡的角度分析725℃以后H2百分含量随时间增长呈现该变化趋势的原因______。
(2)在恒温T、恒压P的条件下,将3.0molCO与4.5molH2通入容积可变的密闭容器中。达平衡时容器的体积为2L,CO的转化率为50%。
①此反应的正、逆反应速率与浓度的关系为v正=k正c(CO)·c2(H2),v逆=k逆c(CH3OH),其中k正、k逆为速率常数。在温度T下k正、k逆的关系式为k正=_____k逆。
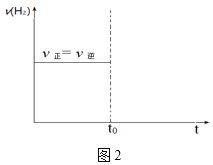
②若平衡时,在t0时刻再向容器中通入9.0molCO,在图2中画出充入CO后的v正、v逆随时间变化的图像_____。
(3)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,请写出生成甲醇的电极反应式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com