
科目: 来源: 题型:
【题目】已知pC=-lgc(B),室温下,某二元酸(H2A)中部分微粒的pC值随溶液pH值变化关系如图所示。下列说法错误的是( )
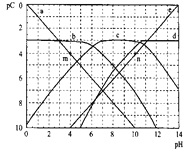
A.曲线a表示的微粒是H+
B.溶液中水的电离程度:m>n
C.pH=8时,溶液中,c(HA-)>c(H2A)
D.pH=1与pH=3时,H2A的浓度几乎相同
查看答案和解析>>
科目: 来源: 题型:
【题目】溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。
实验操作I:在试管中加入5mL 1mol/L NaOH水溶液和5mL溴乙烷,将试管按如图固定后,加热。
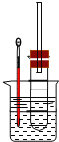
(1)请写出该反应的化学方程式_______。
(2)观察到_____现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)欲将生成的有机物从反应混合物中进行分离出来,最简单的操作是____(填操作名称)。
(4)请述如何检验溴乙烷中含有溴元素___________
实验操作Ⅱ:在试管中加入5 mL NaOH的乙醇溶液和5mL溴乙烷,将试管如图固定后,加热。
(5)请写出该反应的化学方程式_______。
(6)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是_______(写化学式),检验的方法是_________(需说明:所用的试剂、简单的实验操作及预测产生的实验现象)
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学—选修3:物质结构与性质]国务院批复通过的《全国矿产资源规划(2016﹣﹣2020年)》中,首次将萤石等24种矿产列入战略性矿产目录。萤石为氟化钙的俗名,其重要用途是生产氢氟酸。
(1)基态F原子核外电子共有_____种运动状态,基态Ca2+的最外层电子排布图为_____。
(2)实验室制氟化氢是用萤石与浓硫酸反应,但该反应不可以在玻璃器皿中进行,请用化学反应方程式解释原因_____,该反应涉及的元素电负性最大的是_____(用元素符号表示)。该反应的产物之一会与反应物继续反应生成H2SiF6,则H2SiF6分子的中心原子价层电子对数为_____。
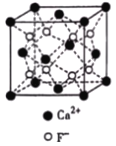
(3)CaF2与CaCl2熔点比较低的物质是_____,原因是_______________。CaF2晶胞如图,其中Ca2+的配位数为_____。在CaF2晶体中Ca2+的离子半径为a cm,F﹣的离子半径为bcm;则CaF2的密度为_____gcm﹣3(设阿伏加德罗常数的值为NA)。
查看答案和解析>>
科目: 来源: 题型:
【题目】经实验测定某固体样品中只含有Na2O2和Na2CO3。现称取该样品13.1g,加入水充分反应后产生1.12L(标准状况下)气体,所得溶液体积为500mL。试计算:
(1)该样品含有Na2O2的质量分数为_________。
(2)反应后溶液中Na+的物质的量浓度为_________mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关烷烃的说法中,正确的是( )
A.戊烷的同分异构体有2种,其习惯命名分别为:正戊烷、异戊烷
B.沸点:正丁烷<异丁烷
C.符合通式CnH2n+2(n≥0)的物质一定是烷烃的同系物
D.随着碳原子数的依次增加,烷烃中碳的质量分数逐渐增大,无限趋近于![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】绿水青山就是金山银山,生产生活中污染物的合理处理对环境保护具有重要意义。
(1)利用某些催化剂,成功实现将空气中的碳氧化合物和氮氧化合物转化为无毒的大气循环物质。
已知:① 2NO(g)+O2(g)![]() 2NO2(g)△H3=﹣112.0kJmol﹣1
2NO2(g)△H3=﹣112.0kJmol﹣1
② NO(g)+CO(g)![]()
![]() N2(g)+CO2(g)△H2=﹣379.9kJmol﹣1
N2(g)+CO2(g)△H2=﹣379.9kJmol﹣1
③ N2(g)+O2(g)![]() 2NO(g)△H1=+179.8kJmol﹣1
2NO(g)△H1=+179.8kJmol﹣1
则反应NO(g)+CO2(g)![]() NO2(g)+CO(g)的△H=_____kJmol﹣1;某温度下,反应①②③的平衡常数分別为K1、K2、K3,则该反应的K= ____(用K1、K2、K3表示)。
NO2(g)+CO(g)的△H=_____kJmol﹣1;某温度下,反应①②③的平衡常数分別为K1、K2、K3,则该反应的K= ____(用K1、K2、K3表示)。
(2)一定温度下,向某密闭容器中充入1 mol NO2,发生反应:2NO2(g) ![]() N2O4(g),测得反应体系中气体体积分数与压强之间的关系如图所示:
N2O4(g),测得反应体系中气体体积分数与压强之间的关系如图所示:
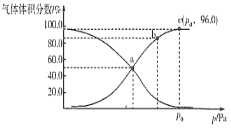
①a、b、c三点逆反应速率由大到小的顺序为___________。平衡时若保持压强、温度不变,再向体系中加入一定量的Ne,则平衡___________移动(填“正向”“逆向”或“不”)。
②a点时NO2的转化率为___________,用平衡分压代替平衡浓度也可求出平衡常数Kp,则该温度下Kp=___________Pa-1。
(3) 常温下,分别取未知浓度的HA和MOH溶液,加水稀释至原来体积的n倍。稀释过程中,两溶液的pH变化如图所示。
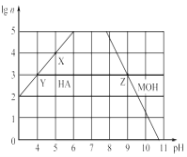
①HA为______酸,MOH为 ________碱(填“强”或“弱”);
②X、Y、Z三点水的电离程度关系是:________________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸亚铁可用于治疗缺铁性贫血。实验室里先制得硫酸亚铁,后将硫酸亚铁与碳酸氢钠反应制得碳酸亚铁(FeSO4+2NaHCO3![]() Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
Na2SO4+FeCO3↓+CO2↑+H2O)。实验装置如下图所示(部分夹持仪器略去)。
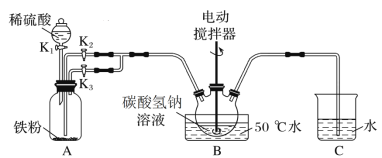
回答下列问题:
(1)A装置中发生反应的化学方程式是________。
(2)实验过程中,将生成的FeSO4溶液和NaHCO3溶液混合的操作是________。
(3)装置B发生反应生成FeCO3的离子方程式是______。
(4)碳酸亚铁在潮湿的空气中逐渐被氧化生成氢氧化铁和一种气体,反应的化学方程式为_________。
(5)配制溶液所用的蒸馏水必须先除去溶解的氧气,具体方法是_______。
(6)设计实验检验制得的产品中是否含Fe3+:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的四种短周期主族元素,X与Y位于同一主族,X与W能够形成多种化合物,其中一种为红棕色气体,Y与Z形成的一种化合物Y2Z2的分子结构模型为![]() 。下列叙述正确的是( )
。下列叙述正确的是( )
A.X与W、Y及Z均能组合成多种化合物B.简单离子半径:Y>Z>X>W
C.W的氧化物的水化物一定为强酸D.化合物Y2Z2中Y不满足8电子稳定结构
查看答案和解析>>
科目: 来源: 题型:
【题目】配制100 mL0.020mol/L KMnO4溶液的过程如下图所示:
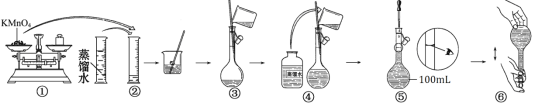
回答下列问题:
(1)图示中有两步操作不正确,它们是_____和_____ (填序号)。
(2)操作⑤图示中的两种仪器分别是________、 __________(填名称)。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将_______(填“偏大”或“偏小”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】扭曲烷( Twistane)是一种具有挥发性的环烷烃,其结构和球棍模型如图所示。下列说法正确的是( )

A.分子式为C10H18
B.与邻二乙苯互为同分异构体
C.分子结构中含有4个六元环
D.二氯代物多于3种(不含立体异构)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com