
科目: 来源: 题型:
【题目】已知![]() 为
为![]() 和
和![]() 的混合物,且知氧化性顺序:
的混合物,且知氧化性顺序:![]() ,取
,取![]() 样品进行如下图所示的实验:
样品进行如下图所示的实验:

(1)写出③步可能发生反应的3个离子方程式为________________________、________________________、________________________。
(2)若溶液E中只有一种金属离子,则一定是______;若D固体是纯净物,该固体是______。(填化学式)
(3)向溶液A中加入![]() 粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上__________________________________________。
粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有效去除大气中的NOx和SO2是环境保护的重要课题。
(1)酸性条件下,NaClO2吸收NO的相关热化学方程式如下:
4NO(g) + 3NaClO2(aq) + 2H2O(l) = 4HNO3(aq) + 3NaCl(aq) ΔH= a kJ·mol1
5NaClO2(aq) + 4HCl(aq) = 4ClO2(g) + 2H2O(l) + 5NaCl(aq) ΔH= b kJ·mol1
反应5NO(g) + 3ClO2(g) + 4H2O(l) = 5HNO3(aq) + 3HCl(aq) ΔH=________kJ·mol1。
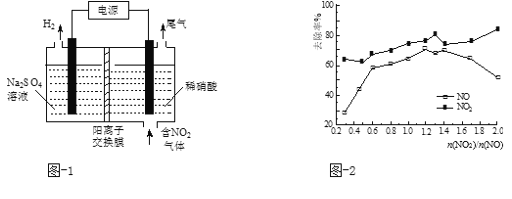
(2)用电解法处理氮氧化物可回收硝酸。实验室模拟电解NO2的装置如图-1所示。写出电解时阳极的电极反应式:________。
(3)用CO(NH2)2水溶液吸收SO2并通入O2,反应生成(NH4)2SO4和CO2。写出该反应的化学方程式:___________。
(4)利用活性焦炭的吸附作用,可以对烟气进行脱硫和脱硝。被吸附的NO2与活性焦炭反应生成N2和CO2,当生成1 mol N2时,转移的电子数为_________mol。
(5)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入0.05 mol·L1的Ca(OH)2乳浊液中,发生的反应为:3NO2 + 2OH-= NO +2NO3-+ H2O;NO + NO2 +2OH-= 2NO2- + H2O。改变![]() ,NOx的去除率见图-2。
,NOx的去除率见图-2。
①![]() 的合适范围是___________________。
的合适范围是___________________。
②当![]() 大于1.4时,NO2去除效率升高,但NO去除效率却降低。其可能的原因是______ 。
大于1.4时,NO2去除效率升高,但NO去除效率却降低。其可能的原因是______ 。
③O3和NO发生的主要反应为:NO + O3 = NO2 + O2。保持NO的初始浓度不变,改变![]() ,将反应后的混合气体通入0.05mol·L1Ca(OH)2乳浊液中吸收。为节省O3的用量,又能保持NOx去除效果,则
,将反应后的混合气体通入0.05mol·L1Ca(OH)2乳浊液中吸收。为节省O3的用量,又能保持NOx去除效果,则![]() 合适的值约为_________。
合适的值约为_________。
a.0.6 b.0.8 c.1.4
查看答案和解析>>
科目: 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用如图的实验装置测定Na2O2试样的纯度。
回答下列问题:

(1)装置A中盛放稀盐酸的仪器名称为__________________。
(2)装置B的作用是______________________________________。
(3)装置C的作用是____________________________________________。
(4)装置D中发生反应的化学方程式是_____________、_______________。
(5)装置E中碱石灰的作用是______________________________________。
(6)若开始时称得样品的质量为4.52 g,反应结束后称得固体的质量为6.36g,则Na2O2试样的纯度为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F六种元素,它们的相关信息如下:①原子序数依次增大,②A和C的L能层中都有两个未成对的电子,③C、D同主族且位于相邻周期,④E和F的原子序数相差3,F原子除最外能层只有1个电子外,其余各能层均全充满。根据以上信息填空(涉及的具体物质用元素符号或化学式回答):
(2)基态D原子中,具有______种不同能量的电子,E2+的价层电子轨道表达式是______。
(2)六种元素中电负性最强的元素是______。
(3)A元素的最高价氧化物中心原子采取的轨道杂化方式为______,D元素的最简单氢化物的VSEPR模型为______。
(4)与化合物AC2互为等电子体的分子的分子式为______(任写一种,下同),与化合物AC2互为等电子体且含有的元素只能是上述六种元素中的一价阴离子为______。
(5)某种化合物由D、E、F三种元素组成,其晶胞结构如图所示,则其化学式为______,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度:ρ=______g·cm-3(只要求列出计算式)。
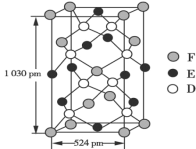
查看答案和解析>>
科目: 来源: 题型:
【题目】制备钙掺杂纳米Fe3O4,并模拟吸附废水中磷元素的主要实验流程如下:

已知:①CaO2能氧化溶液中的FeCl2,反应生成Fe(OH)3和Fe3+。
②掺杂的Ca2+嵌入Fe3O4中,洗涤时不损失,吸附时不形成Ca3(PO4)2等沉淀。
③溶液的pH对吸附剂表面所带电荷有影响。pH越高,表面所带负电荷越多; pH越低,表面所带正电荷越多。
(1)向FeCl2、FeCl3混合溶液中滴加NaOH溶液,一定条件下反应生成Fe3O4,其离子方程式为___________。
(2)步骤Ⅱ调节pH至11,共沉淀需在70℃条件下进行,适宜的加热方式为________。为提高共沉淀效果,还可采取的措施为_______________。
(3)磷元素的吸附效果、H3PO4水溶液中含磷物种分布分数与pH的关系分别如图1和图2所示。

①步骤Ⅳ用KH2PO4溶液模拟废水,测得酸性条件下(pH > 2)对磷元素吸附量较大,原因是:pH越低,吸附剂表面所带正电荷越多,有利于吸附阴离子;___________________
②步骤Ⅴ将吸附剂取出,用碱液解吸回收磷。结合表中数据,分析钙掺杂纳米Fe3O4吸附剂与其他类型吸附剂相比的优势有:________。
不同类型吸附剂对磷酸盐吸附能力比较
吸附剂 | 本产品 | 纯Fe3O4 | 陶瓷材质 |
吸附量/mg·g-1 | 24.1 | 5.0 | 12.5 |
(4)请设计从步骤Ⅱ反应结束后的烧瓶中获取钙掺杂纳米Fe3O4产品的实验方案:用磁铁将沉淀物和溶液分离,______________,用筛网筛分得到产品 (实验中须使用的试剂和仪器有:蒸馏水、无水乙醇、pH计、研钵、烘箱)。
查看答案和解析>>
科目: 来源: 题型:
【题目】净水剂能够改善水质,给人们的生活、健康带来很大的益处。
(1) 明矾[KAl(SO4)2·12H2O]是常见的净水剂。其在水中的电离方程式为_______;明矾可净水是因为在天然水中生成胶状Al(OH)3,Al(OH)3具有____的作用。
(2)碱式氯化铝(简称BAC)是高效净水剂的主要成分。实验室模拟利用铝土矿(主要含Al2O3,还含少量Fe2O3及其他不溶杂质)制取碱式氯化铝[Al2(OH)nCl6-n]的过程如下:

①盐酸溶解铝土矿过程中,发生反应的离子方程式为_____________、_______;溶解过程中需不断搅拌,目的是________________。
②加适量铝粉的主要作用是_______________。
③蒸发浓缩所需玻璃仪器为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】莲花清瘟胶囊对新冠肺炎轻症状患者有显著疗效,其有效成分绿原酸存在如图转化关系,下列有关说法正确的是
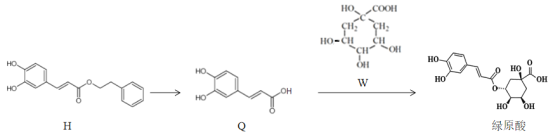
A.H的分子式为C17H14O4
B.Q中所有碳原子不可能都共面
C.1mol绿原酸与足量NaHCO3溶液反应,最多放出1molCO2
D.H、Q、W均能发生氧化反应、取代反应、显色反应
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究铁与氯气的反应,某同学甲设计了如下的实验方案及步骤。

实验装置图
(1)用注射器吸取20 mL左右的________(填化学式)。
(2)按图所示连接实验装置,并固定在铁架台上。经检验装置不漏气。在硬质玻璃管内加入一定量的细铁丝,一支试管内加入硫氰化钾溶液,另一支试管中加入氢氧化钠溶液。
(3)加热硬质玻璃管内铁丝约1 min,然后把注射器中的氯气注入到硬质玻璃管内,观察实验现象。硬质玻璃管内可观察到产生__________色的烟,盛硫氰化钾溶液的试管内显____________。
(4)请写出加入硫氰化钾溶液试管中所发生反应的离子方程式:_____________________。其中,氢氧化钠溶液的作用是______________。
(5)某同学取适量生成物溶于水得50.0mL溶液,加入足量的AgNO3溶液,得21.525g白色沉淀。则溶液中c(Cl-)=__________mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、X、Y、Z、Q、R、T 分别代表原子序数依次增大的短周期元素。元素A是原子半径最小的元素;X、Y、Z同周期且相邻,都是蛋白质的组成元素;X、R同族,Q与T原子的最外层电子数之和是R原子最外层电子数的2倍,T单质为淡黄色固体。U是d区元素,U2+的核外最高能级有2对成对电子。请回答下列问题:
(1)Y元素在周期表中的位置______,位于周期表______区;Q原子的核外电子排布式为______。
(2)X、Y、Z元素的第一电离能由大到小的顺序是______。
(3)TZ3分子为______分子(填“极性”或“非极性”),YZ2–离子实际构型是______。
(4)Z和T的简单气态氢化物稳定性好的是______(填化学式),原因是______。
(5)A、X、Z可形成分子式为A2XZ的有机物,则该化合物分子中X原子的轨道杂化类型是______;1mol该分子中含有π键的数目是______。(用“NA”表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,向![]() 盐酸中滴加
盐酸中滴加![]() 溶液,溶液的pH随
溶液,溶液的pH随![]() 溶液体积的变化如图。已知
溶液体积的变化如图。已知![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
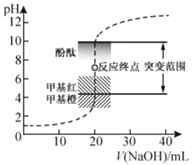
A.![]() 与盐酸恰好完全反应时,
与盐酸恰好完全反应时,![]()
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.![]() 时,
时,![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com