
科目: 来源: 题型:
【题目】含有K2Cr2O7的废水具有较强的毒性,工业上常用钡盐沉淀法处理含有K2Cr2O7的废水并回收重铬酸,具体的流程如下:

已知:CaCr2O7、BaCr2O7易溶于水,其它几种盐在常温下的溶度积常数如下表所示。
物质 | CaSO4 | CaCrO4 | BaCrO4 | BaSO4 |
溶度积 | 9.1×10-6 | 2.30×10-2 | 1.17×10-10 | 1.08×10-10 |
(1)用离子方程式表示K2Cr2O7溶液中同时存在K2CrO4的原因(将离子方程式补充完整):
![]() +__________=
+__________=![]() +__________。____________
+__________。____________
(2)向滤液1中加入BaCl2·2H2O的目的,是使![]() 从溶液中沉淀出来。
从溶液中沉淀出来。
①结合上述流程说明熟石灰的作用:__________。
②结合表中数据,说明选用Ba2+而不选用Ca2+处理废水的理由:__________。
③研究温度对![]() 沉淀效率的影响。实验结果如下:在相同的时间间隔内,不同温度下
沉淀效率的影响。实验结果如下:在相同的时间间隔内,不同温度下![]() 的沉淀率
的沉淀率 ,如下图所示。
,如下图所示。

已知:BaCrO4(s) ![]() Ba2+(aq)+
Ba2+(aq)+ ![]() ΔH>0
ΔH>0
![]() 的沉淀效率随温度变化的原因是__________。
的沉淀效率随温度变化的原因是__________。
(3)向固体2中加入硫酸,回收重铬酸。
①硫酸浓度对重铬酸的回收率如下图所示。结合化学平衡移动原理,解释使用0.450mol/L的硫酸时,重铬酸的回收率明显高于使用0.225mol/L的硫酸的原因:__________。

②回收重铬酸的原理如图所示。当硫酸浓度高于0.450mol/L时,重铬酸的回收率没有明显变化,其原因是__________。

(4)综上所述,沉淀BaCrO4并进一步回收重铬酸的效果与__________有关。
【答案】 1 H2O 2 2 H+ 沉淀![]() ;调节溶液pH,使
;调节溶液pH,使![]() 转化为
转化为![]() 而沉淀 BaCrO4比CaCrO4更难溶,可以使
而沉淀 BaCrO4比CaCrO4更难溶,可以使![]() 沉淀更完全 温度升高,沉淀速率加快 c(H2SO4)增大,则c(
沉淀更完全 温度升高,沉淀速率加快 c(H2SO4)增大,则c(![]() )增大,与Ba2+生成沉淀,促进BaCrO4(s)
)增大,与Ba2+生成沉淀,促进BaCrO4(s) ![]() Ba2+(aq)+
Ba2+(aq)+ ![]() (aq)ΔH>0平衡右移,c(
(aq)ΔH>0平衡右移,c(![]() )增大;同时,c(H+)也增大,共同促进
)增大;同时,c(H+)也增大,共同促进![]() +H2O
+H2O![]()
![]() +2H+平衡左移,有利于生成更多的H2Cr2O7 BaSO4与BaCrO4溶解度接近,c(H2SO4)越大,越有利于生成BaSO4,包裹在BaCrO4外,使其难于接触H2SO4,阻碍重铬酸生成 受到溶液pH、温度、H2SO4浓度、BaCrO4颗粒大小等影响
+2H+平衡左移,有利于生成更多的H2Cr2O7 BaSO4与BaCrO4溶解度接近,c(H2SO4)越大,越有利于生成BaSO4,包裹在BaCrO4外,使其难于接触H2SO4,阻碍重铬酸生成 受到溶液pH、温度、H2SO4浓度、BaCrO4颗粒大小等影响
【解析】含有K2Cr2O7的废水同时含有SO42,加入适量熟石灰过滤得到的固体1为硫酸钙和滤液1,向滤液1中加入BaCl22H2O的目的是使CrO42从溶液中沉淀出来,过滤得到固体2为BaCrO4,滤液2检测CrO42含量达标,向固体2中加入硫酸,回收重铬酸,同时生成固体3为硫酸钡沉淀。
(1). K2Cr2O7溶液中同时存在K2CrO4的原因是重铬酸根离子在水溶液中存在化学平衡生成铬酸根离子和氢离子,反应的离子方程式为Cr2O72+H2O2CrO42+2H+,故答案为:1、H2O、2、2、H+;
(2). ①. 根据表中物质的溶度积常数可知,熟石灰的作用是沉淀硫酸根离子,调节溶液pH使Cr2O72转化为CrO42而沉淀,故答案为:沉淀SO42-,调节溶液pH,使Cr2O72转化为CrO42而沉淀;
②. 根据表中数据可知,BaCrO4比CaCrO4更难溶,所以选用Ba2+处理废水可以使CrO42沉淀更完全,故答案为:BaCrO4比CaCrO4更难溶,可以使CrO42沉淀更完全;
③. 根据图象可知,CrO42的沉淀率随温度升高增大,沉淀速率加快,故答案为;温度升高,沉淀速率加快;
(3). ①. c(H2SO4)增大,则c(SO42-)增大,与Ba2+生成沉淀,促使![]() Ba2+(aq)+CrO42(aq)平衡右移,使c(CrO42)增大,同时c(H+)也增大,共同促使Cr2O72+H2O
Ba2+(aq)+CrO42(aq)平衡右移,使c(CrO42)增大,同时c(H+)也增大,共同促使Cr2O72+H2O![]() 2CrO42+2H+平衡左移,可以生成更多的H2Cr2O7,故答案为:c(H2SO4)增大,则c(SO42-)增大,与Ba2+生成沉淀,促使BaCrO4(s)
2CrO42+2H+平衡左移,可以生成更多的H2Cr2O7,故答案为:c(H2SO4)增大,则c(SO42-)增大,与Ba2+生成沉淀,促使BaCrO4(s) ![]() Ba2+(aq)+CrO42(aq)平衡右移,c(CrO42)增大,同时c(H+)也增大,共同促使Cr2O72+H2O
Ba2+(aq)+CrO42(aq)平衡右移,c(CrO42)增大,同时c(H+)也增大,共同促使Cr2O72+H2O![]() 2CrO42+2H+平衡左移,可以生成更多的H2Cr2O7;
2CrO42+2H+平衡左移,可以生成更多的H2Cr2O7;
②. 根据表中各物质的溶度积常数可知,BaSO4与BaCrO4溶解度比较接近,c(H2SO4)越大,越有利于生成BaSO4,包裹在BaCrO4外,使其难与H2SO4接触,阻碍重铬酸生成,故答案为:BaSO4与BaCrO4溶解度接近,c(H2SO4)越大,越有利于生成BaSO4,包裹在BaCrO4外,使其难于接触H2SO4,阻碍重铬酸生成;
(4). 根据上述分析可知,沉淀BaCrO4并进一步回收重铬酸的效果与温度、浓度、溶液pH、硫酸浓度、沉淀颗粒等有关,受到溶液pH、温度、H2SO4浓度、BaCrO4颗粒大小等因素的影响,故答案为:受到溶液pH、温度、H2SO4浓度、BaCrO4颗粒大小等影响。
【题型】综合题
【结束】
19
【题目】以Na2SO3溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间反应的多样性。
实验 | 试剂 | 现象 | |
滴管 | 试管 | ||
| 0.2mol·L-1Na2SO3溶液 | 饱和Ag2SO4溶液 | Ⅰ.产生白色沉淀 |
0.2mol·L-1CuSO4 | Ⅱ.溶液变绿,继续滴加产生棕黄色沉淀 | ||
0.1mol·L-1Al2(SO4)3溶液 | Ⅲ.开始无明显变化,继续滴加产生白色沉淀 | ||
(1)经验检,现象Ⅰ中的白色沉淀是Ag2SO3。用离子方程式解释现象Ⅰ:__________。
(2)经检验,现象Ⅱ的棕黄色沉淀中不含![]() ,含有Cu+、Cu2+和
,含有Cu+、Cu2+和![]() 。
。
已知:Cu+![]() Cu+Cu2+,Cu2+
Cu+Cu2+,Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
①用稀硫酸证实沉淀中含有Cu+的实验现象是__________。
②通过下列实验证实,沉淀中含有Cu2+和![]() 。
。

a.白色沉淀A是BaSO4,试剂1是__________。
b.证实沉淀中含有Cu2+和![]() 的理由是__________。
的理由是__________。
(3)已知:Al2(SO3)3在水溶液中不存在。经检验,现象Ⅲ的白色沉淀中无![]() ,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
,该白色沉淀既能溶于强酸,又能溶于强碱,还可使酸性KMnO4溶液褪色。
①推测沉淀中含有亚硫酸根和__________。
②对于沉淀中亚硫酸根的存在形式提出两种假设:
i.Al(OH)3所吸附;
ii.存在于铝的碱式盐中。对假设ii设计了对比实验,证实了假设ii成立。
a.将对比实验方案补充完整。
步骤一:

步骤二:__________(按上图形式呈现)。
b.假设ii成立的实验证据是__________。
(4)根据实验,亚硫酸盐的性质有__________。盐溶液间反应的多样性与__________有关。
查看答案和解析>>
科目: 来源: 题型:
【题目】酰苯胺作为一种常用药,具有解热镇痛的效果。实验室制备乙酰苯胺时,可以用苯胺与乙酸酐加热来制取,该反应放热:
密度(g/mL) | 相对分子质量 | 颜色、状态 | 溶解性 | |
苯胺 | 1.04 | 93 | 无色油状液体 | 微溶于水, 易溶于乙醇、乙醚 |
乙酸酐 | 1.08 | 102 | 无色透明液体 | 遇水缓慢反应生成乙酸 |
乙酰苯胺 | 135 | 无色片状晶体, 熔点 114℃ | 不溶于冷水,可溶于热 水、乙醇、乙醚 |
实验步骤
①取5.00 mL苯胺,倒入100 mL锥形瓶中,加入20 mL水,在旋摇下分批加入6.00 mL 乙酸酐,搅拌均匀。若有结块现象产生,用玻璃棒将块状物研碎,再充分搅拌;
②反应完全后,及时把反应混合物转移到烧杯中,冷却后,抽滤,洗涤,得粗乙酰苯胺固体;
③将粗产品转移至150 mL烧杯中,加入适量水配制成 80 ℃的饱和溶液,再加入过量20%的水。稍冷后,加半匙活性炭,搅拌下将溶液煮沸3~5 min,_______,冷却结晶,抽滤、洗涤、晾干得乙酰苯胺纯品6.2 g。
请回答:
(1)反应温度过高会导致苯胺挥发,下列操作可控制反应温度,防止反应温度升高过快的是______。
A 加20 mL水 B 旋摇下分批加入6.0 mL乙酸酐
C 玻璃棒将块状物研碎 D 充分搅拌
(2)在步骤②中对粗产品进行洗涤需要用到以下操作:
a 加入洗涤剂至浸没固体;b 洗涤剂缓慢通过;c 关小水龙头;d 开大水龙头; e 重复 2~3 次。
请对以上操作做出正确的排序__________。
(3)步骤③加入过量 20%的水的目的是________,横线处的操作步骤是_________。
(4)下列说法不正确的是______。
A 活性炭吸附有色物质,可以提高产率
B 冷却时,室温冷却比冰水浴冷却更易得到大颗粒晶体便于抽滤
C 抽滤用如图装置,为防止倒吸,结束时可先关闭水龙头,后打开活塞a
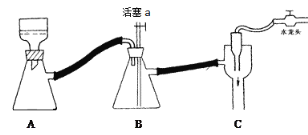
D 产品可放在表面皿上用热水浴烘干,烘干后可通过测量产品熔点判断产品纯度
(5)该实验的产率是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国首架国产大飞机C919采用的先进材料主要有第三代铝锂合金、碳纤维复合材料及钛合金等。回答下列问题:
![]() 基态原子核外电子排布式为______,其核外电子占据最高能层的符号是______。
基态原子核外电子排布式为______,其核外电子占据最高能层的符号是______。
![]() 电子结合能是指在中性原子中当其他电子均处在可能的最低能态时,某电子从指定的轨道上电离时所需能量的负值。Li的2s轨道电子结合能比1s轨道的______
电子结合能是指在中性原子中当其他电子均处在可能的最低能态时,某电子从指定的轨道上电离时所需能量的负值。Li的2s轨道电子结合能比1s轨道的______![]() 填“大”或“小”
填“大”或“小”![]() ,原因是______。
,原因是______。
![]() 基碳纤维是以聚丙烯腈纤维为原料的碳纤维。丙烯腈
基碳纤维是以聚丙烯腈纤维为原料的碳纤维。丙烯腈![]() 分子中
分子中![]() 键和
键和![]() 键的个数比为______,碳原子间共价键的键角约为______。
键的个数比为______,碳原子间共价键的键角约为______。
![]() 工业上用镁还原
工业上用镁还原![]() 的方法制备金属钛,元素Mg、Ti、Cl的电负性分别为
的方法制备金属钛,元素Mg、Ti、Cl的电负性分别为![]() 、
、![]() 、
、![]() ,
,![]() 的熔点______
的熔点______![]() 的熔点
的熔点![]() 填“高于”或“低于”
填“高于”或“低于”![]() 。
。
![]() 钛存在两种同素异构体,
钛存在两种同素异构体,![]() 采纳六方最密堆积,
采纳六方最密堆积,![]() 采纳体心立方堆积,鉴别两种钛晶体可以用______法,由
采纳体心立方堆积,鉴别两种钛晶体可以用______法,由![]() 转变为
转变为![]() 晶体体积______
晶体体积______![]() 填“膨胀”或“收缩”
填“膨胀”或“收缩”![]() 。
。
![]() 由Ba、Ti和O组成的三元离子晶体中,晶胞的顶点被
由Ba、Ti和O组成的三元离子晶体中,晶胞的顶点被![]() 占据,体心被
占据,体心被![]() 占据,面心被
占据,面心被![]() 占据,晶胞参数
占据,晶胞参数![]() ,该晶体的化学式为______。
,该晶体的化学式为______。![]() 为140pm,则
为140pm,则![]() 为______
为______![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知断裂1 mol共价键所需要吸收的能量分别为H—H:436 kJ,I—I:151 kJ,H—I:299 kJ,下列对H2(g)+I2(g)![]() 2HI(g)的反应类型判断错误的是( )
2HI(g)的反应类型判断错误的是( )
A.放出能量的反应B.吸收能量的反应
C.氧化还原反应D.可逆反应
查看答案和解析>>
科目: 来源: 题型:
【题目】火柴头中含有Cl元素的证明,有同学设计了以下实验流程图:

(1)实验中发生的离子反应是______________________
(2)有人提出上述方法中出现白色沉淀并不能充分说明火柴头上 KClO3的存在,其理由是________。如何解决这个问题____________
(3)实验测得火柴头中KClO3的质量分数为____________;未洗涤沉淀,测得KClO3的质量分数将_________(填 “偏大”、“偏小”、或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(NH4)2SO3氧化是氨法脱硫的重要过程。某小组在其他条件不变时,分别研究了一段时间内温度和(NH4)2SO3初始浓度对空气氧化(NH4)2SO3速率的影响,结果如图。下列说法不正确的是
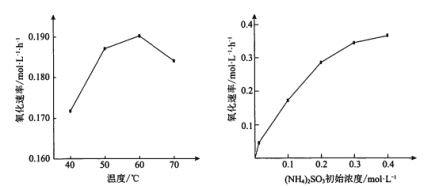
A.60℃之前,氧化速率增大与温度升高化学反应速率加快有关
B.60℃之后,氧化速率降低可能与O2的溶解度下降及(NH4)2SO3受热易分解有关
C.(NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,与SO32-水解程度增大有关
D.(NH4)2SO3初始浓度增大到一定程度,氧化速率变化不大,可能与O2的溶解速率有关
查看答案和解析>>
科目: 来源: 题型:
【题目】HI常用作有机反应中的还原剂,受热会发生分解反应。已知443℃时:2HI(g)![]() H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )
H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )

A.0~20min内的平均反应速率可表示为v(H2)=0.0045mol·L-1·min-1
B.升高温度,再次平衡时,c(HI)>0.78mol·L-1
C.该反应的化学平衡常数计算式为![]()
D.反应进行40 min时,体系吸收的热量约为0.94kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,判断下列叙述中正确的是

A.每生成2分子AB吸收b kJ热量
B.该反应的反应热ΔH= +(a-b)kJ·mol-1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1mol A-A键和1mol B-B键,放出a kJ能量
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)①0.1 mol/L (NH4)2SO4溶液中各种离子的浓度由大到小顺序为__________。
②用离子方程式表示NaHCO3溶液显碱性的原因:______________。实验室中配制FeCl3溶液时常加入________溶液以抑制其水解。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=____________mol/L,在pH=3的CH3COOH溶液中,水电离出的c(H+)=__________ mol/L。
(3)利用反应Cu + H2O2 + H2SO4 = CuSO4 + 2H2O设计一个原电池,回答下列问题:
①负极材料为____________;正极反应式为__________________________。
②反应过程中SO42-向_______极移动。
③当电路中转移0.1mol电子时,电解液质量(不含电极)增加了______克。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在体积均为20mL、浓度均为0.1mol/L的HX溶液、HY溶液中分别滴加0.1mol/L的NaOH溶液,反应后溶液中水电离的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加NaOH溶液体积的关系如图所示。下列推断正确的是
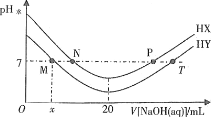
A.HX的电离方程式为HX=H++X-
B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-)
C.常温下用蒸馏水分别稀释N、P点溶液,pH都一定降低
D.常温下,HY的电离常数![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com