
科目: 来源: 题型:
【题目】下列反应物按所给物质的量配比进行反应,其中固体完全反应的是( )
A.n(Cu):n(HNO3浓)=1:4B.n(Fe):n(HNO3浓)=1:2
C.n(C):n(H2SO4浓)=1:2D.n(MnO2):n(HCl浓)=1:4
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,将3molA和1molB两种气体混合于2L恒容密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g)。2min末该反应达平衡,生成0.8molD,并测得C的浓度为0.2 mol·L-1。下列判断正确的是( )
xC(g)+2D(g)。2min末该反应达平衡,生成0.8molD,并测得C的浓度为0.2 mol·L-1。下列判断正确的是( )
A.x=2B.2min内B的反应速率为0.2 mol·L-1·min-1
C.A的转化率为40%D.若混合气体的密度不变,则表明该反应已达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B. 绿色化学要求从源头上消除或减少生产活动对环境的污染
C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D. 天然气和液化石油气是我国目前推广使用的清洁燃料
查看答案和解析>>
科目: 来源: 题型:
【题目】氯水中存在多种分子和离子,它们在不同的反应中表现出不同的性质。下列结论正确的是( )
A. 加入有色布条,片刻后有色布条褪色,说明有Cl2存在
B. 溶液呈浅黄绿色,且有刺激性气味,说明有Cl2存在
C. 先加入盐酸酸化,再加入AgNO3溶液,生成白色沉淀,说明有Cl-存在
D. 加入NaOH溶液,氯水的浅黄绿色消失,说明有HClO存在
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对图像的叙述正确的是
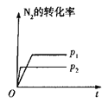

甲 乙 丙 丁
A.图甲可表示压强对反应:![]()
![]() 的影响
的影响
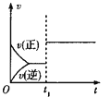
B.图乙中,![]() 时刻改变的条件一定是加入了催化剂
时刻改变的条件一定是加入了催化剂
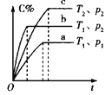
C.若图丙表示反应:![]() ,则
,则![]() 、
、![]()
D.图丁表示水中![]() 和
和![]() 的关系,ABC所在区域总有
的关系,ABC所在区域总有![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等。已知:饱和NaClO2溶液在温度低于38℃时析出NaCO23H2O晶体,温度高于38℃时析出NaClO2晶体,温度高于60℃时,NaClO2分解生成NaClO3和NaCl。其生产工艺如图所示。
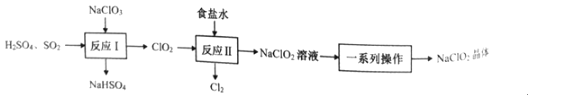
回答下列问题:
(1)NaClO2中氯元素的化合价为__。
(2)“反应Ⅰ”中氧化剂与还原剂的物质的量之比为__。
(3)“反应”所用“食盐水”由粗盐水精制而成。精制时,为除去粗盐水中的Ca2+、Mg2+和SO42-,需要用到试剂:①NaOH溶液②Na2CO3溶液③BaCl2溶液④稀盐酸,所用试剂的加入顺序正确的是__。(填标号)
A.①②③④
B.②①③④
C.③①②④
D.③②①④
(4)“一系列操作”为蒸发浓缩、趁热过滤、__、干燥,其中“趁热过滤”应控制的温度范围是__。
(5)“反应Ⅱ”产生的Cl2可用于制备含氯消毒剂。将Cl2通入足量NaOH溶液中,加热后得到NaCl、NaCIO、NaClO3的混合液。经测定ClO-与ClO3-的物质的量浓度之比为3:1,则Cl2与NaOH溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.向0.1mol/L 100mL CH3COONa的溶液中再加0.1mol CH3COONa固体后c(CH3COO-)/c(Na+)变大
B.向0.1mol/L的二元弱酸盐Na2A中不断通入HCl(g),则c(H+)/c(H2A)先变大后变小
C.已知:FeCl3(aq)+ 3KSCN(aq)![]() 3KCl(aq)+Fe(SCN)3(aq),向该平衡体系中加入固体KCl后溶液颜色变浅
3KCl(aq)+Fe(SCN)3(aq),向该平衡体系中加入固体KCl后溶液颜色变浅
D.室温时,0.1mol/L NH4HCO3溶液pH=8.1,则Ka1(H2CO3) >Kb(NH3·H2O)>Ka2(H2CO3)
查看答案和解析>>
科目: 来源: 题型:
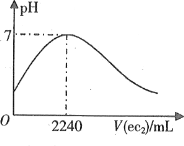
【题目】短周期元素a、b、c、d、e的原子序数依次增大。a的简单阴离子与锂离子具有相同的电子层结构,b原子最外层电子数等于内层电子数的2倍。d的单质与稀盐酸剧烈反应放出a2。在1L0.2mol·L-1a2e的水溶液中缓慢通入ec2气体,该溶液的pH与ec2气体体积(标准状况)的关系如图所示。下列说法不正确的是
A.a和b可构成所有原子共平面的分子
B.在b、c、e的气态氢化物中,c的最稳定
C.d的氯化物一定能破坏水的电离平衡
D.e的最高价含氧酸与其氢化物可能发生氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)基态Cu原子的核外电子排布式为____________________
(2)从原子轨道重叠方式考虑,氮分子中的共价键类型有____________;
(3)![]() 水溶液中
水溶液中
①水分子中氧原子的杂化类型是_____,![]() 键键角____
键键角____![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]()
②不存在的微粒间作用力有______ 。
A.离子键 ![]() 极性键
极性键 ![]() 配位键
配位键 ![]() 氢键
氢键 ![]() 范德华力
范德华力
(4)黄铜矿冶炼铜时产生的![]() 可经过
可经过![]() 途径形成酸雨。
途径形成酸雨。
①![]() 的空间构型为________。从结构角度,解释
的空间构型为________。从结构角度,解释![]() 的酸性强于
的酸性强于![]() 的原因是_______
的原因是_______
②已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域![]() 键”
键”![]() 或大
或大![]() 键
键![]() 。大
。大![]() 键可用
键可用![]() 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大![]() 键的原子个数和电子数,如苯分子中大
键的原子个数和电子数,如苯分子中大![]() 键表示为
键表示为![]() 。下列微粒中存在“离域
。下列微粒中存在“离域![]() 键”的是_____;
键”的是_____;
A.![]() B.
B.![]() C.
C.![]()
③铜晶体中Cu原子的堆积方式如图①所示,其堆积方式为_____,配位数为_______.

④金铜合金的晶胞如图②所示。金铜合金具有储氢功能,储氢后Au原子位于顶点,Cu原子位于面心,H原子填充在由1个Au原子和距Au原子最近的3个Cu原子构成的四面体空隙中,若Cu原子与Au原子的最短距离为![]() ,阿伏加德罗常数的位为
,阿伏加德罗常数的位为![]() ,则该晶体储氢后密度为______
,则该晶体储氢后密度为______![]() 列出计算式
列出计算式![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】把0.6mol X气体和0.6mol Y气体混合于2L密闭容器中,使它们发生如下反应:2X(g)+Y(g)=nM(g)+2W(g)2min 末,若测知以W 的浓度变化表示的反应速率为0.05molL﹣1min﹣1,容器内气体的总物质的量与反应前容器内气体的总物质的量之比为5:4,则:
(1)前2min内用Y的浓度变化表示的平均反应速率为___________。
(2)2min末时X的浓度为_________。
(3)化学反应方程式中n的值是____________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com