
科目: 来源: 题型:
【题目】已知甲为恒压容器、乙为恒容容器。相同条件下充入等物质的量NO2气体,且起始时体积相同。发生反应:2NO2(g) ![]() N2O4(g) ΔH<0一段时间后相继达到平衡状态。下列说法中正确的是( )
N2O4(g) ΔH<0一段时间后相继达到平衡状态。下列说法中正确的是( )

A.平衡时NO2体积分数:甲<乙
B.乙比甲先达到平衡状态
C.该反应的平衡常数表达式![]()
D.NO2的平衡转化率:甲<乙
查看答案和解析>>
科目: 来源: 题型:
【题目】已知汽车尾气无害化处理反应为2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)。下列说法正确的是
N2(g)+2CO2(g)。下列说法正确的是
A.升高温度可使该反应的逆反应速率降低
B.达到化学平衡时,化学反应已经停止
C.v正(NO)=v正(CO2)时,说明达到了化学平衡
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是425℃时,在1 L密闭容器中发生化学反应的浓度随时间的变化示意图。下列叙述错误的是
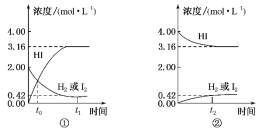
A.图①中t0时,三种物质的物质的量相同
B.图①中t0时,反应达到平衡状态
C.图②中的逆反应为H2(g)+I2(g) ![]() 2HI(g)
2HI(g)
D.图①②中当c(HI)=3.16 mol·L-1时,反应达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】燃煤脱硫可减少SO2尾气的排放,燃煤脱硫技术受到各界科研人员的关注。一种燃煤脱硫技术的原理是:CaO(s)+3CO(g)+SO2(g)![]() CaS(s)+3CO2(g) △H=-394.0kJ/mol。保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度):
CaS(s)+3CO2(g) △H=-394.0kJ/mol。保持其他条件不变,不同温度下起始CO物质的量与平衡时体系中CO2的体积分数的关系如图所示(T表示温度):
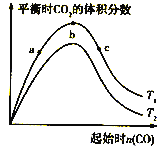
下列有关说法正确的是
A. T1比T2高 B. b点SO2转化率最高
C. b点后曲线下降是因CO体积分数升高 D. 减小压强可提高CO、SO2转化率
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.二氯化砜(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2反应制取少量的SO2Cl2。装置如图(有些支持装置省略了)所示。已知SO2Cl2的熔点为-54.1℃,沸点为69. 1℃;常温下比较稳定,受热易分解,遇水能发生剧烈的水解反应,产物之一为氯化氢气体。
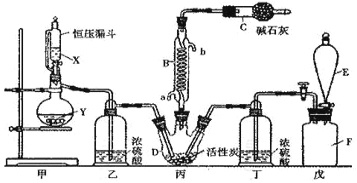
(1)仪器E的名称是_____________,由B的使用可知SO2与氯气之间的反应属于______(填“放”或“吸”)热反应,B处反应管冷却水应从____________ (填“a”或“b”)接口通入。如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是_______________________________________。
(2)试剂X、Y的组合最好是_________。
a.98%硫酸和铜 b.稀硝酸和亚硫酸钠固体 c.60%硫酸和亚硫酸钾固体
(3)戊是贮气装置,则E中的试剂是_________;若缺少装置乙和丁,潮湿的氯气和二氧化硫之间发生反应的化学方程式是___________________________.
(4)取1.00g蒸馏后的液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.50g,则所得馏分中二氯化砜的质量百分含量为___________ %(结果保留小数点后1位)。
(5)二氯化砜应储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是_______________________________。
Ⅱ.乙同学设计了一套电解饱和食盐水的实验装置,来验证氯气的某些性质和测定产生的氢气的体积。
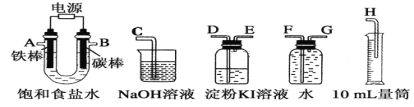
(1)所选仪器接口的连接顺序是A接________,________接________;B接________,________接________。
(2)若装入的饱和食盐水为100mL(氯化钠足量,电解前后溶液体积变化可忽略,假设两极产生的气体全部逸出),当测得氢气为112mL(标准状况下)时停止通电。将U形管内的溶液倒入烧杯,常温时测得溶液的pH约为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g) ![]() 2Z(g) ΔH< 0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
2Z(g) ΔH< 0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10-3 mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v正)
C.其他条件不变,向平衡体系中再充入0.16mol气体X,与原平衡相比,达到新平衡时,气体Y的转化率增大,X的体积分数增大,Z的体积分数减少
D.保持其他条件不变,起始时向容器中充入0.32mol气体X和0.32mol气体Y,到达平衡时,n(Z)<0.24mol
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下某体积一定的密闭容器中发生的反应aA(g)+bB(g)![]() xC(g)符合下图甲所示关系(c%表示平衡混合气体中C的百分含量,T表示温度,p表示压强)。则图乙中纵轴y是指
xC(g)符合下图甲所示关系(c%表示平衡混合气体中C的百分含量,T表示温度,p表示压强)。则图乙中纵轴y是指

A. 平衡混合气的密度
B. 平衡混合气中B的百分含量
C. 平衡混合气的总物质的量
D. 平衡混合气的平均相对分子质量
查看答案和解析>>
科目: 来源: 题型:
【题目】离子液体是一种只由离子组成的液体,在低温下也能以液态稳定存在,是一种很有研究价值的溶剂。对离子液体的研究显示最常见的离子液体主要由以下的正离子和负离子组成:
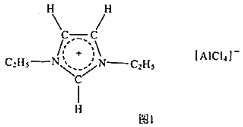
回答下列问题:
(1)![]() 在周期表中的位置是______,其价电子排布式为______图1中负离子的空间构型为______。
在周期表中的位置是______,其价电子排布式为______图1中负离子的空间构型为______。
(2)氯化铝的熔点为![]() ,氮化铝的熔点高达
,氮化铝的熔点高达![]() ,它们都是活泼金属和非金属的化合物,熔点相差这么大的原因是______。
,它们都是活泼金属和非金属的化合物,熔点相差这么大的原因是______。
(3)图中正离子有令人惊奇的稳定性,它的电子在其环状结构中高度离域。该正离子中N原子的杂化方式为______,C原子的杂化方式为______。
(4)为了使正离子以单体形式存在以获得良好的溶解性能,与N原子相连的![]() 不能被H原子替换,请解释原因:______。
不能被H原子替换,请解释原因:______。
(5)![]() 、Mg、Al三种元索的第一电离能由大到小的顺序是______。
、Mg、Al三种元索的第一电离能由大到小的顺序是______。
(6)已知氮化铝的晶胞结构如图2所示。晶体中氮原子堆积方式如图3所示,这种堆积方式称为______。六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为N,氮化铝晶体的密度为______![]() 列出计算式
列出计算式![]() 。
。
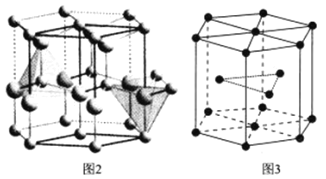
查看答案和解析>>
科目: 来源: 题型:
【题目】丹参素能明显抑制血小板的聚集。其结构如图所示,下列有关说法正确的是
![]()
A. 丹参素苯环上最多能与3mol Br2反应
B. 在Ni催化下1 mol丹参素最多可与4 mol H2加成
C. 1 mol丹参素在一定条件下与足量金属钠反应可生成4 mol H2
D. 丹参素能发生取代、消去、中和、氧化等反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+n(B)(g) ![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
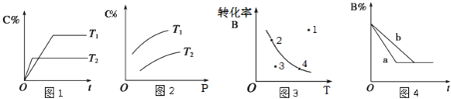
A.由图1可知,T1<T2,该反应正反应为吸热反应
B.由图2可知,该反应m+n<p
C.图3中,表示反应速率v(正)>v(逆)的是点3
D.图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com