
科目: 来源: 题型:
【题目】下表中是A、B、C、D、E五种短周期元素的某些性质,下列判断正确的是( )

A. C、D、E的氢化物的稳定性:C>D>E
B. 元素A的原子最外层轨道中无自旋状态相同的电子
C. 元素B、C之间不可能形成化合物
D. 与元素B同周期且第一电离能最小的元素的单质能与H2O发生置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】以A(α-蒎烯)为原料可制备香料中间体D和H,合成路线如下:
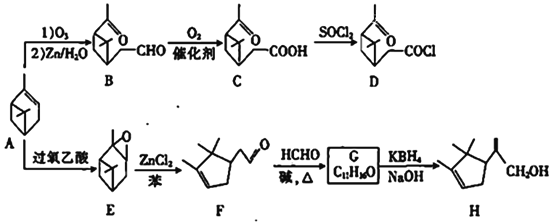
已知:①R1CHO+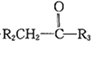
![]()
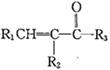 (R1、R2、R3为H或烃基)
(R1、R2、R3为H或烃基)
②一定条件下,R-C≡C-OH可存在。
回答下列问题:
(1)A中的官能团名称是____________,E的分子式为___________
(2)C生成D的反应类型是___________
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳。E中有________个手性碳。
(4)G的结构简式为___________
(5)H与足量Br2的CCl4溶液反应的化学方程式为_____________________
(6)W是B的同分异构体,W中没有环状结构,一定条件下,W能水解生成X和Y,X能与NaHCO3反应生成CO2,其核磁共振氢谱只有两组峰,峰面积之比为1:1,Y的核磁共振氢谱有三组峰,蜂面积之比为9:6:1,W的可能结构有_______种.
(7)设计由苯酚制备![]() 的合成路线(无机试剂任选)_________________。
的合成路线(无机试剂任选)_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得滴定曲线如图。下列说法不正确的是( )

A. 在曲线上任一点均存在:c(Na+)c(OH-) = c(CH3COO-)c(H+)
B. 点①所示溶液中:c(CH3COO-)+2c(OH-) = c(CH3COOH)+2c(H+)
C. 点②所示溶液中:c(Na+) = c(CH3COO-)
D. 点③所示溶液中:c(Na+) > c(OH-) > c(CH3COO-) > c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】现有 A、B、C、D、E、F 六种短周期主族元素,原子序数依次增大。已知 A 的气态氢化物能与其最高价氧化物对应的水化物反应得到一种离子化合物,B 的一种单质具有杀菌消毒的作用,C+和 D3+的电子层结构相同,E 的主族序数是其周期序数的2倍。
(1)F 在元素周期表中的位置是__________________。
(2)上述元素形成的简单离子中,半径最大的是__________________ (填离子符号)
(3)由上述元素中的一种或几种组成的物质甲可以发生如图反应:
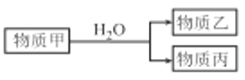
①若丙具有漂白性,则甲和水反应的离子方程式为_________________。
②若乙的水溶液是强碱性溶液,物质丙为B 的一种单质,则甲中含有的化学键类型为_______________,D 的单质与乙的水溶液反应的离子方程式为______________。
(4)A 的最高价氧化物对应的水化物的稀溶液与金属铜反应的离子方程式为_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】环己烯是重要的化工原料。其实验室制备流程如下:
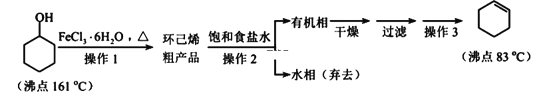
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为____________,现象为__________________。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
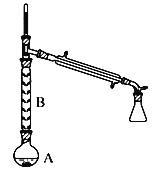
①烧瓶A中进行的可逆反应化学方程式为___________________,浓硫酸也可作该反应的催化剂,选择FeCl36H2O而不用浓硫酸的原因为________________(填序号)。
a.浓硫酸易使原料炭化并产生SO2
b. FeCl36H2O污染小、可循环使用,符合绿色化学理念
c.同等条件下,用FeCl36H2O比浓硫酸的平衡转化率高
②仪器B的作用为____________。
(3)操作2用到的玻璃仪器是____________。
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,____________,弃去前馏分,收集83℃的馏分。
Ⅱ.环己烯含量的测定
在一定条件下,向ag环己烯样品中加入定量制得的bmolBr2,与环己烯充分反应后,剩余的Br2与足量KI作用生成I2,用cmolL-1的Na2S2O3标准溶液滴定,终点时消耗Na2S2O3标准溶液vml (以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①Br2+![]() →
→![]()
②![]()
③![]()
(5)样品中环己烯的质量分数为___________(用字母表示)。
(6)下列情况会导致测定结果偏低的是____________(填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c. Na2S2O3标准溶液部分被氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下,4.48L的Cl2通入水中反应转移的电子数为0.2NA
B.常温下pH=3的FeCl3溶液中由水电离出的H+的数目为0.001NA
C.273K、101kPa下,22.4L甲烷充分燃烧后,所得气体产物的分子总数为NA
D.1L0.1molL1氢氧化钠溶液中含有的H-O键的数目为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
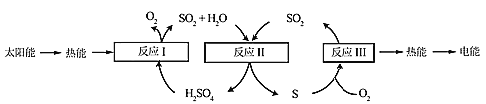
(1)反应Ⅰ:2H2SO4(l)=2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1
反应Ⅲ:S(s)+O2(g)=SO2(g) ΔH3=-297 kJ·mol-1
反应Ⅱ的热化学方程式:________________。
(2)对反应Ⅱ,在某一投料比时,两种压强下,H2SO4在平衡体系中物质的量分数随温度的变化关系如图所示:
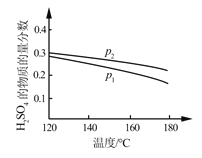
p2_______p 1(填“>”或“<”)。
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。将ii补充完整。
i.SO2+4I-+4H+=S↓+2I2+2H2O
ii.I2+2H2O+_________=_________+_______+2 I-
(4)探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到 2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号 | A | B | C | D |
试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
①B是A的对比实验,则a=__________。
②比较A、B、C,可得出的结论是______________________。
③实验表明,SO2的歧化反应速率D>A,结合i、ii反应速率解释原因:________________。
(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图所示。则b电极上的电极反应式为__________________。
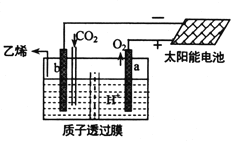
查看答案和解析>>
科目: 来源: 题型:
【题目】下表列出了①~⑩十种元素在周期表中的位置。
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ④ | ⑩ | |||||
3 | ⑤ | ⑥ | ⑦ | ③ | ⑧ | ⑨ | ||
回答下列问题:
(1)①、④按原子个数比1:1 组成的分子的电子式为____________________ ;由②、④两种元素组成的一种无毒化合物的结构式为 _____________________。
(2)这10种元素中,化学性质最不活泼的元素是_____________(填元素符号,下同),得电子能力最强的原子是__________________,失电子能力最强的单质与水反应的化学方程式是_________________________。
(3)用化学方程式表示②和⑨两种元素的非金属性强弱:________________________ 。
(4)元素③的气态氢化物和元素⑧的气态氢化物中,易于制备的是 ____________________(填化学式)
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应,其离子方程式为 ______________________________。
(6)元素 ①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式:___________________ ;写出一种离子化合物的化学式:______________________。
(7)写出⑥的单质置换出②的单质的化学方程式:________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的1/10。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式。
正极:_____________________;负极:____________________。
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用下图所示甲的方案,其中焊接在铁闸门的固体材料R可以采用_______________。
A.铜 B.钠 C.锌 D.石墨
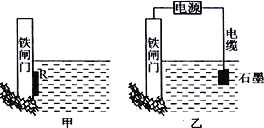
(3)上图中乙方案也可降低铁闸门腐蚀速率,其中铁闸门应该连接在直流电源的_____________极。
(4)除了以上金属防护的方法外,请再例举两种办法:___________;___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组探究醋酸的溶液情况,进行了如下实验。
(1)取一定量的冰醋酸配制250 mL 0.5000 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、___________和___________。
(2)该学习小组用pH试纸对上述0.5000 mol·L-1醋酸溶液进行了pH测定,请用文字描述pH试纸的使用方法______。
(3)用上述0.5000 mol·L-1的醋酸溶液再进行稀释,为测定稀释后醋酸溶液的准确浓度,用0.2000 mol·L-1的NaOH溶液对25.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 25.05 | 25.00 | 23.80 | 24.95 |
则该醋酸溶液的浓度为________________。
(4)实验(2)中,滴定过程中pH变化曲线如图所示(室温条件下)。

①滴定过程中,当滴加12.50mLNaOH时,所得混合溶液中离子浓度由大到小顺序为____________。
②当滴加25.00mLNaOH时,反应后测得混合溶液的pH=9。则混合溶液中:水的电离度是纯水的_____倍;
(5)在滴定过程中,下列操作会造成结果偏高的是________。
A.滴定终点时,滴定管尖嘴处有半滴悬而未落
B.读取NaOH溶液体积时,开始仰视读数,滴定结束后俯视读数
C.滴定过程中向锥形瓶中加水
D.滴定管水洗后未用标准液润洗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com