
科目: 来源: 题型:
【题目】冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一。
(1)使用甲醇汽油可以减少汽车尾气对环境的污染。工业上在200℃和10MPa的条件下可用甲烷和氧气通过铜制管道反应制得甲醇,已知一定条件下,CH4和CH3OH的燃烧热分别784kJ/mol和628kJ/mol ,则CH4(g) +![]() O2(g) = CH3OH(g) △H=___。
O2(g) = CH3OH(g) △H=___。
(2)二甲醚也是清洁能源。用合成气在催化剂存在下制备二甲醚的反应原理为:2CO(g) + 4H2(g) ![]() CH3OCH3(g) + H2O(g) △H<0。
CH3OCH3(g) + H2O(g) △H<0。
①.某温度下,将2.0molCO(g)和6.0molH2(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中 CH3OCH3(g) 的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的是___。
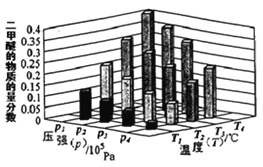
A. P1>P3, T1>T3 B. P3>P2,T3>T2 C.P2>P4,T4>T2 D.P1>P4,T2>T3
②在恒容密闭容器里按体积比为1:3充入一氧化碳和氢 气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是___
A.氢气的转化率减小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.某反应物的体积百分含量增大
(3)在一容积可变的密闭容器中充有10 mol CO和20 mol H2, 发生反应CO(g)+2H2(g) ![]() CH3OH(g),CO的平衡转化率[与温度(T)、压强(p)的关系如图所示。
CH3OH(g),CO的平衡转化率[与温度(T)、压强(p)的关系如图所示。

①A、B、C三点对应的平衡常数KA、KB、KC的大小关系为______。
②若达到平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积为________L。
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年诺贝尔化学奖授予约翰·古迪纳夫、斯坦利·威廷汉和吉野彰,表彰他们对锂离子电池研究的贡献。磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片(除LiFePO4外,还含有Al箔、少量不溶于酸碱的导电剂)中的资源,部分流程如图:
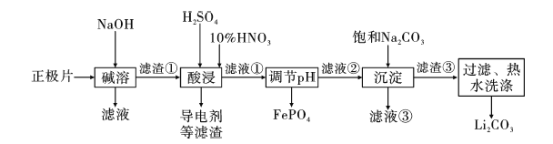
已知:KSP ( Li2CO3)=2.0×10-3 。部分物质的溶解度(S)如下表所示:
T℃ | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g |
20 | 1.33 | 34.2 | 0.039 |
80 | 0.85 | 30.5 | —— |
100 | 0.72 | —— |
(1) 流程中用“热水洗涤”的原因是____________。
(2)写出碱溶时Al箔溶解的化学方程式 ___________。
(3)酸浸时,用H2O2代替HNO3更好,其优点是________。
(4)磷酸亚铁锂电池在工作时,正极发生LiFePO4和FePO4的转化,该电池放电时正极的电极反应式为____。
(5)若滤液②中c(Li+)=4mol/L,加入等体积的Na2CO3溶液后,Li+的沉降率达到90%,计算滤液③中c(CO32-)=____mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】五倍子是一种常见的中草药,其有效成分为X。一定条件下X可分别转化为Y、Z,如下所示。
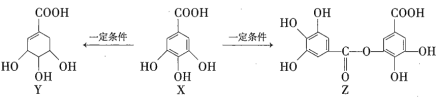
下列说法错误的是( )
A.![]() 最多能与
最多能与![]() 发生取代反应
发生取代反应
B.等物质的量的Z分别与Na和![]() 恰好反应时,消耗Na和
恰好反应时,消耗Na和![]() 的物质的量之比为6∶1
的物质的量之比为6∶1
C.一定条件下,Y能发生加成反应、取代反应、消去反应和氧化反应
D.![]() 最多能与
最多能与![]() 发生反应
发生反应
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,几种物质的电离平衡常数如表:下列说法正确的是( )
HCOOH | CH3COOH | NH3·H2O | |
Ka | 1.77×10-4 | 1.75×10-5 | 1.76×10-5 |
A.浓度相同的HCOOH溶液与NH3·H2O溶液等体积混合,所得溶液显碱性
B.用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液,HCOOH消耗NaOH溶液的体积大
C.0.2mol·L-1HCOOH与0.1mol·L-1NaOH等体积混合后的溶液中:c(HCOO-)+c(OH-)=c(HCOOH)+c(H+)
D.0.2mol·L-1CH3COONa与0.1mol·L-1盐酸等体积混合后的溶液中(pH<7):c(CH3COO-)>cCl-)>c(CH3COOH)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H>0
B.硅单质可用作光导纤维的原料
C.CH3COOH溶液加水稀释后,溶液中![]() 的值减小
的值减小
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液pH减小
查看答案和解析>>
科目: 来源: 题型:
【题目】请写出下列物质的电子式:
(1)H2S________; (2)CO2________; (3)N2________;
(4)OH-________; (5)HClO________;(5)Na2O2________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一恒容的密闭容器中充入0.1 mol·L-1 CO2、0.1 mol·L-1CH4,在一定条件下发生反应:CH4(g)+CO2(g) ![]() 2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图。下列有关说法不正确的是( )
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图。下列有关说法不正确的是( )
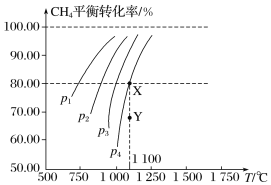
A.压强为p4时,在Y点:v正<v逆B.上述反应的ΔH>0
C.压强:p4>p3>p2>p1D.1 100 ℃时该反应平衡常数约为1.64
查看答案和解析>>
科目: 来源: 题型:
【题目】在2 L和密闭容器中放入4mol N2O5,发生如下反应:2N2O5(g)![]() 4NO2(g)+O2(g),反应进行到5min时,测得N2O5转化了20%,求:
4NO2(g)+O2(g),反应进行到5min时,测得N2O5转化了20%,求:
(1)5min时,剩余N2O5的物质的量________;
(2)前5min,v(NO2)为多少__________;
(3)5min时,O2的物质的量占混合气体总物质的量的百分比_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】通常人们把拆开(或生成)1 mol 某化学键所吸收(或放出)的能量看成该化学键的键能。化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
化学键 | A—A | B—B | A—B |
生成1mol化学键时放出的能量 | 436kJ/mol | 243kJ/mol | 431kJ/mol |
则下列热化学方程式不正确的是
A.![]() A2(g)+
A2(g)+![]() B2(g)=AB(g) ΔH=-91.5kJ/mol
B2(g)=AB(g) ΔH=-91.5kJ/mol
B.A2(g)+B2(g)=2AB(g) ΔH=-183kJ/mol
C.![]() A2(g)+
A2(g)+![]() B2(g)=AB(g) ΔH=+91.5kJ/mol
B2(g)=AB(g) ΔH=+91.5kJ/mol
D.2AB(g)=A2(g)+B2(g) ΔH=+183kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应的热化学方程式是( )
2NH3的能量变化如图所示,该反应的热化学方程式是( )
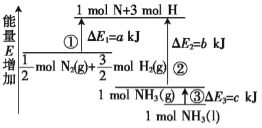
A.N2(g)+3H2(g)![]() 2NH3(l) △H=2(a-b-c)kJ/mol
2NH3(l) △H=2(a-b-c)kJ/mol
B.N2(g)+3H2(g)![]() 2NH3(g) △H=2(b-a)kJ/mol
2NH3(g) △H=2(b-a)kJ/mol
C.N2(g)+H2(g)![]() NH3(l) △H=(b+c-a)kJ/mol
NH3(l) △H=(b+c-a)kJ/mol
D.N2(g)+H2(g)![]() NH3(g) △H=(a+b)kJ/mol
NH3(g) △H=(a+b)kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com