
科目: 来源: 题型:
【题目】一定条件下存在反应:2SO2(g)+ O2(g)![]() 2SO3(g) △H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,并在400℃条件下开始反应,达到平衡时,下列说法正确的是( )
2SO3(g) △H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,并在400℃条件下开始反应,达到平衡时,下列说法正确的是( )

A.容器I、Ⅲ中平衡常数相同
B.容器II、Ⅲ中正反应速率始终相同
C.容器Ⅱ、Ⅲ中的反应达平衡时,SO3的转化率:II>III
D.容器I中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1
查看答案和解析>>
科目: 来源: 题型:
【题目】日前新合成的砷化镉三维材料具有超强导电性,这种材料的电气性能与石墨烯相当,可代替石墨烯使用。
(1)Cd与Zn同族且相邻,若Cd基态原子将次外层1个d电子激发进入最外层的np能级,则该激发态原子的外围电子排布式为___。
(2)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3强于PH3,分析其原因是___。
(3)As、Ge、Se的第一电离能由大到小的顺序为___(用元素符号表示)。
(4)含砷有机物“对氨基苯胂酸”的结构简式如图,其中C原子轨道杂化类型为___,1mol对氨基苯胂酸含σ键数目为___。
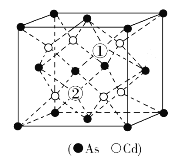
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构如图,As为面心立方堆积,Cd占据As围成的四面体空隙,空隙占有率75%,如图“①”和“②”位是“空位”。则砷化镉化学式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯气相直接水合反应制备乙醇:C2H4(g)+H2O(g) ![]() C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如下(起始时,n(H2O)=n(C2H4)=1 mol,容器体积为1 L)。
C2H5OH(g)。乙烯的平衡转化率随温度、压强的变化关系如下(起始时,n(H2O)=n(C2H4)=1 mol,容器体积为1 L)。

下列分析不正确的是
A. 乙烯气相直接水合反应的H<0
B. 图中压强的大小关系为:p1>p2>p3
C. 图中a点对应的平衡常数K =![]()
D. 达到平衡状态a、b所需要的时间:a>b
查看答案和解析>>
科目: 来源: 题型:
【题目】钛酸钙(CaTiO3)材料制备原理之一是CaCO3+TiO2![]() CaTiO3+CO2↑。下列有关判断不正确的是( )
CaTiO3+CO2↑。下列有关判断不正确的是( )
A.TiO2是金属氧化物,所以不是酸性氧化物
B.CaCO3、CaTiO3均属于含氧酸盐
C.CaCO3难溶于水,属于强电解质
D.上述反应不是氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:①A的产量通常用来衡量一个国家的石油化工水平;
②![]() 。
。
现以A为主要原料合成化合物E,其合成路线如图所示。回答下列问题:
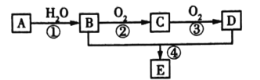
(1)写出下列物质的官能团名称:B_____;C______。
(2)反应④的化学方程式为_____________,反应类型是__________。
(3)某学习小组设计B的催化氧化的实验装置如图所示,试回答下列问题。
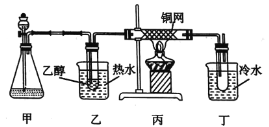
①甲的锥形瓶中盛放的固体药品可能为_______(填字母)。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
②实验过程中,丙装置硬质玻璃管中发生反应的化学方程式为_____________。
③物质B的催化氧化产物与葡萄糖具有相同的特征反应,将所得的氧化产物与新制氢氧化铜悬浊液混合后加热,现象为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用合成气制备甲醇。反应为![]() 某温度下,在容积为2L的密闭容器中进行该反应,其相关数据如图:
某温度下,在容积为2L的密闭容器中进行该反应,其相关数据如图:
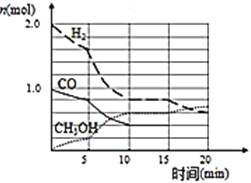
(1)从反应开始至平衡时,用CO表示化学反应速率为 ______ ,该温度下的平衡常数为 ______
(2)![]() 至10min时速率变化的原因可能是 ______ ;
至10min时速率变化的原因可能是 ______ ;
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图所示(夹持仪器、酒精灯等已略去)。

取17.1gA放入装置中,通入过量![]() 燃烧,生成
燃烧,生成![]() 和
和![]() ,请回答下列有关问题:
,请回答下列有关问题:
(1)通入过量![]() 的目的是__________。
的目的是__________。
(2)C装置的作用是_______;D装置的作用是________。
(3)通过该实验,能否确定A中是否含有氧原子_______(填“能”或“不能”)。
(4)若A的摩尔质量为![]() ,C装置增重9.99g,D装置增重26.4g,则A的分子式为______。
,C装置增重9.99g,D装置增重26.4g,则A的分子式为______。
(6)A可发生水解反应,![]() A可水解生成2种互为同分异构体的产物,且这两种产物均为
A可水解生成2种互为同分异构体的产物,且这两种产物均为![]() ,则A在催化剂作用下水解的化学方程式为____________。
,则A在催化剂作用下水解的化学方程式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年诺贝尔化学奖授予了锂离子电池开发的三位科学家。一种锂离子电池的结构如图所示,电池反应式为 LixC6 + Li1-xCoO2![]() C6 + LiCoO2(x<1)。下列说法正确的是
C6 + LiCoO2(x<1)。下列说法正确的是
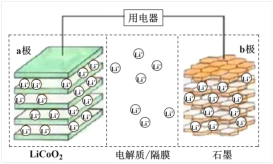
A.充电时 a 极接外电源的负极
B.放电时Li+在电解质中由a极向b极迁移
C.充电时若转移0.02 mol电子,石墨电极将减重0.14 g
D.该废旧电池进行“放电处理”有利于锂在LiCoO2极回收
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列几种有机物:①![]() ②
②![]() ③
③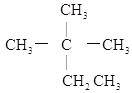 ④癸烷⑤
④癸烷⑤![]() ⑥
⑥![]() ⑦
⑦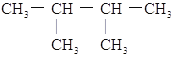 ⑧丙烷。请根据上述物质按要求回答下列问题。
⑧丙烷。请根据上述物质按要求回答下列问题。
(1)相对分子质量为44的烷烃的结构简式为________(填化学式)。
(2)与③互为同分异构体的是_______(填序号)。
(3)有机物②在加热条件下和![]() 反应的化学方程式为________。
反应的化学方程式为________。
(4)在120℃、![]() 条件下,某种气态烃与足量的
条件下,某种气态烃与足量的![]() ,完全反应后,测得反应前后气体的体积没有发生改变,则该烃是_______(填序号)。
,完全反应后,测得反应前后气体的体积没有发生改变,则该烃是_______(填序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫化氢俗称“臭蛋气”,是一种无色具有臭鸡蛋气味的剧毒气体,由含硫物质分解而来,属于常见的酸性有害气体中的一种。研究硫化氢的利用及污染的防治很有意义。
(1)已知下列反应的热化学方程式:
①2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ΔH1=-1123.6kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH2=-296kJ·mol-1
③2H2(g)+O2(g)=2H2O(l) ΔH3=-571.6kJ·mol-1
写出H2S分解为单质硫(用S表示)和H2的热化学方程式:___。
(2)H2S在一定条件下发生如下形式的分解:2H2S(g)![]() S2(g)+2H2(g),利用该反应可制备H2和硫磺。在2.0L的恒容密闭容器中充入0.1molH2S发生上述反应,不同温度下测得H2S的转化率与时间的关系如图所示。
S2(g)+2H2(g),利用该反应可制备H2和硫磺。在2.0L的恒容密闭容器中充入0.1molH2S发生上述反应,不同温度下测得H2S的转化率与时间的关系如图所示。
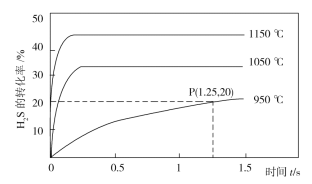
①温度升高时,混合气体的平均摩尔质量减小的原因是___。
②P点时容器内气体压强与起始时气体压强之比为___。
③1050℃时,此反应的平衡常数___(填序号)。
a.等于3.125×10-4 b.大于3.125×10-4
c.小于3.125×10-4 d.无法判断
(3)科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构示意图如图所示:
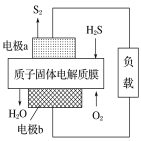
①电极a上发生反应的电极反应式为___。
②当有1molH+经质子膜进入正极区时,反应消耗H2S的体积为___L(标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com