
科目: 来源: 题型:
【题目】为达到下列实验目的,对应的实验方法以及相关解释均正确的是( )
选项 | 实验目的 | 实验方法 | 相关解释 |
A | 测量氯水的pH |
| pH试纸遇酸变红 |
B | 探究正戊烷(C5H12) 催化裂解 |
| C5H12裂解为分子较小的烷烃和烯烃 |
C | 实验温度对平衡移动的影响 |
| 2NO2(g) |
D | 用AlCl3溶液制备AlCl3晶体 |
| AlCl3沸点高于溶剂水 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示。以下有关该物质的说法中不正确的是( )
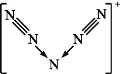
A. 每个N5+中含有35个质子和34个电子
B. 该离子中有非极性键和配位键
C. 该离子中含有4个π键
D. 与PCl4+互为等电子体
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列给定条件的溶液中,一定能大量共存的离子组是( )
A.无色溶液:Ca2+、H+、Cl-、HSO3-
B.能使pH试纸呈红色的溶液:Na+、NO3-、I-、AlO2-
C.FeCl3溶液:K+、Na+、Fe2+、S2-
D.![]() =0.1 molL-1的溶液:Na+、K+、SiO32-、NO3-
=0.1 molL-1的溶液:Na+、K+、SiO32-、NO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA
B.反应 5NH4NO3![]() 2HNO3+4N2↑ +9H2O 中,生成 28 g N2 时,转移的电子数目为3.75 NA
2HNO3+4N2↑ +9H2O 中,生成 28 g N2 时,转移的电子数目为3.75 NA
C.0.1 mo1·L-1 MgCl2溶液中含Cl-数为0.2NA
D.3.9 g Na2O2 晶体中含有的离子总数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】在2 L密闭容器中发生反应4A(s)+3B(g)=2C(g)+D(g),经2 min,B的物质的量减少0.6 mol,下列对该反应速率表示正确的是
A.用B表示的反应速率:v (B)=0.3 mol·L-1·min-1
B.分别用B、C表示的反应速率其比值为2∶3
C.用D表示的平均反应速率为:v (D)= 0.05 mol·L-1·min-1
D.用A表示的反应速率为:v (A)=0.4 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.2 molNO2与水充分反应,转移电子数为NA
B.含0.1molH3PO4的水溶液中PO43-的数目为0.1NA
C.0.5molNa2O2中O-的数目为NA
D.标况下,42g丙烯和丁烯混合物含C数目为3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知H2(g)+![]() O2(g)=H2O(g),如图是1molH2燃烧的反应过程中能量变化示意图。
O2(g)=H2O(g),如图是1molH2燃烧的反应过程中能量变化示意图。
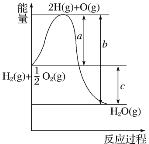
请回答下列问题:
(1)该反应是__(填“吸热”或“放热”)反应。
(2)氢气在氧气中燃烧,破坏1molH—H键吸收Q1kJ的能量,破坏1molO=O键吸收Q2kJ的能量,形成1molH—O键释放Q3kJ的能量,则下列关系式正确的是___。
A.2Q1+Q2>4Q3 B.2Q1+Q2<4Q3
C.Q1+Q2<Q3 D.2Q1+Q2=4Q3
(3)已知1gH2(g)完全燃烧生成水蒸气时放出热量121kJ,且O2(g)中1molO=O键完全断裂时吸收热量496kJ,H2O(g)中1molH—O键形成时放出热量463kJ,则H2(g)中1molH—H键断裂时吸收热量为__kJ。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是
A.0.1 mol·L-1FeCl3溶液:Mg2+、Al3+、MnO4-、SCN-
B.能使紫色石蕊试液变蓝的溶液:Ca2+、Na+、ClO-、I-
C.0.1 mol·L-1 NH4HCO3溶液:Ba2+、K+、OH-、NO3—
D.![]() =10-12的溶液:NH4+、Na+、SO42-、Cl-
=10-12的溶液:NH4+、Na+、SO42-、Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组用如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯),反应原理: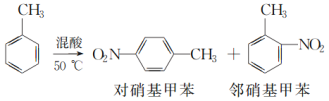
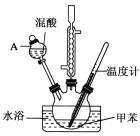
实验步骤:①浓硝酸与浓硫酸按体积比1:3配制混合溶液(即混酸)共40mL;
②在三颈烧瓶中加入13g甲苯(易挥发),按图所示装好药品和其他仪器;
③向三颈烧瓶中加入混酸;
④控制温度约为50~55℃,反应大约10min,三颈烧瓶底部有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到对硝基甲苯和邻硝基甲苯共15g。
相关物质的性质如下:
有机物 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 |
甲苯 | 0.866 | 110.6 | 不溶于水 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
(1)A的仪器名称是___。
(2)水浴加热的优点是__。
(3)配制混酸的方法是__。
(4)若实验后在三颈烧瓶中收集的产物较少,可能的原因是__。
(5)分离反应后产物的方案如下:
混合液![]()
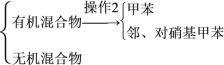
操作1的名称是__,操作2中不需要用到下列仪器中的__(填序号)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(6)本实验中邻、对硝基甲苯的产率为__(结果保留至小数点后一位数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com