
科目: 来源: 题型:
【题目】下表提供的试剂,用如图所示装置,能制备相应气体的是
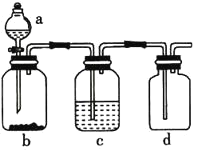
选项 | a中试剂 | b中试剂 | c中试剂 | 实验目的 |
A. | 浓盐酸 | 二氧化锰 | 饱和食盐水 | 制备并收集氯气 |
B. | 稀盐酸 | 石灰石 | 浓硫酸 | 制备并收集二氧化碳 |
C. | 稀硫酸 | 粗锌 | 浓硫酸 | 制备并收集氢气 |
D. | 稀硝酸 | 铜粉 | 浓硫酸 | 制备并收集一氧化氮 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)有一种燃料电池,所用燃料为H2和空气,电解质为熔融的K2CO3。回答下列问题
①CO![]() 移向____________极。
移向____________极。
②正极反应式为____________________。
③电池中CO![]() 的物质的量将逐渐________________(填增大、减少、不变)。
的物质的量将逐渐________________(填增大、减少、不变)。
(2)用上面的电池对下物质进行电解,其中a、b、c、d、e、f电极均为惰性电极,通电后,a极产生的气体明显多于b极,2分钟后,测得乙池的pH为12,则
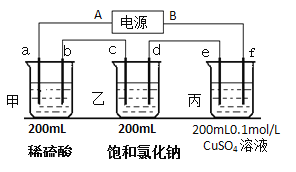
①电源A极是______________极。
②c极上的电极反应式:___________________。
③甲、乙两池共可收集到________mol气体。
④丙装置上某极可析出固体________克,溶液的pH为________________。(常温,不考虑溶液体积变化)
⑤电解n分钟后,硫酸铜正好消耗完,再将e、f电极反接电源,用同样的电流再电解n分钟,则丙溶液中的硫酸铜的物质的量浓度为______________mol/L。(不考虑溶液体积变化)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,可逆反应2X(g)+Y(s)![]() 2Z(g)△H=-akJ·mol-1,下列说法一定正确的是( )
2Z(g)△H=-akJ·mol-1,下列说法一定正确的是( )
A. 当反应消耗1molY时,反应放出akJ的热量
B. 当反应达到平衡时,X、Y、Z 三者的物质量之比为2∶1∶2
C. 当反应达到平衡时,压缩体积,X的正、逆反应速率都增大,平衡向正反应方向移动
D. 恒温恒容,反应达到平衡后,加入1molY平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】雾霾天气的“罪魁祸首”是空气中的CO、NO、NO2等污染气体在大气中反应产生PM2.5 颗粒物,研究NO、NO2、CO 等污染物的处理,对环境保护有重要的意义。
(1)已知:
NO2(g)+CO(g) = CO2 (g)+NO(g) △H =-230.0kJ·mol-1
N2 (g)+O2 (g) = 2NO(g) △H =-180.0 kJ·mol-1
2NO(g)+O2 (g) = 2NO2 (g) △H =-112.3kJ·mol-1
若NO2气体和CO 气体反应生成无污染气体,其热化学方程式为_____。
(2) 由CO生成CO2的化学方程式为CO+O2![]() CO2+O。其正反应速率为v正=K正·c(CO) ·c(O2),逆反应速率为v逆=K逆·c(CO2) ·c(O),K正、K逆为速率常数。已知某一温度时,该反应的平衡常数K=0.40,K正=1.24×105 L·s-1·mol-1,此时K逆=_____L·s-1·mol-1。
CO2+O。其正反应速率为v正=K正·c(CO) ·c(O2),逆反应速率为v逆=K逆·c(CO2) ·c(O),K正、K逆为速率常数。已知某一温度时,该反应的平衡常数K=0.40,K正=1.24×105 L·s-1·mol-1,此时K逆=_____L·s-1·mol-1。
(3)汽车的排气管上安装“催化转化器”,其反应的热化学方程式为:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) △H<0。T℃时,将等物质的量的NO 和CO 充入容积为2L 的密闭容器中,若温度和体积不变,反应过程中(0~15min) NO 的物质的量随时间变化如图。
2CO2(g)+N2(g) △H<0。T℃时,将等物质的量的NO 和CO 充入容积为2L 的密闭容器中,若温度和体积不变,反应过程中(0~15min) NO 的物质的量随时间变化如图。
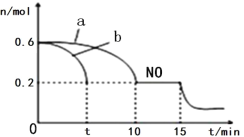
①图中a、b 分别表示在相同温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n (NO)的变化曲线,其中表示催化剂表面积较大的曲线是________(填“a”或“b”) 。
②T℃时,该反应的化学平衡常数K=____;(保留小数点后一位小数)平衡时若保持温度不变,再向容器中充入CO、CO2各0.2 mol,则平衡将_____移动。(填“向左”、“向右”或“不”)
③15min 时,若改变外界反应条件,导致n (NO)发生图中所示变化,则改变的条件可能是_________(任答一条即可)。
(4)NO2可用氨水吸收生成NH4NO3。25℃时,将x mol NH4NO3溶于水,溶液显酸性,原因是_________用离子方程式表示)。向该溶液滴加c L 氨水后溶液呈中性,则所滴加氨水的浓度为_____molL﹣1。(NH3H2O 的电离平衡常数K =2×10﹣5 molL﹣1)
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科研人员提出了以Ni / Al2O3 为催化剂,由CO2和H2转化为产品CH4的反应历程,其示意图如下:

下列说法不正确的是
A. 总反应方程式为:CO2+4H2![]() CH4+2H2O
CH4+2H2O
B. 催化剂可有效提高反应物的平衡转化率
C. 在反应历程中,H―H键与C=O键断裂吸收能量
D. 反应过程中,催化剂参与反应,改变反应路径,降低反应的活化能
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下在密闭容器中发生如下可逆反应:2M(g)+N(g)![]() 2E(g),若开始时只充入2mol E(g),达平衡时,E的转化率为40%;若开始时充入2mol M和1mol N的混合气体,达平衡时混合气体的压强比起始时减少了( )
2E(g),若开始时只充入2mol E(g),达平衡时,E的转化率为40%;若开始时充入2mol M和1mol N的混合气体,达平衡时混合气体的压强比起始时减少了( )
A.20%B.40%C.60%D.80%
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:H2的标准燃烧热为-286 kJ · mol-1,CO的标准燃烧热为-283 kJ · mol-1,液态甲醇(CH3OH)标准燃烧热为-726 kJ · mol-1。由H2(g)与CO2(g)合成CH3OH(l)的ΔH为:
A. +297 kJ · mol-1 B. +151 kJ · mol-1
C. -132 kJ · mol-1 D. -1548 kJ · mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向两只分别盛有50 mL0.100 mol/L盐酸的烧杯中各自匀速滴加50 mL蒸馏水、50 mL0.100 mol/L醋酸铵溶液,装置如图所示(夹持仪器等已略)。
已知:常温下,CH3COONH4溶液pH约为7。
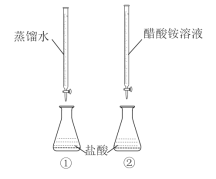
下列说法正确的是( )
A.实验①滴加过程中溶液所有离子浓度都减小
B.实验②滴至pH=2时,溶液中c(Cl-)+c(CH3COO-)+c(OH-)=0.01 mol/L
C.实验②滴加过程中,溶液中均存在c(CH3COO-)<c(NH4+)
D.滴定结束后,①中水的电离程度比②中大
查看答案和解析>>
科目: 来源: 题型:
【题目】中山大学中山医学院颜光美教授课题组发现一种叫![]() 的天然病毒(属于蛋白质),其能杀死癌细胞而不伤害正常细胞,该病毒含有C、H、O、N、S等元素,其直径大约为
的天然病毒(属于蛋白质),其能杀死癌细胞而不伤害正常细胞,该病毒含有C、H、O、N、S等元素,其直径大约为![]() 。下列说法不正确的是( )。
。下列说法不正确的是( )。
A.![]() 病毒中的C、H、O、N、S原子最有可能以共价键结合
病毒中的C、H、O、N、S原子最有可能以共价键结合
B.![]() 病毒不属于高分子化合物
病毒不属于高分子化合物
C.![]() 病毒溶于水形成的液体具有丁达尔效应
病毒溶于水形成的液体具有丁达尔效应
D.![]() 病毒在生物体内的水解产物可能是氨基酸
病毒在生物体内的水解产物可能是氨基酸
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒容密闭容器中,用铜铬的氧化物作催化剂,用一定量的HCl(g)和O2制取Cl2的原理为:4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
2Cl2(g)+2H2O(g) ΔH<0。下列有关说法不正确的是
A. 平衡前,随着反应的进行,容器内压强变小
B. 平衡时,其他条件不变,分离出H2O(g),逆反应速率减小
C. 平衡时,其他条件不变,升高温度平衡常数增大
D. 其他条件不变,使用不同催化剂,HCl(g)的转化率不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com