
科目: 来源: 题型:
【题目】如图所示,甲、乙两池中的电极材料都是铁棒与碳棒,请回答下列问题。
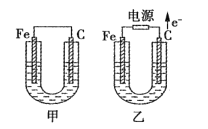
(1)若两池中的电解质溶液均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的__棒,乙池中的__棒。
②乙池中阳极的电极反应式是__。
(2)若两池中的电解质溶液均为饱和NaCl溶液:
①乙池中总反应的离子方程式为__。
②乙池中碳棒上的电极反应属于__(填“氧化反应”或“还原反应”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.浓硫酸与铁加热反应后,铁片有剩余,生成的气体除水蒸气外为![]()
B.用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值
C.工业上电解熔融氯化铝可得到金属铝
D.使用滴定管时水洗后需润洗,但容量瓶水洗后不用润洗
查看答案和解析>>
科目: 来源: 题型:
【题目】下列现象或事实可用同一原理解释的是
A.浓硫酸和浓盐酸长期暴露在空气中浓度降低
B.亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质
C.漂白粉、活性炭、![]() 都能使红墨水褪色
都能使红墨水褪色
D.![]() 和
和![]() 溶液使酸性高锰酸钾的紫色褪去
溶液使酸性高锰酸钾的紫色褪去
查看答案和解析>>
科目: 来源: 题型:
【题目】钼![]() 是一种难熔稀有金属,我国的钼居世界第二。钼及其合金在冶金,农业、电器、化工、环保等方面有着广泛的应用。
是一种难熔稀有金属,我国的钼居世界第二。钼及其合金在冶金,农业、电器、化工、环保等方面有着广泛的应用。
(1)已知:![]()
![]()
![]() ,则
,则![]() ______
______![]() 用含
用含![]() 、
、![]() 的代数式表示
的代数式表示![]()
(2)密闭容器中用![]() 作固硫剂,同时用一定量的氢气还原辉钼矿
作固硫剂,同时用一定量的氢气还原辉钼矿![]() 的原理是:
的原理是:![]() ,实验测得平衡时的有关变化曲线如图所示:
,实验测得平衡时的有关变化曲线如图所示:
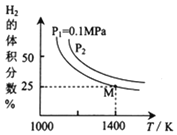
![]() 由图可知,该反应的
由图可知,该反应的![]() ______0
______0![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() ,
,![]() ______
______![]() MPa
MPa![]() 填“
填“![]() ”或“
”或“![]() ”
”![]() 。
。
![]() 如果上述反应在体积不变的密闭容器中达平衡,下列说法错误的是______
如果上述反应在体积不变的密闭容器中达平衡,下列说法错误的是______![]() 选填编号
选填编号![]() 。
。
A.![]()
![]() 容器内气体的密度不变时,一定达平衡状态
容器内气体的密度不变时,一定达平衡状态
C.再加入![]() ,则
,则![]() 转化率增大
转化率增大![]() 容器内压强不变时,一定达平衡状态
容器内压强不变时,一定达平衡状态
(3)电氧化法提纯钼的原理:将辉钼矿![]() 放入装有食盐水的电解槽中,用惰性电极电解,
放入装有食盐水的电解槽中,用惰性电极电解,![]() 被氧化为
被氧化为![]() 和
和![]() 阴极的电极反应式为______。
阴极的电极反应式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
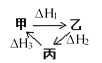
A.甲、乙、丙三物质转化如图所示,则![]()
B.1molCO完全燃烧生成稳定氧化物放出热量为![]() ,则2
,则2 ![]()
![]() ,
,![]()
C.若![]() ,
,![]() ,故在某容器中充入
,故在某容器中充入![]() 与
与![]() 充分反应后,放出的热量为
充分反应后,放出的热量为![]()
D.常温下,稀HCl和稀NaOH溶液反应生成![]() 放出热量为
放出热量为![]() ,其热化学方程式为
,其热化学方程式为![]() ,
,![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是__________________。(用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol·L-1 NH4Al(SO4)2中c(NH4+)________(填“等于”“大于”或“小于”)0.1 mol·L-1 NH4HSO4中c(NH4+)。
(3)0.1 mol·L-1电解质溶液的pH随温度变化的图像如图所示:
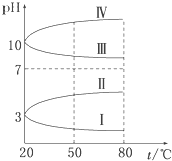
①其中符合0.1 mol·L-1 NH4Al(SO4)2的pH随温度变化的曲线是________(填写序号),导致pH随温度变化的原因是__________________;
②20℃时,0.1mol·L-1NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=________(填数值)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(9分)某化学兴趣小组对生石灰与水反应是显著放热反应进行了实验探究,在除了用手触摸试管壁感觉发热外,还设计了下列几个可行性方案。
甲方案:将温度计与盛放有生石灰的小试管用橡皮筋捆绑在一起,放入有水的小烧杯中,用胶头滴管向小试管中缓缓滴入水,看到的现象是 ,说明反应放热。(下列装置中支撑及捆绑等仪器已略去)

乙方案:将盛放有生石灰的小试管插入带支管的试管中,支管接①或②,用胶头滴管向小试管中缓缓滴入水,看到的现象是(接①) ,(接②) ,说明反应放热。
丙方案:用胶头滴管向盛放有生石灰且带支管的试管中滴加水,支管接的导管中盛适量无水硫酸铜粉末,看到的现象是 ,说明反应放热,其原因是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G是前四周期元素,原子序数依次增大,根据表中提供的有关信息,回答问题:
元素 | 相关信息 |
A | 所有单质中密度最小 |
B | 形成化合物种类最多的元素 |
D | 基态原子中只有3个能级,有2个未成对电子 |
E | 短周期中原子半径最大 |
F | 第三周期中电负性最大的元素 |
G | 最外层只有一个电子,内层填满电子 |
(1)E元素在周期表中的位置是______,F元素原子最外层电子排布式为______,BD2的立体构型为______。
(2)由D、E、F三种元素形成的一种常见物质的水溶液显碱性,用离子方程式表示其显碱性的原因:______。
(3)氢化物稳定性:B______D;最高价氧化物对应的水化物酸性:C______F。(填“<”或“>”)
(4)每个B2A4分子中含有______个σ键,______个π键。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原滴定实验与中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.001 mol·L-1KMnO4酸性溶液滴定未知浓度的无色NaHSO3溶液。反应的离子方程式是2MnO![]() +5HSO
+5HSO![]() +H+=2Mn2++5SO42-+3H2O
+H+=2Mn2++5SO42-+3H2O
填空完成问题:
(1)该滴定实验所需仪器有下列中的____________。
A酸式滴定管(50 mL) B碱式滴定管(50 mL) C量筒(10 mL) D锥形瓶 E铁架台
F滴定管夹 G烧杯 H白纸 I胶头滴管 J漏斗
(2)不能用________(填“酸”或“碱”)式滴定管盛放高锰酸钾溶液。试分析原因________________。
(3)选何种指示剂,说明理由____________________________。
(4)滴定前平视KMnO4溶液液面,刻度为a mL,滴定后俯视液面刻度为b mL,则(b-a)mL比实际消耗KMnO4溶液体积________(填“多”或“少”)。根据(b-a)mL计算得到的待测浓度,比实际浓度________(填“大”或“小”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com