
科目: 来源: 题型:
【题目】中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是

A. C3N4中C的化合价为 -4
B. 反应的两个阶段均为吸热过程
C. 阶段Ⅱ中,H2O2既是氧化剂,又是还原剂
D. 通过该反应,实现了化学能向太阳能的转化
查看答案和解析>>
科目: 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
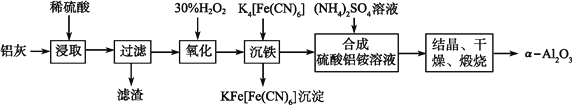
(1)写出铝灰与硫酸反应涉及的离子方程式_____________。
(2)图中“滤渣”的主要成分为________(填化学式)。
(3)加30%H2O2溶液发生的离子反应方程式为_________________________________。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]![]() 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
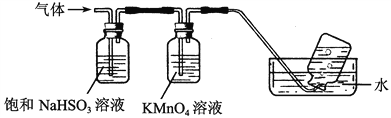
①集气瓶中收集到的气体是________(填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有________(填化学式)。
③KMnO4溶液褪色(MnO被还原为Mn2+),发生的离子反应方程式为___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】向仅含Fe2+、I-、Br-的溶液中通入适量氯气,溶液中这三种离子的物质的量随消耗氯气物质的量的变化如下图所示。下列说法中正确的是( )
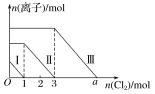
A.线段Ⅲ代表Fe2+的变化情况
B.线段Ⅰ代表Br-的变化情况
C.a值等于6
D.原混合溶液中n(FeBr2)=4mol
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物M、N、Q的转化关系为,下列说法正确的是( )
![]()
A. M至N的反应类型是取代反应 B. N的同分异构体有6种
C. 可用酸性KMnO4溶液区分N与Q D. 0.3molQ与足量金属钠反应生成0.15NA个H2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 糖类、油脂、蛋白质在一定条件下均能水解
B. 乙二醇、苯乙烯在一定条件下均可聚合生成高分子化合物
C. 分子式为C4H8C12的有机物共有(不含立体异构)8种
D. ![]() 处于同一平面上的原子数最多为18个
处于同一平面上的原子数最多为18个
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)常温下实验测得4g液态甲醇(CH3OH)在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出90.8kJ的热量。试写出甲醇燃烧热的热化学方程式______。
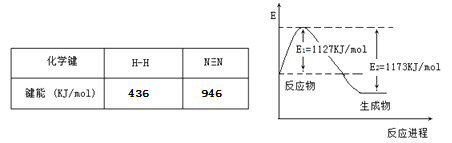
(2)现己知N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化如图所示。根据下列键能数据计算N-H键键能为_____kJmol-1。
(3)用如图所示装置进行中和热测定实验,请回答下列问题:
①仪器A的名称为_______________。
②取50mL0.1molL-1 HCl溶液与50mL0.1molL-1 NaOH溶液在小烧杯中进行中和反应,通过实验并计算可得中和热为54.8kJmol-1,上述实验数值与57.3kJmol-1有偏差,产生此偏差的原因可能是_______(填字母序号)。
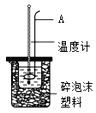
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度
c.一次性把NaOH溶液倒入盛有盐酸的小烧杯中
③若用50mL 0.1molL-1 CH3COOH溶液代替HCl溶液进行上述实验,测得反应前后温度的变化值会_____________(填“偏大”、“偏小”、“不受影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】水热法制备![]() 纳米颗粒的反应为
纳米颗粒的反应为![]() ,下列说法中不正确的是
,下列说法中不正确的是
A.每生成1mol![]() 转移4mol电子
转移4mol电子
B.该反应中![]() 和
和![]() 都是还原剂
都是还原剂
C.3mol![]() 被氧化时有
被氧化时有![]() 被还原
被还原
D.反应方程式中化学计量数![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是___(填编号)。若测定结果偏高其原因可能是__(填字母)。
A.配制标准溶液的固体NaOH中混有Na2O杂质
B.滴定终点读数时,俯视滴定管的刻度,其他操作正确
C.盛装待测液的锥形瓶用蒸馏水洗过后再用待测液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
(2)判断滴定终点的现象是___。
(3)如图是某次滴定时滴定管中的液面,其读数为___mL。
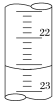
(4)根据下列数据,请计算待测盐酸的浓度:___molL-1。
滴定次数 | 待测体积(mL) | 标准NaOH溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 2.00 | 24.10 |
第三次 | 20.00 | 4.00 | 24.00 |
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定体积的18molL﹣1的浓硫酸中加入过量铜片并加热,被还原的硫酸的物质的量为0.9mol,则浓硫酸的实际体积为( )
A.等于50 mL B.大于50 mL C.等于100 mL D.大于100 mL
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
实验编号 | 实验温度/℃ | c(Na2S2O3)/mol·L-1 | V(Na2S2O3)/mL | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | V(H2O)/mL |
① | 25 | 0.1 | 5.0 | 0.1 | 10.0 | a |
② | 25 | 0.1 | 10.0 | 0.1 | 10.0 | 0 |
③ | 25 | 0.2 | 5.0 | 0.1 | 5.0 | b |
④ | 50 | 0.2 | 5.0 | 0.1 | 10.0 | 5.0 |
其他条件不变时:探究温度对化学反应速率的影响,应选择实验__________(填实验编号);若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中a和b分别为________和________。
(2)某同学设计如下实验流程探究Na2S2O3的化学性质。
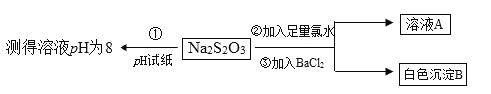
实验操作①中测试时pH试纸的颜色应该接近_____________。
A.红色 B.黄色 C.深蓝色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的_____性。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com