
科目: 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理来解释的是
A. 开启啤酒瓶后,瓶中马上泛起大量泡沫
B. 红棕色的NO2,加压后颜色先变深后变浅
C. 含酚酞的氨水溶液,微热后红色变深
D. H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三种不同的物质中均含有同一种元素,它们之间的转化关系如图示(部分反应物及生成物已略去)。下列说法错误的是:
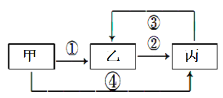
A.若甲为气态氢化物,乙为淡黄色固体,则丙具有漂白性
B.若甲为气体单质,乙为含有极性共价键的非极性分子,则反应②为吸热反应
C.若甲为金属氧化物,乙的水溶液呈酸性,则丙既能与强酸又能与强碱反应
D.若甲为金属单质,反应④为置换反应,则往乙溶液中滴加KSCN,溶液变为血红色
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A.杂化轨道只用于形成![]() 键或用于容纳未参与成键的孤电子对
键或用于容纳未参与成键的孤电子对
B.凡是中心原子采取![]() 杂化轨道成键的分子,其几何构型都是正四面体形
杂化轨道成键的分子,其几何构型都是正四面体形
C.CH2=CH2分子中共有四个σ键和一个π键
D.若把H2S分子写成H3S分子,违背了共价键的方向性
查看答案和解析>>
科目: 来源: 题型:
【题目】向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后,生成深蓝色的配合离子![]()
C.![]() 比
比![]() 中的配位键稳定
中的配位键稳定
D.用硝酸铜溶液代替硫酸铜溶液进行实验,不能观察到同样的现象
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需要0.1mol/LNaOH溶液500mL和0.5mol/L的硫酸溶液500mL。根据这两种溶液的配制情况回答下列问题。
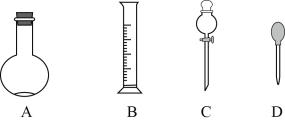
(1)在下图所示仪器中,配制上述溶液肯定不需要的是______________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是________________________。
(2)在容量瓶的使用方法中,下列操作不正确的是______________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加入至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(3)根据计算用托盘天平称取的质量为_________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1mol/L(填“大于”、“小于”或“等于”)。
(4)根据计算得知,需用量筒取质量分数为98%,密度为1.84g/cm3的浓硫酸的体积______mL,如果实验室有15mL、20mL、50mL量筒,应选用______mL量筒最好。在实验中其他操作均正确,若量取浓硫酸时仰视刻度线,则所得溶液浓度______0.5mol/L(填“大于”、“小于”或“等于”)
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA是阿伏加德罗常数的数值。下列说法正确的是
A.用惰性电极电解CuSO4溶液后,如果加入0.1molCu(OH)2能使溶液复原,则电路中转移电子的数目为0.2NA
B.28克由C3H6和C4H8组成的混合气体中含共用电子对数目为6NA个
C.0.1mol氧气作为氧化剂得到电子的数目一定为0.4NA
D.常温下,0.1mol·L-1的碳酸钠溶液中含有的阴离子数大于0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组混合物中,不论二者以什么比例混合,只要总质量一定,完全燃烧时生成CO2的质量也一定的是( )
A.甲烷、辛醛B.丙炔、苯乙烯C.甲醛、甲酸甲酯D.苯、甲苯
查看答案和解析>>
科目: 来源: 题型:
【题目】设 n![]() 是阿伏加德罗常数的数值,下列说法正确的是
是阿伏加德罗常数的数值,下列说法正确的是
A.常温常压下,![]() 克 HCl溶于水后溶液中含有 N
克 HCl溶于水后溶液中含有 N![]() 个HCl分子
个HCl分子![]()
B.标准状况下,![]() 和
和![]() 混合气体含有 N
混合气体含有 N![]() 个氧原子
个氧原子
C.![]() 的
的![]() 溶液中含有阴离子大于
溶液中含有阴离子大于![]() N
N![]() 个
个
D.![]() 与足量Fe反应,转移的电子数为3 N
与足量Fe反应,转移的电子数为3 N![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,该反应中,________是还原剂,________是氧化剂,________是氧化产物,被还原的物质是________。
(2)在一定条件下,反应2NH3+3CuO![]() 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是_______(填序号)。
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是_______(填序号)。
A.该反应是置换反应
B.反应中NH3被氧化为N2
C.在反应中体现了金属铜的还原性
D.在反应中每生成1 mol H2O转移1 mol电子
(3)在反应H2SO3+2H2S==3H2O+3S↓中被氧化的元素与被还原的元素的质量比______。
查看答案和解析>>
科目: 来源: 题型:
【题目】298K时,1mol N2与3mol H2完全反应生成2molNH3的能量变化曲线如图,下列叙述正确的是
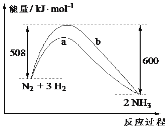
A.形成6 mol N—H键,吸收600 kJ能量
B.b曲线是加入催化剂时的能量变化曲线
C.该反应的ΔH=-92 kJmol-1
D.加入催化剂,能提高N2的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com