
科目: 来源: 题型:
【题目】某同学用中和滴定法测定某烧碱样品的纯度。实验步骤如下:
Ⅰ.配制待测液:用托盘天平称量5.0g烧碱样品(杂质不与盐酸反应),配制成1000mL溶液。
Ⅱ.滴定:取20.00mL所配待测液用0.10mol/L的盐酸标准液进行滴定,达到滴定终点后重复此操作两次。
Ⅲ.记录数据如下:
测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
滴定前读数 | 滴定后读数 | ||
1 | 20.00 | 0.50 | 20.64 |
2 | 20.00 | 1.20 | 24.32 |
3 | 20.00 | 1.30 | 21.40 |
请根据上述实验回答以下问题:
(1)配制待测液时,除烧杯和玻璃棒外,还需要用到的主要玻璃仪器有_____。
(2)盛装0.10mol/L的盐酸标准液应该使用____滴定管(选填“酸式”或“碱式”),滴定时眼睛应注意观察_____。
(3)误差讨论:(选填“偏高”、“偏低”或“无影响”)
①用蒸馏水冲洗锥形瓶,测定结果_____;
②在滴定过程中不慎将数滴酸液滴在锥形瓶外,测定结果____;
③读数时,滴定前俯视,滴定后仰视,测定结果_____。
(4)计算纯度:烧碱样品的纯度是_____(保留一位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)![]() xC(g)ΔH未知,有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)
xC(g)ΔH未知,有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)

A.P3>P4,y轴表示C的转化率
B.P3<P4,y轴表示B的体积分数
C.P3<P4,y轴表示混合气体的密度
D.P3>P4,y轴表示混合气体的平均摩尔质量
查看答案和解析>>
科目: 来源: 题型:
【题目】以食盐为原料进行生产并综合利用的某些过程如图:
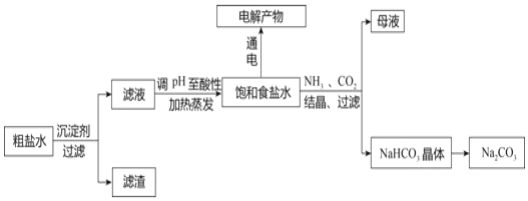
(1)除去粗盐中的微溶物质CaSO4通常用Na2CO3处理,请用平衡移动原理解释说明:____。
(2)人们习惯上把电解饱和食盐水的工业叫做氯碱工业。图1表示电解饱和NaCl溶液的装置,X、Y是石墨棒。实验开始时,在两边同时各滴入几滴酚酞溶液,请回答以下问题:
检验Y电极反应产物的方法是_____。电解NaCl溶液的离子方程式是____。
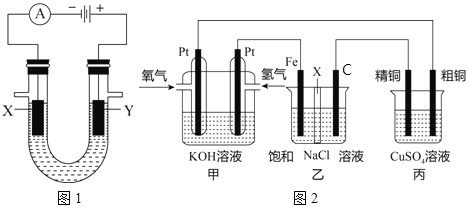
(3)某同学设计一个燃料电池(如图2所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:
①通入氢气电极的反应式为____。
②石墨电极为_____(填“阳极”或“阴极”),反应一段时间后,在乙装置中滴入酚酞溶液,_____区(填“铁极”或“石墨极”)的溶液先变红。
③如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将____(填“增大”“减小”或“不变”)。
④若在标准状况下,有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为_____L;丙装置中阴极析出铜的质量为_____g。(铜的摩尔质量为64)
查看答案和解析>>
科目: 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
(1)根据下列能量变化示意图,请写出![]() 和CO反应的热化学方程式______。
和CO反应的热化学方程式______。

(2)在固定体积的密闭容器中,进行如下化学反应: ![]()
![]() H<0,其平衡常数K与温度T的关系如下表:
H<0,其平衡常数K与温度T的关系如下表:
T/K | 298 | 398 | 498 |
平衡常数K |
|
|
|
①试判断![]() ______
______![]() (填写>、=,<)
(填写>、=,<)
②下列各项能说明该反应已达到平衡状态的是_______(填字母)
a. 容器内![]() 、
、![]() 、
、![]() 的浓度之比为1:3:2
的浓度之比为1:3:2
b. ![]()
c. 容器内压强保持不变
d. 混合气体的密度保持不变
(3)对反应![]()
![]() H>0,在温度分别为
H>0,在温度分别为![]() 、
、![]() 时,平衡体系中
时,平衡体系中![]() 的体积分数随压强变化曲线如下图所示。
的体积分数随压强变化曲线如下图所示。

①A、C两点的反应速率:A_________C(填>、=、<)
②A、C两点![]() 的转化率:A_________C(填>、=、<)
的转化率:A_________C(填>、=、<)
③由状态B到状态A,可以采用的方法是__________。
(4)一定温度下
①若在1L的密闭容器中,充入1 mol![]() 和3 mol
和3 mol![]() 发生反应,并维持容积恒定,10min达到平衡时,气体的总物质的量为原来的7/8,则
发生反应,并维持容积恒定,10min达到平衡时,气体的总物质的量为原来的7/8,则![]() 的转化率a(
的转化率a(![]() )=______,以
)=______,以![]() 表示该过程的反应速率v(
表示该过程的反应速率v(![]() )=_________.
)=_________.
②若在1L的密闭容器中,充入2mol![]() 和6mol
和6mol![]() 发生反应,并维持压强恒定,达到平衡时,
发生反应,并维持压强恒定,达到平衡时, ![]() 平衡浓度比①中
平衡浓度比①中![]() 平衡浓度的2倍________。(填>、=、<)
平衡浓度的2倍________。(填>、=、<)
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒容密闭容器中,将10mol CO和一定量的H2S混合加热并达到下列平衡:CO(g)+H2S(g) ![]() COS(g)+H2(g) K=1,平衡后CO物质的量为8mol。下列说法正确的是( )
COS(g)+H2(g) K=1,平衡后CO物质的量为8mol。下列说法正确的是( )
A.CO、H2S的转化率之比为1∶1
B.达平衡后H2S的体积分数为4%
C.升高温度,COS浓度减小,表明该反应是吸热反应
D.恒温下向平衡体系中再加入CO、H2S、COS、H2各1mol,平衡不移动
查看答案和解析>>
科目: 来源: 题型:
【题目】主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Z族序数之和为10;Y的原子半径在同周期主族元素中最小;W与Z形成的化合物常温下可与饱和NaCl溶液反应,产生的气体常用于切割和焊接金属。下列说法错误的是( )
A.X的单质是人类将太阳能转化为电能的常用材料
B.Y元素可以形成多种含氧酸
C.X元素在自然界中只有化合态没有游离态
D.W与Z形成的化合物与饱和NaCl溶液的反应产生的气体分子中只含极性键
查看答案和解析>>
科目: 来源: 题型:
【题目】欲除去下列物质中的杂质(括号内为杂质)所用试剂和操作方法都正确的( )
①Cl2(HCl):饱和食盐水、过滤
②CO2(SO2):饱和Na2CO3溶液、洗气
③铁粉(铝粉):NaOH溶液、过滤
④MnO2(KCl):水、溶解后过滤
⑤碳粉(碘单质):CCl4、分液
⑥C2H5OH(H2O):加新制CaO后蒸馏
A.①②③B.③④⑥C.②④⑤D.①④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】对下列图像的描述正确的是
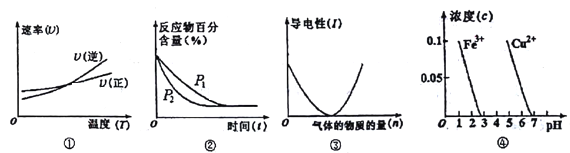
A. 根据图①判断反应A2(g)+3B2(g) ![]() 2AB3(g)的 △H>0
2AB3(g)的 △H>0
B. 图②可表示压强(P)对反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响
3C(g)+D(s)的影响
C. 图③可表示向醋酸溶液通入氨气时,溶液导电性随氨气量的变化
D. 根据图④,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中各微粒的浓度关系正确的是
A.0.1 mol·L-1NaHSO4溶液中:c(Na+)>c(SO42-)>c(H+) >c(OH-)
B.0.1 mol·L-1Na2S溶液中:2 c(Na+)=c(S2-)+c(HS-)+c(H2S)
C.0.1 mol·L-1NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)
D.等体积、等物质的量浓度的乙酸溶液和氢氧化钠溶液混合后:C(Na+)=c(CH3COO-)>c(H+)=c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
A.在0.1molL-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
B.在0.1molL-1Na2CO3溶液中:c(OH-)+c(H+)=c(HCO3-)+2c(H2CO3)
C.向0.2molL-1NaHCO3溶液中加入等体积0.1molL-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D.常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1molL-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com