
科目: 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
I. 分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况下),则该物质的实验式是__________.
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为__________,该物质的分子式是__________.
(3)根据价键理论,预测A的可能结构并写出结构简式__________.
II.结构式的确定:
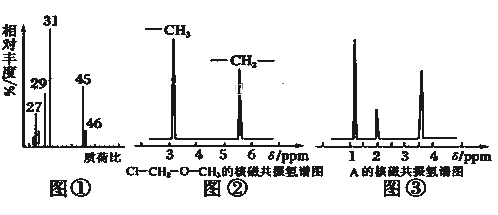
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl﹣CH2﹣O﹣CH3)有两种氢原子如图②.经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________.
查看答案和解析>>
科目: 来源: 题型:
【题目】下面有关晶体的叙述中,不正确的是
A. 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B. 12g石墨中含有σ键的个数为2NA (NA表示阿伏伽德罗常数)
C. 氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D. 干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 沸点:邻二甲苯>间二甲苯>对二甲苯
B. 鸡蛋淸在NH4Cl溶液中能发生盐析,但是不能和盐酸发生化学反应
C.  有机物A的分子式为C16H16O3
有机物A的分子式为C16H16O3
D.  滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键
查看答案和解析>>
科目: 来源: 题型:
【题目】氨基锂(LiNH2)是一种白色有光泽的结晶或粉末,熔点是390 ℃,沸点是430 ℃,溶于冷水,遇热水则强烈水解。在380~400 ℃时锂与氨气直接反应可制得LiNH2,下面是实验室制备LiNH2时可能用到的装置图,回答下列问题。
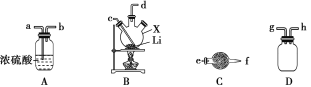
(1)仅从试剂性质角度分析,下列各组试剂不宜用于实验室制备NH3的是__________(填字母)。
A. 浓氨水、CaO B. NH4Cl固体、Ca(OH)2固体
C. 浓氨水 D. NH4NO3固体、NaOH固体
(2)用(1)中合适的试剂制取的NH3按气流方向自左向右,则图中装置的连接顺序为__________(填接口处字母),装置A的作用是__________。
(3)装置C中仪器的名称是___________,盛装的试剂是___________。实验开始后,向X中通入NH3与加热仪器X的先后顺序为___________。
(4)实验室还可用浓氨水与固体NaOH混合制备氨气,但多次实验表明,此方法收集到的NH3量总是比理论值低许多,其最可能的原因是_________。
(5)氨基锂能与热水反应生成LiOH与一种气体,请推测该气体的成分并用实验验证你的结论:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列甲、乙、丙、丁各装置中发生的反应,有关说法正确的是 ( )
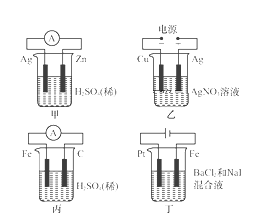
A.甲中负极反应式为2H++2e-=H2↑
B.乙中电解一段时间,溶液的质量会增重
C.丙中H+向碳棒方向移动
D.丁中电解开始时阴极产生黄绿色气体
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20mL的某稀H2SO4溶液中滴入0.1mol/L氨水,溶液中水电离出氢离子浓度随滴入氨水体积变化如图。下列分析正确的是
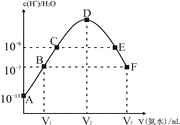
A.E溶液中存在:c(NH4+)>c(SO42-)> c(OH-)> c(H+)
B.稀硫酸的浓度为0.1mol/L
C.C点溶液pH=14-b
D.V2=20mL
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究某固体化合物X(含三种元素)的组成和性质,设计并完成如下实验,其中气体C能使带火星的木条复燃。
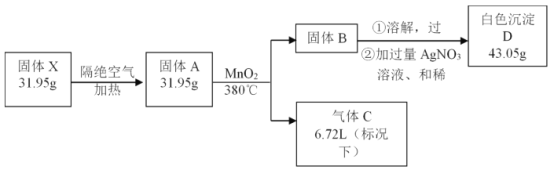
请回答:
(1)白色沉淀D是_______。
(2)固体A中物质生成B和C的化学方程式为__________________。
(3)X的化学式是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体.(图中夹持及尾气处理装置均已略去)请回答下列问题:
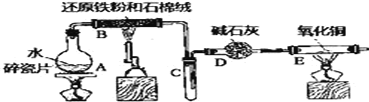
(1)装置B中发生反应的化学方程式是_______________________.
(2)D的作用是________。点燃E处酒精灯之前应进行的操作是_________。E中出现的现象是__________.
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3·6H2O晶体.
①欲检验溶液中含有Fe3+,选用的试剂为____________,现象是_____________.
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因:_______________.
③将此滤液中FeCl2完全氧化为FeCl3最好选择下列物质中的___________.
A.酸性KMnO4溶液 B.Cl2 C.Na2O2 D.FeCl3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.要证明硫酸亚铁铵晶体中含有![]() ,可以取少量晶体溶于水,加入足量NaOH浓溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体
,可以取少量晶体溶于水,加入足量NaOH浓溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体
B.![]() 、
、![]() 、
、![]() 等强氧化剂或其混合物不能研磨,否则将引起爆炸
等强氧化剂或其混合物不能研磨,否则将引起爆炸
C.常温下用pH试纸分别测定![]() 溶液和
溶液和![]() 溶液的pH,可以比较浓度对水解程度的影响
溶液的pH,可以比较浓度对水解程度的影响
D.过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.在铁片上镀铜时,若阴极增重3.2g,则电镀液中通过的电子的物质的量为0.1mol
B.钢铁电化学腐蚀的两种类型主要区别在于水膜的PH不同,引起的负极反应不同
C.参加反应的物质的性质是决定化学反应速率的重要因素
D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极区产生的Cl2进入阳极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com