
科目: 来源: 题型:
【题目】四甲基氢氧化铵[(CH3)4NOH]是强碱,常温下甲胺(CH3NH2·H2O)的电离常数为Kb,且pKb=-lgKb=3.38。常温下,在体积均为20mL、浓度均为0.1mol·L-1的四甲基氢氧化铵溶液和甲胺溶液,分别滴加浓度为0.1mol·L-1的盐酸,溶液的导电率与盐酸体积的关系如图所示。

下列说法正确的是
A. 曲线1代表四甲基氢氧化铵溶液
B. 在b、c、e三点中,水的电离程度最大的点是e
C. b点溶液中存在c(H+)=c(OH-)+c(CH3NH2·H2O)
D. 常温下,CH3NH3Cl水解常数的数量级为10-11
查看答案和解析>>
科目: 来源: 题型:
【题目】对室温下氢离子浓度、体积均相同的HCl溶液和CH3COOH溶液分别采取以下措施,
有关叙述正确的是( )
A.加适量的CH3COONa晶体,两溶液的氢离子浓度减小
B.使温度升高20 ℃,两溶液的氢离子浓度不变
C.加水稀释2倍,两溶液的氢离子浓度增大
D.加足量的Zn充分反应后,两溶液中产生的氢气一样多
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH-ΔΗ>0,下列叙述正确的是( )
H++OH-ΔΗ>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体NaOH,平衡逆向移动,c(OH-)降低
D.向水中加入少量固体NaCl,pH变大
查看答案和解析>>
科目: 来源: 题型:
【题目】正己烷是优良的有机溶剂,其某种模型如图所示。下列有关说法正确的是( )

A.正己烷的分子式为![]()
B.正己烷的一氯代物有3种
C.正己烷能与溴水发生取代反应而使溴水褪色
D.正己烷中的所有碳原子位于同一条直线
查看答案和解析>>
科目: 来源: 题型:
【题目】对于常温下pH=1的硝酸溶液,有关叙述:
①该溶液1mL稀释至100mL后,pH=3
②向该溶液中加入等体积、pH=13的氢氧化钡溶液恰好完全中和
③该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为1×10﹣12
④向该溶液中加入等体积、等浓度的氨水,所得溶液pH=7
其中正确的是
A. ①② B. ①③ C. ②④ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.可以用灼烧后闻气味区别棉花和羊毛
B.油脂水解一定全部生成甘油和高级脂肪酸
C.向蛋白质溶液中加入重金属盐溶液可使蛋白质产生盐析
D.淀粉和纤维素的组成都是![]() ,但淀粉水解纤维素不能水解
,但淀粉水解纤维素不能水解
查看答案和解析>>
科目: 来源: 题型:
【题目】下列曲线中,可以描述乙酸(甲, Ka=1.8×10-5)和一氯乙酸(乙, Ka=1.4×10-3)在水中的电离度与浓度关系的是()

A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法不正确的是( )

A.图中五点Kw间的关系:B>C>A=D=E
B.若从A点到E点,可采用在水中加入少量碱的方法
C.若从A点到C点,可采用温度不变时在水中加入适量NH4Cl固体的方法
D.若处在B点时,将pH=2的硫酸与pH=12的KOH溶液等体积混合后,溶液显碱性
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研小组以难溶性钾长石(K2OAl2O36SiO2)为原料,提取Al2O3、K2CO3等物质,工艺流程如下:
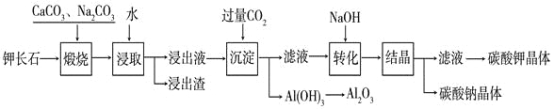
(1)煅烧过程中钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式是:______________________________。
(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2—+ 2H2O![]() Al(OH)3 + OH— ,“浸取”时应保持溶液呈___________性(填“酸”或“碱”)。
Al(OH)3 + OH— ,“浸取”时应保持溶液呈___________性(填“酸”或“碱”)。
(3)“转化”时加入NaOH的主要作用是______________________________(用离子方程式表示)。
(4)上述工艺中可以循环利用的主要物质是_______________、_______________和水。
(5)以Al2O3为原料,以石墨为电极,通过电解法可制得金属铝。电解池中接电源负极的一极的电极反应式是___________________。长时间电解后,需要更换新的石墨电极的是________极(填“阴”或“阳”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】废旧锂离子电池的回收利用意义重大,其正极废料的主要成分是![]() ,铝、炭黑及其他杂质,回收利用的流程如图1:
,铝、炭黑及其他杂质,回收利用的流程如图1:
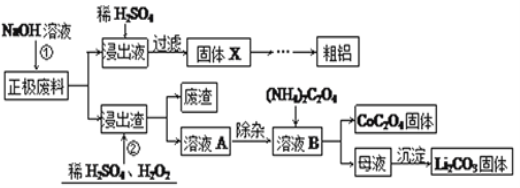
图1
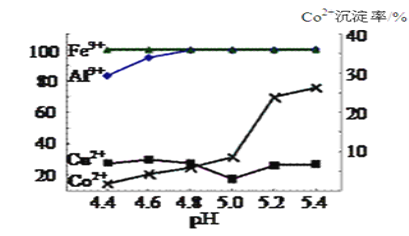
图2
已知A溶液主要的金属离子是![]() 、
、![]() ,还含有少量
,还含有少量![]() 、
、![]() 、
、![]() .
.
![]() 步骤
步骤![]() 中铝溶解的离子方程式为 ______ ,固体X的成分是 ______ ;
中铝溶解的离子方程式为 ______ ,固体X的成分是 ______ ;
![]() 步骤
步骤![]() 中
中![]() 固体溶解的化学方程式为 ______ ,该反应的还原剂是 ______ ;
固体溶解的化学方程式为 ______ ,该反应的还原剂是 ______ ;
![]() 实验表明溶液A中各种金属离子的沉淀率随pH的变化如图2,除杂时加入氨水调节溶液的pH,可除去杂质离子是 ______ ;
实验表明溶液A中各种金属离子的沉淀率随pH的变化如图2,除杂时加入氨水调节溶液的pH,可除去杂质离子是 ______ ;
![]() 母液中含量最大三种离子是 ______ ;
母液中含量最大三种离子是 ______ ;
![]() 从1000g锂离子电池正极材料
从1000g锂离子电池正极材料![]() 元素含量为
元素含量为![]() 中可回收
中可回收![]() 质量为 ______
质量为 ______ ![]() 已知回收率为
已知回收率为![]() ,
,![]() 的化学式量为74).
的化学式量为74).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com