
科目: 来源: 题型:
【题目】重铬酸钾![]() 是高中化学常见的氧化剂,工业上以铬铁矿为原料用碱溶氧化法制备.铬铁矿中通常含有
是高中化学常见的氧化剂,工业上以铬铁矿为原料用碱溶氧化法制备.铬铁矿中通常含有![]() 、FeO、
、FeO、![]() 、
、![]() 等.
等.

已知:①![]() 遇水强烈水解.
遇水强烈水解.
②![]() 黄色
黄色![]() 橙色
橙色![]()
请回答下列问题:
(1)将矿石粉碎的目的是 ______ ;高温灼烧时![]() 发生反应的化学方程式为 ______ .
发生反应的化学方程式为 ______ .
(2)滤渣1中有红褐色物质,写出生成该物质反应的离子方程式 ______ ![]() 滤渣2的主要成分是
滤渣2的主要成分是![]() 和 ______ .
和 ______ .
(3)用简要的文字说明![]() 溶液中加入KCl固体,降温析出
溶液中加入KCl固体,降温析出![]() 的原因 ______ .
的原因 ______ .
(4)![]() 时,对反应
时,对反应![]() 黄色
黄色![]() 橙色
橙色![]() ,取
,取![]() 溶液进行实验,测得部分实验数据如下:
溶液进行实验,测得部分实验数据如下:
时间 | 0 |
|
|
|
|
|
|
|
|
| |
| 0 |
|
|
|
①反应达到平衡时,溶液的![]() ,该反应平衡常数K为 ______ .
,该反应平衡常数K为 ______ .
②下列有关说法正确的 ______ .
![]() 加少量
加少量![]() 固体,可使溶液的橙色加深
固体,可使溶液的橙色加深
![]() 时
时![]()
![]() 溶液中
溶液中![]() :
:![]() :1时该反应已达平衡状态
:1时该反应已达平衡状态
![]() 反应达到平衡时
反应达到平衡时![]() 的转化率为
的转化率为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2=NH4BO2+4H2O。已知两极室中电解质足量,下列说法正确的是( )

A.正极的电极反应式为2H++2e-═H2↑
B.电池工作时,H+通过质子交换膜向负极移动
C.电池工作时,正、负极分别放出H2和NH3
D.工作一段时间后,若左右两极室质量差为1.9g,则电路中转移0.6mol电子
查看答案和解析>>
科目: 来源: 题型:
【题目】100℃时,向某恒容密闭容器中加入1.6 mol ·L-1的Q后会发生如下反应:2Q(g) ![]() M(g) 。其中M的物质的量浓度随时间的变化如图所示。
M(g) 。其中M的物质的量浓度随时间的变化如图所示。
下列说法错误的是
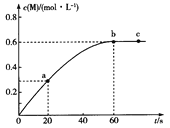
A.从反应开始到刚达到平衡时间段内,v(Q)=0.02 mol·L-1·s-1
B.a、b两时刻生成Q的速率:v(a)<v(b)
C.用Q浓度变化值表示的ab、bc两个时段内的反应速率:v(ab)>v(bc)=0
D.其他条件相同,起始时将0. 2 mol·L-1氦气与Q混合,则反应达到平衡所需时间少于60 s
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:

已知:
颜色、状态 | 沸点(℃) | 密度(g·cm-3) | |
苯甲酸 | 无色、片状晶体 | 249 | 1.265 9 |
苯甲酸乙酯 | 无色澄清液体 | 212.6 | 1.05 |
乙醇 | 无色澄清液体 | 78.3 | 0.789 3 |
环己烷 | 无色澄清液体 | 80.8 | 0.731 8 |
*苯甲酸在100 ℃会迅速升华。
实验步骤如下:
a.在100 mL圆底烧瓶中加入12.20 g苯甲酸、25 mL乙醇(过量)、20 mL 环己烷,以及4 mL浓硫酸,混合均匀并加入沸石,按下图所示装好仪器,控制温度在65~70 ℃加热回流2 h。反应时环己烷—乙醇—水会形成“共沸物”(沸点62.6 ℃)蒸馏出来,再利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。

b.反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
c.将烧瓶内反应液倒入盛有适量水的烧杯中,加入饱和Na2CO3溶液。
d.用分液漏斗分出有机层,水层用25 mL乙醚萃取分液,然后合并至有机层。加入氯化钙,对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收210~213 ℃的馏分。
e.检验合格,测得产品体积为12.86 mL。
回答下列问题:
(1)反应中浓硫酸的作用是:________________。步骤a中加入沸石作用:____________。温度在65~70 ℃加热的方法是:________________。
(2)仪器A的名称是:________________。该反应类型为______________。
(3)关于步骤d中的分液操作叙述正确的是________。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞。将分液漏斗倒转过来,用力振摇
B.振摇几次后需打开分液漏斗下口的玻璃活塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,需将玻璃塞上的凹槽对准漏斗口上的小孔
(4)上述实验中饱和碳酸钠溶液的作用是___________________。
(5)当达到该反应的限度,也即达到化学平衡状态。下列描述能说明该反应已达到化学平衡状态的有(填序号)_______________________。
①单位时间里,生成1mol苯甲酸乙酯,同时生成1mol水
②单位时间里,生成1mol苯甲酸乙酯,同时生成1mol乙醇
③单位时间里,消耗1mol乙醇,同时消耗1mol苯甲酸
④正反应的速率与逆反应的速率相等
⑤合物中各物质的浓度不再变化
⑥混合物中各物质的浓度相等
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量.查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:

(1)提取前将铝土矿“粉碎”目的是__________。
(2)固体B的主要用途有________________(写出一条即可)。
(3)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式有: _____________(至少写一个)。
(4)第②步中加入过量盐酸的目的是____________________;实验室配制200mL 8mol/L的盐酸需要的玻璃仪器有__________________。
(5)能否把第③步中的氨水换成氢氧化钠__________,理由___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将V 1 mL 0.1mol·L-1的Fe2(SO4)3溶液与2mL 0.1mol·L-1KI溶液混合,待充分反应后,下列方法可证明该反应具有一定限度的是( )
A.若V1<1,加入淀粉B.若V1≤1,加入KSCN溶液
C.若V1≥1,加入AgNO3溶液D.加入Ba(NO3)2溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
A.异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B.2氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应
C.甲苯在一定条件下发生硝化反应生成一硝基甲苯的反应
D.邻羟基苯甲酸与NaHCO3溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W的原子序数依次增大,四种元素形成的单质依次为m、n、p、q;r、t、u 是这些元素组成的二元化合物,其中u为葡萄酒中的抑菌成分;25 ℃,0.01 mol/L的v溶液中:  = 1.0×10-10。上述物质的转化关系如图所示,下列说法不正确的是
= 1.0×10-10。上述物质的转化关系如图所示,下列说法不正确的是

A. 简单离子半径:W>Y>Z>X
B. W,Y分別与X元素形成的简单化合物的沸点: Y> W
C. Z2Y和ZX都只存在离子键
D. v能抑制水的电离,u能促进水的电离
查看答案和解析>>
科目: 来源: 题型:
【题目】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:在容器为1L的密闭容器中充入1molCO2和3molH2 ,平衡时CO2的物质的量为0.25mol,CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。
CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。

请回答下列问题:
(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量______(填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:__________。甲醇分子中的化学键类型是________(填“离子键”或“共价键”)。
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是__________,发生的是__________(填"氧化"或"还原")反应。
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:___________________
(5)平衡时H2的转化率为__________平衡时混合气体中CH3OH(g)的体积分数为__________。
(6)下列事实能表明该反应已达平衡状态的是(_______)(填序号)
A.CO2(g)的浓度不再发生变化
B.单位时间内消耗1mol CO2的同时生成3mol H2
C.在一个绝热的容器中,混合物的温度不再发生变化
D.在一个容积固定的容器内,压强不再发生变化
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关图像的说法正确的是

A. 图甲表示:向某明矾溶液中逐滴加入NaOH溶液至过量,生成沉淀的物质的量与滴加NaOH溶液体积的关系
B. 图乙表示:向含等物质的量的NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸至过量,生成气体的体积与滴加HCl溶液体积的关系
C. 图丙表示:在稀硝酸溶液中逐渐加入铁粉至过量,溶液中Fe3+物质的量与逐渐加入铁粉物质的量的变化关系
D. 除去混在硝酸钾中少量的氯化钠可用“蒸发浓缩、趁热过滤”的方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com