
科目: 来源: 题型:
【题目】列各组离子一定能在指定环境中大量共存的是( )
A.在c(H+)=10-10 mol/L的溶液中 Al3+ 、NH![]() 、Cl- 、NO
、Cl- 、NO![]()
B.pH值为13的溶液 K+ 、SO![]() 、Na+、S2-
、Na+、S2-
C.水电离出来的c(H+)=10-12mol/L的溶液 K+、NH4+、Cl-、ClO-
D.甲基橙呈红色的溶液中 Fe3+、Na+ 、SO42-、CO![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=-41kJ·mol-1。相同温度下,在容积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
CO2(g)+H2(g) ΔH=-41kJ·mol-1。相同温度下,在容积相同的两个恒温密闭容器中,加入一定量的反应物发生反应。相关数据如下:
容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系能量的变化 | |||
CO | H2O | CO2 | H2 | ||
① | 1 | 4 | 0 | 0 | 放出热量:32.8kJ |
② | 0 | 0 | 1 | 4 | 热量变化:QkJ |
下列说法中,不正确的是( )
A.容器①中反应达平衡时,CO的转化率为80%
B.容器①中CO的转化率等于容器②中CO2的转化率
C.平衡时,两容器中CO2的浓度相等
D.容器①时CO的反应速率等于H2O的反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】在一容积为2L的恒温恒容密闭容器中充入2mol SO2和1mol O2,发生反应2SO2(g)+O2(g) ![]() 2SO3(g) △H=-Q kJ·mol-l (Q>O),下列有关说法不正确的是
2SO3(g) △H=-Q kJ·mol-l (Q>O),下列有关说法不正确的是
A. 反应达到平衡时,放出热量为QkJ
B. 若容器的压强不再发生交化,则反应达到平衡
C. 反应过程中c(SO2)+ c(SO3)=1 mol·L-1恒成立
D. 平衡时,SO2、O2的转化率相等
查看答案和解析>>
科目: 来源: 题型:
【题目】下列能量转化过程与氧化还原反应无关的是
A. 硅太阳能电池 | B. 锂离子电池放电 | C. 火箭的燃料燃烧 | D. 葡萄糖提供能量 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】已知下列物质在 20 ℃下的 Ksp 如下,试回答下列问题:
化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
Ksp | 2.0×10-10 | 5.4×10-13 | 8.3×10-17 | 2.0×10-48 | 2.0×10-12 |
(1)20 ℃时,上述五种银盐饱和溶液中,Ag+物质的量浓度由大到小的顺序是_______(用化学式表示)。
(2)向等浓度的 KCl 和 KBr 的混合溶液中逐渐加入 AgNO3 溶液,当两种沉淀共存时,![]() =__________。
=__________。
(3)测定水中 Cl-含量时,常用 Ag+进行滴定,滴定时,应加入的指示剂是_____。
A.KBr B.KI C.K2S D.K2CrO4
查看答案和解析>>
科目: 来源: 题型:
【题目】I.依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。
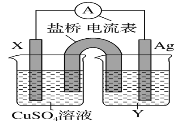
请回答下列问题:
(1)电极 X 的材料是__________填化学式);电解质溶液 Y 是______填化学式)。
(2)银电极发生______填“氧化”或“还原”)反应,其电极反应式为_________;X 电极反应式为_____。
II. 高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放 电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
请回答下列问题:
(1)已知放电时负极反应为 Zn-2e-+2OH- ===Zn(OH)2,则正极反应 为_____________。
(2)放电时,_____(填“正”或“负”)极附近溶液的 pH 升高。
(3)高铁电池充电时,电池的负极与电源的_____(填“正极”或“负极”),充 电时与电池负极相连的电极反应为__________。
III.近几年开发的甲醇燃料电池采用铂作电极催化剂,电池中的质子交换膜只允许质子和 水分子通过。其工作原理的示意图如下:
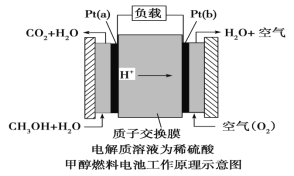
请回答下列问题: (1)该燃料电池的总反应为_________。
(2)Pt(a)电极是电池的_____(填“正”或“负”)极,电极反应式为:__________; Pt(b)电极反应式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有常温条件下甲、乙、丙三种溶液,甲为 0.1 mol·L-1 的 NaOH 溶液, 乙为 0.1 mol·L-1 的 HCl 溶液,丙为 0.1 mol·L-1 的 CH3COOH 溶液,试回答下列问题:
(1)甲溶液的 pH=_____。
(2)丙溶液中存在的电离平衡为_____(用电离方程式表示)。
(3)甲、乙、丙三种溶液中由水电离出的 c(OH-)的大小关系为 _____。
A. 甲=乙=丙 B. 甲=乙>丙 C.甲=乙<丙 D.无法判断
(4)某同学用甲溶液分别滴定 20.00 mL 乙溶液和 20.00 mL 丙溶液,得到如图所示两 条滴定曲线,请完成有关问题:
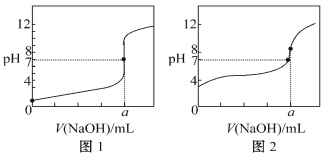
①甲溶液滴定丙溶液的曲线是_____(填“图 1”或“图 2”);
②a=_____mL。
(5)将等体积的甲溶液和丙溶液混合后,溶液呈_____(填“酸性”、“中性”或 “碱性”)。溶液中离子浓度大小顺序为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在恒温恒容的密闭容器中发生反应:![]() 下列说法不正确的是
下列说法不正确的是
A.该反应的平衡常数表达式: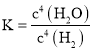
B.若容器内气体的压强保持不变,说明该反应已达到平衡状态
C.若![]() 足量,改变起始充入
足量,改变起始充入![]() 的浓度,达平衡时
的浓度,达平衡时![]() 的转化率不变
的转化率不变
D.经2min后,![]() 浓度下降了
浓度下降了![]() 则反应速度为
则反应速度为![]() .
.
查看答案和解析>>
科目: 来源: 题型:
【题目】一种新型的乙醇电池(DEFC)是用磺酸类质子溶剂作电解质,在 200℃左右时供电( 如 下 图 所 示 ), 比 甲 醇 电 池 效 率 高 出 32 倍 , 且 比 较 安 全 。 电 池 总 反 应 为C2H5OH+3O2==2CO2+3H2O。则下列说法正确的是( )
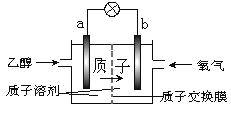
A.a 极为电池的正极
B.电池正极的电极反应:O2 + 4H+ + 4e- = 2H2O
C.电池工作时电子由 b 极沿导线经灯泡再到 a 极
D.溶液中 H+ 向 a 电极移动
查看答案和解析>>
科目: 来源: 题型:
【题目】某密闭容器中,![]() 在一定条件下达到平衡,下列说法正确的是
在一定条件下达到平衡,下列说法正确的是
A.加入少量A,B的转化率增大
B.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
C.增大压强,平衡不移动,正、逆反应速率不变
D.加入催化剂,反应速率增大,平衡常数不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com