
科目: 来源: 题型:
【题目】下列说法不正确的是
A.用石灰石或石灰乳进行燃煤烟气脱硫![]() 除
除![]() 可获得副产品石膏
可获得副产品石膏
B.金属的电化学防护措施有牺牲阳极的阴极保护法和外加电流的阴极保护法
C.若在水果贮藏室中,放几块被![]() 溶液浸透过的“砖块”,可延长水果保存时间
溶液浸透过的“砖块”,可延长水果保存时间
D.常温时,某可逆反应的平衡常数越大则其反应速率就越快
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生活密切相关,下列有关说法正确的是
①糖类、蛋白质、油脂属于天然高分子化合物
②煤经气化和液化两个物理变化过程,可变为清洁能源
③制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料
④用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出
⑤苯、油脂均不能使酸性![]() 溶液褪色
溶液褪色
⑥葡萄糖、果糖的分子式均为![]() ,二者互为同分异构体
,二者互为同分异构体
⑦甲烷和![]() 的反应与乙烯和
的反应与乙烯和![]() 的反应属于同一类型的反应
的反应属于同一类型的反应
⑧乙醇、乙酸均能与Na反应放出![]() ,二者分子中官能团相同
,二者分子中官能团相同
⑨中和滴定实验时,用待测液润洗锥形瓶
⑩非金属元素组成的化合物中只含共价键
A.1B.2C.3D.4
查看答案和解析>>
科目: 来源: 题型:
【题目】下表中实验操作、现象与结论对应关系正确的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 以酚酞为指示剂,用盐酸标准液滴定氢氧化钠溶液 | 溶液由红色变为浅红色便立刻读数 | 测得氢氧化钠溶液的浓度偏大 |
B | 用广泛pH试纸测定1mol/L NaHSO3 溶液的酸碱性 | 测得pH=3.2 | NaHSO3 溶液呈酸性,证明HSO3-的电离大于水解 |
C | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体 | 有白色沉淀生成,溶液红色变浅 | 证明纯碱溶液呈碱性是由CO32-水解引起的 |
D | 在0.1mol/LNa2S溶液中滴加少量等浓度的ZnSO4溶液,再加入少量等浓度的CuSO4溶液 | 先产生白色ZnS沉淀,后产生黑色CuS沉淀 | Ksp(ZnS)>Ksp(CuS) |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数值。关于常温下pH=2的H3PO4溶液,下列说法正确的是( )
A. 加水稀释使电离度增大,溶液pH减小
B. 每升溶液中的H+数目为0.02NA
C. 加入NaH2PO4固体,溶液酸性增强
D. c(H+)=c(H2PO4-)+2c(HPO42-)+3c(PO43-)+c(OH)
查看答案和解析>>
科目: 来源: 题型:
【题目】铁及其化合物在生活、生产中有广泛应用。请回答下列问题:
(1)在实验室中,![]() 可用铁粉和______反应制备,
可用铁粉和______反应制备,![]() 可用铁粉和______反应制备。
可用铁粉和______反应制备。
(2)黄铁矿![]() 主要成分为
主要成分为![]() 是生产硫酸和冶炼钢铁的重要原料。高温下可发生反应:
是生产硫酸和冶炼钢铁的重要原料。高温下可发生反应:
![]() ,该过程中若有
,该过程中若有![]()
![]() 参加反应,则反应过程中转移______mol电子。
参加反应,则反应过程中转移______mol电子。
(3)![]() 与Zn组成新型二次电池高铁电池,电解液为碱溶液,其反应式为:
与Zn组成新型二次电池高铁电池,电解液为碱溶液,其反应式为:![]() ,放电时电池的负极反应式为______;充电时电解液的pH______
,放电时电池的负极反应式为______;充电时电解液的pH______![]() 填“增大”“减小”或“不变”之一
填“增大”“减小”或“不变”之一![]() 。
。
(4)某同学向盛有![]() 溶液的试管中加入几滴酸化的
溶液的试管中加入几滴酸化的![]() 溶液,溶液变成棕黄色,发生反应的离子方程式为______;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是______;生成沉淀的原因是______
溶液,溶液变成棕黄色,发生反应的离子方程式为______;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是______;生成沉淀的原因是______![]() 用平衡移动原理解释
用平衡移动原理解释![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y原子的最外层电子数是电子层数的2倍,Z是地壳中含量最高的非金属元素,Q元素形成的单质是重要的半导体材料,R元素原子核外的M电子层电子数比L层少2个。请回答下列问题:
(1)画出Z的原子结构示意图__________,其氢化物的电子式__________。
(2)![]() 、Z、Q三种元素的原子半径由大到小的顺序__________
、Z、Q三种元素的原子半径由大到小的顺序__________![]() 用元素符号表示
用元素符号表示![]() 。
。
(3)![]() 元素在周期表中的位置_________,与Q同主族第四周期的元素的原子序数是_____,在周期表的以下区域中,可以找到类似的半导体材料的是__________
元素在周期表中的位置_________,与Q同主族第四周期的元素的原子序数是_____,在周期表的以下区域中,可以找到类似的半导体材料的是__________![]() 填字母序号
填字母序号![]() 。
。
![]() 过渡元素区域
过渡元素区域
![]() 金属和非金属元素的分界线附近
金属和非金属元素的分界线附近
![]() 含有氟、氯、硫、磷等元素的区域
含有氟、氯、硫、磷等元素的区域
![]() 下列能说明Y与R元素非金属性相对强弱的是__________。
下列能说明Y与R元素非金属性相对强弱的是__________。
![]() 单质与氢气化合的难易程度
单质与氢气化合的难易程度
![]() 含氧酸的酸性:
含氧酸的酸性:![]()
![]() 与R相互形成的化合物中元素的化合价
与R相互形成的化合物中元素的化合价
Ⅱ![]() 已知:
已知:
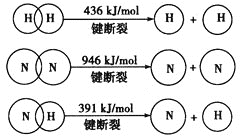
合成氨的热化学方程式是___________________________________。
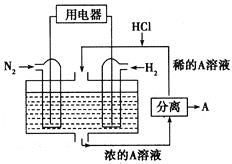
Ⅲ![]() 有人设想以
有人设想以![]() 和
和![]() 为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。正极的电极方程式为_________。
为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。正极的电极方程式为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇属于可再生能源,可作汽车的燃料,下列能正确表示甲醇燃烧热的热化学方程式为
A.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=+763.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=+763.3 kJ·mol-1
B.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ΔH=-763.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=-763.3 kJ·mol-1
C.CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(g) ΔH=-675.3 kJ·mol-1
O2(g)=CO2(g)+2H2O(g) ΔH=-675.3 kJ·mol-1
D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1 526.6 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组设计如图装置,验证黄铜矿(主要成分CuFeS2)在空气中的氧化产物并测定CuFeS2的纯度(杂质不参与反应)。
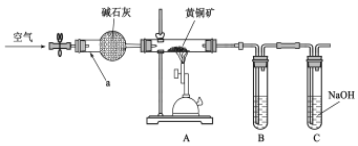
回答下列问题。
(1)仪器a的名称_________,碱石灰的作用______________________________________。
(2)为检验灼烧黄铜矿产生的气体,B中可选__________________
a.HNO3溶液 b.品红溶液 c.BaCl2溶液 d.溴水 e.KMnO4溶液
(3)C中NaOH的作用____________________________________________________
(4)样品经煅烧后的固体中铜元素以泡铜(Cu、Cu2O)形式存在,其中Cu2O能与稀H2SO4反应生成Cu和CuSO4。
①请设计实验验证泡铜中含有Cu2O____________________________________________。
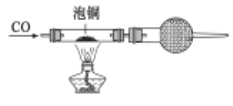
②用泡铜与CO反应来制取粗铜装置如下图,实验时依次进行的操作:
组装仪器→检查装置气密性→加装药品→____________→____________→…→尾气处理;CO还原Cu2O的化学方程式_______________________________________________
(5)为测定CuFeS2的纯度,称取a g黄铜矿样品充分灼烧,从灼烧产物中分离出泡铜,完全溶于稀硝酸,并配成200 mL的溶液,取20.00 mL该溶液用c mol· L-1的标准液EDTA(用H2Y2-表示)滴定至终点(标准液不与杂质反应),消耗EDTA V mL,则CuFeS2的纯度为____________。(滴定时的反应为:Cu2++H2Y2-===CuY2-+2H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)为原料,制备粗铅,实现铅的再生利用.其工作流程如图1所示:
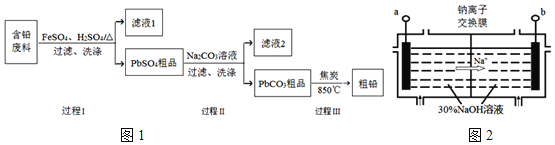
已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-14.
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是______.
(2)过程Ⅰ中,Fe2+催化过程可表示为:
![]()
![]() .
.
![]() 写出ii的离子方程式:______.
写出ii的离子方程式:______.
![]() 下列实验方案可证实上述催化过程.将实验方案补充完整.
下列实验方案可证实上述催化过程.将实验方案补充完整.
![]() 向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红.
向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红.
![]() ______.
______.
(3)过程Ⅱ的目的是脱硫.若滤液2中c(SO42-)=1.6molL-1,c(CO32-)=0.1molL-1,则PbCO3中______![]() 填“是”或“否”
填“是”或“否”![]() 混有PbSO4.
混有PbSO4.
(4)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图2所示.将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:![]()
![]() 与外接电源的______极相连.
与外接电源的______极相连.
![]() 电解过程中,PbO2、PbO、HPbO2-在阴极放电,其中PbO2放电的电极反应式为______.
电解过程中,PbO2、PbO、HPbO2-在阴极放电,其中PbO2放电的电极反应式为______.
![]() 与传统无膜固相电解法相比,使用钠离子交换膜可以提高Pb元素的利用率,原因是______.
与传统无膜固相电解法相比,使用钠离子交换膜可以提高Pb元素的利用率,原因是______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com