
科目: 来源: 题型:
【题目】全钒液流电池充电时间短,续航能力强,其充放电原理为VO2++V3++H2O![]() VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是
VO2++V2++2H+。以此电池为电源,用石墨电极电解Na2SO3溶液,可得到NaOH和H2SO4示意图如下。下列说法错误的是

A. 全钒液流电池放电时,正极的电极反应式为VO2++2H++e-=VO2++H2O
B. 图中a电极为阴极,N物质是H2
C. 全钒液流电池充电时,V3+被氧化为VO2+
D. 电解时,b电极的反应式为SO32-+H2O-2e-=SO42-+2H+
查看答案和解析>>
科目: 来源: 题型:
【题目】将10 mL0.2 mol/L氨水和10 mL0.1 mol/L盐酸混合后,溶液里各种离子物质的量浓度的关系是 ( )
A.c (OH-) = c(NH4+) + c (H+)B.c (Cl-)> c(NH4+)> c (H+) > c (OH-)
C.c(NH4+) > c (Cl-)> c (OH-)> c (H+)D.c (Cl-)> c (H+) > c (NH4+) > c (OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
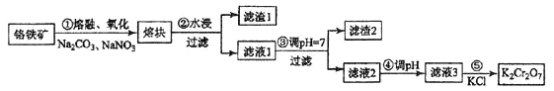
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3![]() Na2CrO4+ Fe2O3+CO2+ NaNO2
Na2CrO4+ Fe2O3+CO2+ NaNO2
上述反应配平后FeO·Cr2O3与NaNO3的系数比为__________。该步骤不能使用陶瓷容器,原因是________________。
(2)滤渣1中含量最多的金属元素是____________,滤渣2的主要成分是_____________及含硅杂质。
(3)步骤④调滤液2的pH使之变____________(填“大”或“小”),原因是___________________(用离子方程式表示)。
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到___________(填标号)得到的K2Cr2O7固体产品最多。

a.80℃ b.60℃ c.40℃ d.10℃
步骤⑤的反应类型是___________________。
(5)某工厂用m1 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品 m2 kg,产率为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】合理利用资源,降低碳的排放,实施低碳经济是今后经济生活主流方向。
(1)下列措施不利于有效减少二氧化碳排放的是________。
A.植树造林,保护森林,保护植被
B.加大对煤和石油的开采,并鼓励使用石油液化气
C.推广使用节能灯和节能电器,使用空调时夏季温度不宜设置过低,冬天不宜过高
D.倡导出行时多步行和骑自行车,建设现代物流信息系统,减少运输工具空驶率
(2)CO2合成生产燃料甲醇(CH3OH)是碳减排的新方向。进行如下实验:某温度下在1 L的密闭容器中,充2 mol CO2和6 mol H2,发生:CO2(g)+3H2(g )![]() CH3OH(g)+H2O(g),现测得CO2和CH3OH(g)的浓度随时间变化如下图1所示。从反应开始到平衡时CO2的转化率为_________。氢气的平均反应速率v(H2)=_______mol/(L·min)。该温度下的平衡常数为________。
CH3OH(g)+H2O(g),现测得CO2和CH3OH(g)的浓度随时间变化如下图1所示。从反应开始到平衡时CO2的转化率为_________。氢气的平均反应速率v(H2)=_______mol/(L·min)。该温度下的平衡常数为________。
(3)CO在催化作用下生成甲醇:CO(g)+2H2(g)![]() CH3OH(g)。已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如图所示。
CH3OH(g)。已知密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率(α)与温度、压强的关系如图所示。
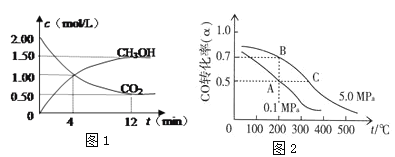
①该反应的ΔH_____0;ΔS____0。 (填“>、=、<”)
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA ____ tC(填“>、=、<”)
③A、B、C三点对应的平衡常数分别为KA、KB、KC,则的大小关系是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】二甲醚是一种重要的精细化工产品,被广泛用于制药、染料、农药及日用化工。以下为其中一种合成二甲醚的方法:
①CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.1kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1kJ·mol-1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-24.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5kJ·mol-1
③2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H3
CH3OCH3(g)+3H2O(g) △H3
(1)△H3=________kJ·mol-1。
(2)某温度下在容积为2L的密闭容器中加入CH3OH(g)发生反应②,测得有关数据如下:
反应时间/min | 0 | 1 | 2 | 3 | 4 |
n(CH3OH)/mol | 1.02 | 0.4 | 0.2 | 0.02 | 0.02 |
①前2min内,H2O(g)的平均反应速率为________mol·L-1·min-1;此反应在该温度下的平衡常数为________;若再向容器中分别加入CH3OH(g)0.02mol、CH3OCH3(g)1.0mol,此时该反应中υ正________υ逆(填“>”、“<”或“=”)。
②根据文献,甲醇的转化率可以根据冷凝的液相中甲醇与水的百分含量来计算(忽略挥发到气相的甲醇),若以A表示冷凝液中水的质量分数,B表示冷凝液中甲醇的质量分数,则甲醇的转化率α(CH3OH)=________。
(3)一定条件下,发生反应③,原料气中![]() 和温度对CO2转化率影响的实验数据如图所示。
和温度对CO2转化率影响的实验数据如图所示。

结合图像,可得出CO2平衡转化率受外界条件影响的变化规律为:
a:________;
b:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在。Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:

(1)Cr2O72-中元素铬(Cr)的化合价为_____。
(2)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入![]() 溶液直至过量,可观察到的现象是____。
溶液直至过量,可观察到的现象是____。
(3)CrO42-和Cr2O72-在溶液中可相互转化:2CrO42-+2H+![]() Cr2O72-+H2O,室温下,初始浓度为1.0molL-1的Na2CrO4溶液中,c(Cr2O72-)随c(H+)的变化如图所示。
Cr2O72-+H2O,室温下,初始浓度为1.0molL-1的Na2CrO4溶液中,c(Cr2O72-)随c(H+)的变化如图所示。
①溶液酸性增大,CrO42-的平衡转化率_________。(填“增大”“减小”或“不变”)。
②根据A点数据,计算出该转化反应的平衡常数为___________。
③温度升高,溶液中CrO42-的平衡转化率减小,则该反应的ΔH____0(填“>、=、<”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】若用AG表示溶液的酸度,其表达式为![]() 。室温下,实验室里用0.1mol·L-1的盐酸滴定10mL0.1mol·L-1MOH溶液,滴定曲线如图所示。下列说法正确的是
。室温下,实验室里用0.1mol·L-1的盐酸滴定10mL0.1mol·L-1MOH溶液,滴定曲线如图所示。下列说法正确的是
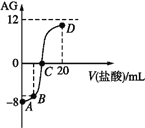
A. MOH为强碱
B. C点时加入盐酸的体积等于10mL
C. 若B点加入的盐酸体积为5mL,所得溶液中:c(M+)+2c(H+)=c(MOH)+2c(OH-)
D. 滴定过程中从A点到D点溶液中水的电离程度:A<B<C<D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A.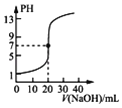 表示0.100 0 molL﹣1 NaOH溶液滴定20.00 mL 0.100 0 molL﹣1醋酸溶液的滴定曲线
表示0.100 0 molL﹣1 NaOH溶液滴定20.00 mL 0.100 0 molL﹣1醋酸溶液的滴定曲线
B.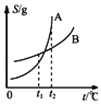 表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数ω(A)>ω(B)
表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数ω(A)>ω(B)
C.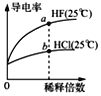 由图可知,a点Kw的数值比b点Kw的数值大
由图可知,a点Kw的数值比b点Kw的数值大
D.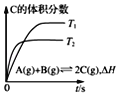 表示在相同的密闭容器中,不同温度下的反应,该反应的△H<0
表示在相同的密闭容器中,不同温度下的反应,该反应的△H<0
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个体积为2L的密闭容器中,高温下发生反应:C(s)+H2O(g)![]() CO(g)+H2(g),其中,H2O、CO的物质的量随时间的变化曲线如下图所示。
CO(g)+H2(g),其中,H2O、CO的物质的量随时间的变化曲线如下图所示。
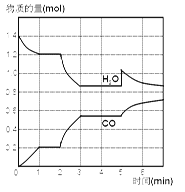
(1)写出上述反应的平衡常数表达式K=______。
(2)计算第1min内v(H2O)=_______。
(3)反应处于平衡状态的时间段是_______。
(4)若反应进行至2min时,改变了温度,使曲线发生了如下图所示的变化,则温度是____,(填“升高、降低、不变”),正反应是_____(填“吸热、放热”)反应。
(5)反应至5min时,若也只改变了某一个条件,使曲线发生如上图所示的变化,该条件可能是下述中的____(填写编号)。
①增加了CO; ②增加了水蒸气; ③加了催化剂; ④扩大了容器体积。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com