
科目: 来源: 题型:
【题目】用0.1000mol·L-1NaOH溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是
A. 盛装待测液的锥形瓶用蒸馏水洗过,没用待测液润洗
B. 酸式滴定管在使用前未用待测液盐酸润洗
C. 滴定前碱式滴定管尖嘴中有气泡,滴定后气泡消失
D. 滴定前读数平视,滴定终点读数时俯视碱式滴定管的刻度
查看答案和解析>>
科目: 来源: 题型:
【题目】(1) A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
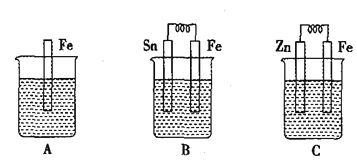
①B中Sn极的电极反应式为__________,Sn极附近溶液的pH_____(填“增大”、“减小”或“不变”)。
②C中总反应离子方程式为_____________,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是______(填“a”或“b”)电极,该极的电极反应是_______。
②电池工作一段时间后电解质溶液的pH____(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】用惰性电极电解法制备硼酸[H3BO3或B(OH) 3]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。下列有关说法正确的是( )
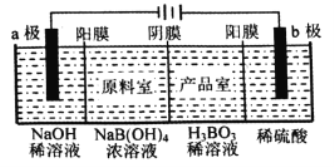
A. 阴极与阳极产生的气体体积比为1:2 B. b极的电极反应式为2H2O-2eˉ=O2↑+4H+
C. 产品室中发生的反应是B(OH)3+OHˉ=B(OH)4ˉ D. 每增加1 mol H3BO3产品,NaOH溶液增重22g
查看答案和解析>>
科目: 来源: 题型:
【题目】R、X、Y和Z是四种元素,其常见化合价均为+2价,且X2+与单质R不反应,X2++Z=X+Z2+,Y+Z2+=Y2++Z。这四种离子被还原成0价时,表现的氧化性强弱顺序为( )
A.R2+>X2+>Z2+>Y2+B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+D.Z2+>X2+>R2+>Y2+
查看答案和解析>>
科目: 来源: 题型:
【题目】(选用)CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-=2CuI↓+I2 而得到。如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI一淀粉溶液中阳极周围变蓝色,则下列说法正确的是

A.若a极变红,则在Pt电极上:2I--2e-=I2碘遇淀粉变蓝
B.若b极变红,在Pt电极上:4OH--4e-=2H2O+O2,O2将I-氧化为I2,碘遇淀粉变蓝
C.若a极变红,在Cu电极上:开始Cu+I--e-=CuI,一段时间后2I--2e-=I2,碘遇淀粉变蓝
D.若b极变红,在Cu极上:Cu-2e-=Cu2+,Cu2+显蓝色
查看答案和解析>>
科目: 来源: 题型:
【题目】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识回答:
(1)A为0.1molL-1的(NH4)2SO4溶液,用离子方程式表示该溶液显酸性的原因:___,在该溶液中各种离子浓度由大到小的顺序为___。
(2)B为0.1molL-1NaHCO3溶液,实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因:__(用离子方程式和必要的文字说明)。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入__,目的是___;若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为摇摆电池![]() 的工作原理图,在充放电过程中,
的工作原理图,在充放电过程中,![]() 在两极之间“摇来摇去”,其总反应为:
在两极之间“摇来摇去”,其总反应为:![]() ,下列有关说法正确的是
,下列有关说法正确的是
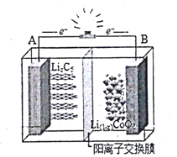
A.放电时,负极反应![]()
B.充电时,A极发生氧化反应
C.充电时,![]() 穿过隔离膜向B极移动
穿过隔离膜向B极移动
D.当B极失去xmol电子,电池消![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)请写出H2SO3的电离平衡常数K1的表达式:________________。
(2) 常温下,将体积为10mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_____后者(填“>”、“<”或“=”)。
(3)一定条件下,冰醋酸加水稀释过程中溶液导电能力I随加水体积V变化曲线如右图所示,则a、b、c三点溶液醋酸的电离程度由大到小为____________________。
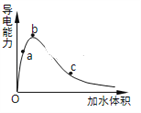
(4)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为___________。
(5)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是_____(填序号)。
(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用0.2000mol/L的NaOH溶液滴定25.00mL某未知浓度的盐酸(指示剂为酚酞),滴定结果如下:
第一次 | 第二次 | |
NaOH起始读数 | 0.10mL | 0.30mL |
NaOH终点读数 | 18.60mL | 18.00mL |
(1)根据以上数据可以计算出盐酸的物质的量浓度为__________mol/L。
(2)达到滴定终点的标志是___________。
(3)该同学的实验操作如下:
A.用酸式滴定管移取25.00mL的稀盐酸于锥形瓶中,滴加几滴酚酞试液;
B.用待测的稀盐酸润洗酸式滴定管;
C.检查滴定管是否漏水;
D.用蒸馏水洗干净滴定管;
E.另取锥形瓶,重复操作一次;
F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管至“0”刻度以上2cm,再把碱式滴定管固定好,调节液面至“0”刻度以下;
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶至滴定终点,记下滴定管液面所在刻度。
滴定操作的正确顺序是(用序号表示):C;_____;_____;A;C;D;F;G;E。
(4)实验操作G中在锥形瓶下垫一张白纸的作用_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,常温下通电5 min后,发现铜电极的质量增加,试回答:
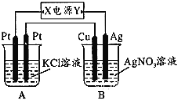
①电源电极X的名称为________(填“正极”或“负极”)。
②电解池B中阳极的电极反应式是________。
③若KCl溶液的体积是200 mL,则当铜电极的质量增加2.16g时A中溶液的pH=_____(忽略电解前后溶液体积的变化),若要使电解后的溶液恢复到与电解前完全相同的状态,则应加入____________(填物质的种类及数量)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com