
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.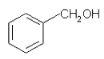 与
与![]() 含有相同的官能团,互为同系物
含有相同的官能团,互为同系物
B.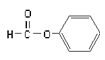 属于醛类,官能团为-CHO
属于醛类,官能团为-CHO
C.![]() 的名称为:2-乙基-1-丁烯
的名称为:2-乙基-1-丁烯
D.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有8种
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化钇主要用于制造微波磁性材料、军工材料、光学玻璃和显像管涂料等。工业上通过如下工艺流程用钇矿石(Y2 FeBe2 Si2O10,Y的化合价为+3)制取氧化钇。
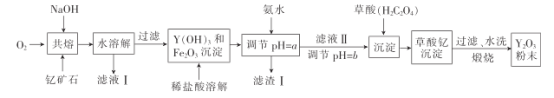
已知:i.铍和铝处于元素周期表的对角线位置,化学性质相似;
ii.Fe3+、Y3+形成氢氧化物沉淀时的pH如下表:
离子 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe3+ | 2.1 | 3.1 |
Y3+ | 6.0 | 8.3 |
(1)用氧化物的形式表示Y2 FeBe2 Si2O10为___, 钇矿石在熔融前要粉碎,目的是___。
(2)共熔时通人氧气的作用是_________。
(3)滤液I中溶质的主要成分是___ ( 假设钇矿石恰好与NaOH完全反应)。
(4)用氨水调节pH=a时,a的取值范围是_____,设计实验证明滤渣I沉淀完全: _______________。
(5)煅烧草酸钇时发生分解反应,其固体产物为氧化钇,气体产物能使澄清石灰水变浑浊。写出草酸钇[Y2(C2O4)3·nH2O]煅烧的化学方程式:_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知下列数据:
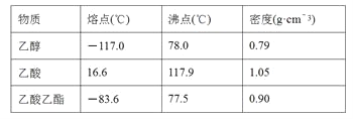
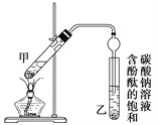
某学生在实验室制取乙酸乙酯的主要步骤如下:
①配制2 mL浓硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯,洗涤、干燥。
(1)配制①中混合溶液的方法为____________;反应中浓硫酸的作用是________________;写出制取乙酸乙酯的化学方程式:____________。
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)_________。
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇
C.减少乙酸乙酯的溶解 D.加速酯的生成,提高其产率
(3)步骤②中需要小火均匀加热,其主要理由是_______;步骤③所观察到的现象是_________;欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器有________;分离时,乙酸乙酯应从仪器________________(填“下口放”或“上口倒”)出。
(4)该同学反复实验,得出乙醇与乙酸的用量和得到的乙酸乙酯生成量如下表:
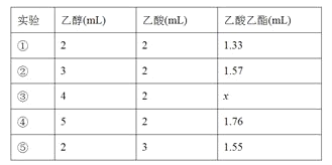
表中数据x的范围是__________________;实验①②⑤探究的是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】环丁基甲酸是有机合成中一种有用的中间体。某研究小组以丙烯醛为原料,设计了如下路线合成环丁基甲酸。


请回答:
(1)化合物C的结构简式是 __________________。
(2)下列说法中不正确的是__________________ 。
A.化合物A能与NaHCO3溶液反应
B.化合物B和C能形成高聚物
C.化合物G的化学式为C6H8O4
D.1 mol化合物B与足量金属钠反应能生成1 mol氢气
(3)写出D + E → F的化学方程式:__________________。
(4)环丁基甲酸与苯酚反应生成一种酯X,写出化合物X满足下列条件的所有同分异构体的结构
简式:__________________
① 能使FeCl3溶液变紫色;
② 含有丙烯醛中所有的官能团;
③ 1H-NMR谱显示分子中含有5种不同化学环境的氢原子。
(5) 以1,3-丁二烯和E为原料可制备环戊基甲酸(![]() ),请你选用必要试剂,设计该合成路线。__________________
),请你选用必要试剂,设计该合成路线。__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)如图是甲烷燃料电池原理示意图,回答下列问题:
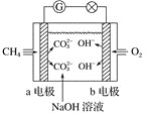
①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为__________________。
②电池工作一段时间后电解质溶液的pH________(填“增大”、“减小”或“不变”)。
(2)熔融盐燃料电池具有很高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650 ℃下工作的燃料电池。请完成有关的电池反应式:
负极反应式:2CO+2![]() -4e-===4CO2;
-4e-===4CO2;
正极反应式:__________________________________________;
总电池反应式:_______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】取A、B两份物质的量浓度相等的NaOH溶液,体积均为50 mL,分别向其中通入一定量的CO2后,再分别稀释到100 mL,在稀释后的溶液中分别逐滴加0.1 mol/L的盐酸,产生的CO2的体积(标准状况)与所加盐酸的体积关系如图所示:

(1)原NaOH溶液的物质的量浓度_________________。
(2)B份混合溶液与盐酸反应产生气体的最大体积为________mL(标准状况)。
查看答案和解析>>
科目: 来源: 题型:
【题目】叠氮化钠(NaN3)是汽车安全气囊最理想的气体发生剂原料。下面是工业水合肼法制备叠氮
化钠的工艺流程:

已知 NaN3 能与 AgNO3 反应生成白色难溶于水的 AgN3;Ag2CrO4 呈红色,可溶于水。有关物质的物理性质如下表:
熔点℃ | 沸点℃ | 溶解性 | |
CH3OH | -9 | 64.7 | 与水互溶 |
水合肼(N2H4H2O) | 2 | 113.5 | 与水、醇互溶,不溶于乙醚和氯仿 |
亚硝酸甲酯(CH3ONO) | -17 | -12 | 难溶于水,可溶于乙醇、乙醚 |
NaN3 | 275 | 300 | 易溶于水,难溶于乙醇 |
请回答:
(1)步骤Ⅰ中NaNO2 与稀硫酸发生副反应生成两种气体(其中一种气体在空气中可以转化为另一种气体)的离子方程式为_____;步骤Ⅱ中生成 NaN3 的化学方程式为_____
(2)实验室模拟步骤Ⅱ实验装置如图(装置中冷却水省略,下同):根据实验发现温度在 20℃左右反应的选择性和转化率最高,但是该反应属于放热反应,因此需要采取的措施是_____。
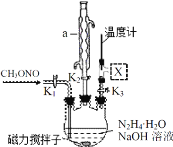
(3)步骤Ⅱ、Ⅲ中制备叠氮化钠并对溶液 A 进行蒸馏的合理操作顺序是_____。
①打开 K1、K2,关闭 K3 ②打开 K3 ③加热 ④关闭 K1、K2
(4)步骤Ⅳ对溶液B 加热蒸发至溶液体积的 1/3,NaN3 结晶析出。
①步骤Ⅴ最好选用_____洗涤晶体。
A.水 B.乙醇 C.乙醚
②沉淀滴定法测定产品纯度,是以淡黄色 K2CrO4 溶液作指示剂,将 AgNO3 标准溶液滴入样品溶液, 滴定终点现象为_________。AgNO3 溶液要装在_____滴定管里进行滴定。下列说法正确的是_____。
A.滴定管和移液管管尖不可接触锥形瓶内壁
B.滴定时滴液速度应先快后慢,接近终点时一滴一摇
C.滴定过程中可用蒸馏水将锥形瓶壁上粘附的溶液冲下
D.若发现滴液过量,可回滴样品溶液
E.若未等滴定管液面稳定就读数会导致测定结果偏高
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,用0.10 mol·L-1KOH溶液滴定10.00 mL 0.10 mol·L-1H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:
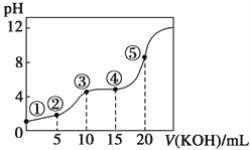
(1)点①所示溶液中,Kw=__________。
(2)点②所示溶液中的电荷守恒式为______________________________________。
(3)点③所示溶液中存在________种平衡。
(4)点④所示溶液中的物料守恒式为0.10 mol·L-1=___________________________。
(5)点⑤所示溶液中各离子浓度的大小顺序为________________________________。
(6)上述5点所示溶液中,水的电离程度最大的是_______,最小的是________(用序号回答)。
查看答案和解析>>
科目: 来源: 题型:
【题目】10℃时加热NaHCO3饱和溶液,测得该溶液的pH随温度的升高发生如下变化:

甲同学认为,该溶液pH升高的原因是随温度的升高HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为____________________。
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度________(填“大于”或“小于”)NaHCO3,该分解反应的化学方程式为_______________。
丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的BaCl2溶液,若产生沉淀,则乙判断正确。为什么?能不能选用Ba(OH)2溶液?_____________________________________________。
(2)将加热后的溶液冷却到10 ℃,若溶液的pH______(填“高于”、“低于”或“等于”)8.3,则__________(填“甲”或“乙”)判断正确。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)醋酸可通过分子间氢键双聚形成八元环,画出该结构_____。(以 O…H—O 表示氢键)
(2)已知碳化镁 Mg2C3可与水反应生成丙炔,画出 Mg2C3的电子式_____。
(3)工业上,异丙苯主要通过苯与丙烯在无水三氯化铝催化下反应获得,写出该反应方程式_____。
(4)将乙酸乙酯与H218O混合后,加入硫酸作催化剂,乙酸乙酯在加热条件下将发生水解反应,写出产物中不含18O的物质的结构简式_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com