
科目: 来源: 题型:
【题目】已知锌能溶解在NaOH溶液中,产生H2。某同学据此设计了测定镀锌铁皮镀层厚度的实验方案,将单侧面积为S、质量为m1的镀锌铁皮与石墨用导线相连,放入6 mol·L-1NaOH溶液中,当石墨棒上不再有气泡产生时,取出铁片用水冲洗、烘干后称量,得质量为m2。下列说法正确的是(双选)( )
A.设锌镀层单侧厚度为h,锌的密度为ρ,则![]() =h
=h
B.锌电极上发生还原反应
C.锌和石墨形成原电池,外电路中电流从锌流向石墨
D.当石墨不再产生气泡时,应立即取出铁皮
查看答案和解析>>
科目: 来源: 题型:
【题目】为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中。试回答:
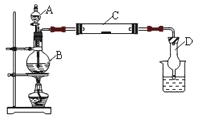
(1)怎样检验装置的气密性_____________________________________;
(2)若C中为淀粉KI试纸,实验片刻后C中可以观察到的实验现象为_______;写出B中发生反应的离子方程式_________________________________________________。
(3)若C中的淀粉KI试纸实验一段时间后又变为无色,原因是__________________。
(4)D的作用是_______________。烧杯中加入的是_____________________。
(5)若实验室暂时无二氧化锰,仍用此装置制取氯气,选用___________药品替代。若实验室暂时无浓盐酸,仍用此装置制取氯气,选用__________________药品替代。
查看答案和解析>>
科目: 来源: 题型:
【题目】用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶液于一洁净的锥形瓶中,然后用0.2000mol·L-1的氢氧化钠溶液(指示剂为酚酞)滴定。滴定结果如下所示:
NaOH溶液起始读数 | NaOH终点读数 | |
第一次 | 0.10mL | 18.60mL |
第二次 | 0.30mL | 19.00mL |
(1)准确配制0.2000mol·L-1的氢氧化钠溶液250mL,需要的主要仪器除量筒、烧杯、玻璃棒外,还必须用到的玻璃仪器有___。
(2)根据以上数据可以计算出盐酸的物质的量浓度为___ mol·L-1。(保留4位有效数字)
(3)用0.2000mol·L-1标准氢氧化钠溶液滴定待测盐酸溶液,滴定时左手控制碱式滴定管的玻璃球,右手不停摇动锥形瓶,眼睛注视___,直到滴定终点。
(4)达到滴定终点的标志是___。
(5)以下操作造成测定结果偏高的原因可能是___ (填字母代号)。
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其他操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为(C7H5NO)。
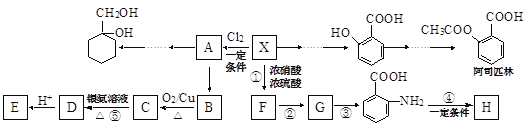
已知:![]() (苯胺,易被氧化)
(苯胺,易被氧化)
完成下列填空:
(1)X的结构简式是______,反应⑤的类型是_________。
(2)反应②③两步能否互换_______(填“能”或“不能”),理由是______。
(3)反应④的化学方程式是____________。
(4)检验B是否完全转化为C的方法是______(选填编号)。
a.定量测熔点 b.定性酸性高锰酸钾溶液
c.定量银氨溶液 d.定性新制氢氧化铜
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)![]() CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图所示。
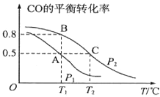
①A、B两点对应的压强大小关系是PA___PB(填“>、<、=”)。
②A、B、C三点的平衡常数KA,KB,KC的大小关系是___。
③下列叙述能说明上述反应能达到化学平衡状态的是___(填代号)。
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
(2)在P1压强、T1℃时,该反应的平衡常数K=___。
(3)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)___v(逆)(填“>、<或=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计了一组电化学装置如图所示,其中乙装置中X为阳离子交换膜,甲醇(CH3OH)具有可燃性。

根据要求回答相关问题:
(1)写出装置甲中负极的电极反应式:___。
(2)装置乙中石墨电极(C)的电极反应式为:___。
(3)当装置甲中消耗0.05molO2时,丙装置中阳极产生气体的体积___L(标况下);
(4)装置乙中溶液的pH为___(溶液体积为200mL不变)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气是一种常用的化工原料,应用十分广泛。以H2合成尿素CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)=2NH3(g) △H1=-92.4kJ·mol-1
②NH3(g)+![]() CO2(g)=
CO2(g)=![]() NH2CO2NH4(s) △H2=-79.7kJ·mol-1
NH2CO2NH4(s) △H2=-79.7kJ·mol-1
③NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l) △H3=+72.5kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】在2L密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间变化如下表:
2NO2(g)体系中,n(NO)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=_____。已知:K(300℃)>K(350℃),则该反应正反应是_________热反应。升高温度,正反应速率_______(填“增大”、“减小”或“不变”)。
(2)下图中表示NO2的变化的曲线是____。用O2表示从0~2 s内该反应的平均速率v(O2)=______。
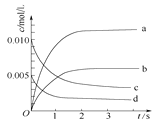
(3)能说明该反应已达到平衡状态的是__________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是_________。
A.及时分离出NO2气体 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
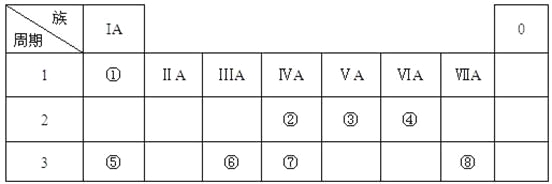
(1)④、⑤、⑥的原子半径由大到小的顺序为______________。
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是__________。
(3)③的气态氢化物的电子式_____。
(4)⑤的最高价氧化物对应水化物的溶液与单质⑥、单质⑧分别反应的离子方程式___、____。
(5)单质①在单质⑧中燃烧,火焰为__________色。
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的H+和OH-)Na+、NH4+、SO42-、CO32-、NO3-。取200mL该溶液,分为等体积的二份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL。实验2:第二份先加入足量的盐酸,无现象,再加足量的BaCl2溶液,得固体2.33克。下列说法正确的是( )
A.该溶液中不一定含有Na+
B.该溶液中肯定含有NH4+、SO42-、CO32-、NO3-
C.该溶液中一定不含NO3-
D.该溶液中一定含Na+,且c(Na+)≥0.1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com