
科目: 来源: 题型:
【题目】已知电离平衡常数:H2CO3>HClO>HCO3-,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是( )
A.常温下,中性溶液中,![]() 、
、![]() 、
、![]() 、
、![]() 能大量共存
能大量共存
B.向含有![]() 的溶液中通入
的溶液中通入![]() 充分反应:4Fe2++2I-+3Cl2=4Fe3++6Cl-+I2
充分反应:4Fe2++2I-+3Cl2=4Fe3++6Cl-+I2
C.向NaClO溶液中通入少量二氧化碳的离子方程式:ClO-+CO2+H2O=HClO+HCO3-
D.向![]() 溶液中滴加少量氯水,再加入
溶液中滴加少量氯水,再加入![]() 溶液振荡,静置,有机层呈橙色
溶液振荡,静置,有机层呈橙色
查看答案和解析>>
科目: 来源: 题型:
【题目】amolFeS与bmolFe3O4投入到VL cmol/L的硝酸溶液中恰好完全反应,假设只产生NO气体。所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为
A.![]()
B.(a+3b)mol
C.![]()
D.(cV-3a-9b)mol
查看答案和解析>>
科目: 来源: 题型:
【题目】咖啡酸具有止血、镇咳、祛痰等疗效,其结构简式如图,下列有关咖啡酸的说法中,不正确的是
![]()
A.咖啡酸可以发生还原、取代、加聚等反应
B.咖啡酸与FeCl3溶液可以发生显色反应
C.1mol咖啡酸最多能与4molBr2反应
D.1 mol咖啡酸最多能消耗3 mol的NaHCO3
查看答案和解析>>
科目: 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,以下说法正确的是
A.2NA个HCl分子与44.8 L H2和Cl2的混合气体所含的原子数目均为4NA。
B.32gCu将足量浓、稀硝酸分别还原为NO2和NO,浓、稀硝酸得到的电子数均为NA。
C.物质的量浓度均为1mol/L的NaCl和MgCl2混合溶液中,含有Cl―的数目为3NA。
D.1mol D318O+(其中D代表![]() )中含有的中子数为10 NA。
)中含有的中子数为10 NA。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学用语表示正确的是
①CSO的电子式:![]()
②对硝基苯酚的结构简式:![]()
③Cl-的结构示意图: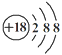
④苯分子的比例模型:
⑤葡萄糖的实验式:CH2O
⑥原子核内有20个中子的氯原子:![]()
⑦HCO3-的水解方程式为:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
A.①④⑤B.①②③④⑤C.③⑤⑥⑦D.全部正确
查看答案和解析>>
科目: 来源: 题型:
【题目】炔烃的偶联反应在开发新型发光材料、超分子等领域有重要研究价值。乙炔发生的偶联反应为 2CH≡CH ![]() CH≡CC≡CH+H2。乙炔偶联反应过程中能量变化如图甲中曲线Ⅰ所示,曲线Ⅱ为改变某一条件的能量变化。下列说法不正确的是( )
CH≡CC≡CH+H2。乙炔偶联反应过程中能量变化如图甲中曲线Ⅰ所示,曲线Ⅱ为改变某一条件的能量变化。下列说法不正确的是( )
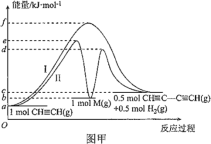
A.曲线Ⅰ,反应物的总键能大于生成物的总键能
B.曲线Ⅱ改变的条件是加入了催化剂
C.曲线Ⅱ对应条件下,第一步反应的 ΔH=+(b-a)kJ·mol-1
D.曲线Ⅱ对应条件下,决定总反应速率的大小是第二步反应
查看答案和解析>>
科目: 来源: 题型:
【题目】用含少量铁的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作:
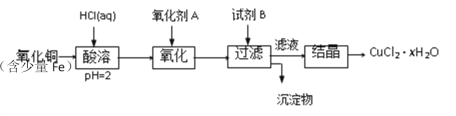
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,Cu2+却不水解。
(1)加热酸溶过程中发生反应的离子方程式有:______
(2)氧化剂A可选用_______(填编号,下同)
①Cl2 ②KMnO4 ③HNO3
(3)要得到较纯的产品,试剂B可选用_______
①NaOH ②FeO ③CuO
(4)试剂B的作用是_______
①提高溶液的pH ②降低溶液的pH
③使Fe3+完全沉淀 ④使Cu2+完全沉淀
(5)从滤液经过结晶得到氯化铜晶体的方法是___________(按实验先后顺序填编号)
①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(6)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止、冷却、称量所得无水CuCl2的质量为n g。
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g。
试评价上述两种实验方案,其中正确的方案是______,据此计算得x = ______________(用含m、n的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:25℃时,0.1000mol·L-lCH3COOH溶液中CH3COOH的电离度(×100%)约为1%。该温度下,用0.1000mol·L-l氨水滴定10.00mL0.1000mol·L-lCH3COOH溶液,溶液的pH与溶液的导电能力(I)的关系如图所示。下列说法中正确的是( )
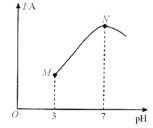
A.M点→N点,水的电离程度逐渐增大
B.25℃时,CH3COOH 的电离常数约为1.0×10-2
C.N点溶液中,c(CH3COO-)>c(NH4+)
D.当滴入20 mL氨水时,溶液中c(CH3COO-)>c(NH4+)
查看答案和解析>>
科目: 来源: 题型:
【题目】碳是一种极其重要的元素,工业上,生活中到处可见。
(1)碳原子核外有________种能量不同的电子,这些电子占据了______个纺锤形轨道。
(2)下列方法可以比较碳与硫的非金属性强弱的是__________
a.比较原子最外层电子数多少 b.比较其最高价氧化物对应水化物的酸性
c.比较气态氢化物的稳定性 d.比较单质的熔沸点高低
(3)煤的气化是煤高效洁净利用的方向之一。在一定温度下的某容积可变的密闭容器中 建立下列化学平衡:C(s)+H2O(g)![]() CO(g)+H2(g)-Q,可认定该可逆反应在一定条件下已达到化学平衡状态的是_____(选填序号)。
CO(g)+H2(g)-Q,可认定该可逆反应在一定条件下已达到化学平衡状态的是_____(选填序号)。
a.体系的压强不再发生变化 b.v正(CO)=v逆(H2O)
c.生成n molCO的同时生成n mol H2 d.1mol H-H键断裂同时断裂2mol H-O键
(4)若上述化学平衡状态从正反应开始建立,达到平衡后,给平衡体系加压(缩小体积),则容器内气体的平均相对分子质量将______(填写不变、变小、变大、无法确定)。若工业上以此方法生产水煤气,提高产率的措施为____。(写出两条措施)
(5)空气中的CO2浓度增大,会导致温室效应,有人提出将CO2通过管道输送到海底,这可减缓空气中CO2浓度的增加。但长期下去,海水的酸性也将增强,破坏海洋的生态系统。请你结合CO2的性质,从平衡角度分析酸性增强原因 _____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮气是制备含氮化合物的一种重要物质,而含氮化合物的用途广泛,两个常见的固氮反应的平衡常数的对数值(lgK)与温度的关系如图所示:①N2+3H22NH3 ②N2+O22NO;根据图中的数据判断下列说法正确的是( )
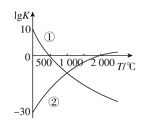
A.反应①和②均为放热反应
B.升高温度,反应①的反应速率减小
C.在1000℃时,反应①和反应②体系中N2的浓度一定相等
D.在标准状况下,利用反应①固氮和利用反应②固氮反应程度相差很大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com