
科目: 来源: 题型:
【题目】氯氧化铋(BiOCl)常用于电子设备等领域,BiOCl难溶于水,它是BiCl3的水解产物。以铋的废料(主要含铋的化合物,含少量铜、铅、锌的硫酸盐及Cu2S和Fe2O3等)为原料生产高纯度BiOCl的工艺流程如下:
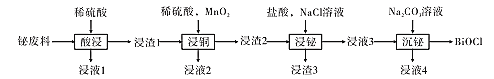
请回答下列问题:
(1)在浸液1中加入过量的锌,过滤,将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥得结晶水合物M,M的摩尔质量为287 g·mol-1,M为 ___(填化学式)。
(2)已知:浸液2呈蓝色,浸渣2含有少量硫单质。“浸铜”中MnO2的作用是____(用离子方程式表示)。
(3)“浸铋”中,铋的浸出率与温度关系如图所示:
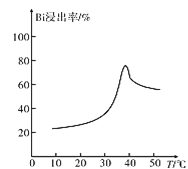
在高于40℃左右时“铋浸出率”开始下降,其主要因素可能是____(从两个角度分析)。
(4)在室温和液固比固定的条件下,c(HCl)=1.0mol·L-1时,铋的浸出率与溶液中c(Cl-)的关系如图所示。“浸铋”操作中,加入NaCl的目的是____。
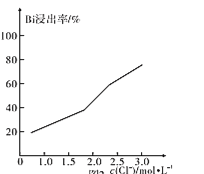
(5)浸液3中主要溶质是BiCl3,“沉铋”过程中,有气体放出。“沉铋”的主要化学反应的方程式为____。从绿色化学角度看,浸液4可以用于____(填“酸浸”、“浸铜”或“浸铋”)。
(6)测定产品的纯度:取mg充分洗涤并干燥后的产品,溶于稍过量的浓硝酸中,加水稀释到100.0mL,取20.0mL于烧杯中,用cmol·L-1的AgNO3标准溶液滴定至终点(用Na2CrO4,作指示剂),消耗AgNO3标准溶液VmL,则产品中BiOCl的质量分数为____%(用含m、c、V的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】乙酸是非常重要的工业原料,其氯代物可由乙酸和氯气在催化剂的作用下制备。实验室模拟工业生产食品香精菠萝酯(![]() ) 的简易流程如下。
) 的简易流程如下。
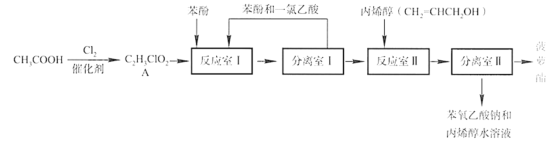
(1)菠萝酯的核磁共振氢谱中有__________个吸收峰。
(2)A中官能团的名称是__________。
(3)根据流程写出下列反应的化学方程式:
i.制备A: __________;该反应属于__________反应。
ii.反应室I中的反应: __________。
(4)分离室II的操作是用饱和Na2CO3溶液洗涤,而不用NaOH洗涤的原因是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】聚酯纤维(PET) 结构简式为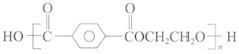 ,其性能优良、应用广泛,产量占合成纤维总量的70%以上,合成原料主要来源于石油和煤的产品。
,其性能优良、应用广泛,产量占合成纤维总量的70%以上,合成原料主要来源于石油和煤的产品。
(1)请你用乙烯和对二甲苯为有机原料,设计该聚酯纤维合成线路: ___________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,无机试剂任选)。
(2)写出上述流程中发生缩聚反应的化学方程式: ___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】美国药物学家最近合成一种可能用于治疗高血压的有机物K,合成路线如下:
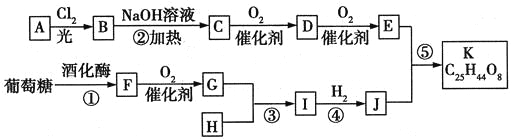
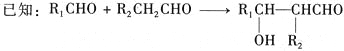
其中A属于碳氢化合物,其中碳的质量分数约为83.3%;E的核磁共振氢谱中只有2组吸收峰。H常温下呈气态,是室内装潢产生的主要污染物之一。G和H以1:3反应生成I。
试回答下列问题:
(1)A的分子式为:______________。
(2)写出下列物质的结构简式:D:____________;G:___________。
(3)反应①―⑤中属于取代反应的有___________。
(4)反应①的化学方程式为_______________;反应④的化学方程式为_________________。
(5)E有多种同分异构体,符合“既能发生银镜反应又能发生水解反应”条件的E的同分异构体有_______种,写出符合上述条件且核磁共振氢谱只有2组吸收峰的E的同分异构体的结构简式:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应[Cu(OH)2悬浊液用于检验反应产物]。
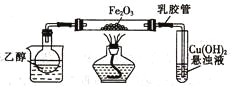
(1)组装好仪器后必须进行的操作是____________________。
(2)为快速得到乙醇气体,可采取的方法是_______________________;
若实验时小试管中的溶液已经开始发生倒吸,应采取的措施是_________(填字母)。
A.取下小试管 B.移去酒精灯 C.将导管从乳胶管中取下 D.以上都可以
(3)乙醇被氧化的产物是__________________(写结构式)。
(4)若M的成分为FexOy,用CO还原法定量测定其化学组成。称取a g M样品进行定量测定,实验装置和步骤如下:
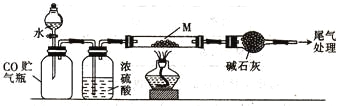
①组装仪器 ②点燃酒精灯 ③加入试剂 ④打开分液漏斗活塞 ⑤检查气密性 ⑥停止加热 ⑦关闭分液漏斗活塞 ⑧称重
ⅰ.正确的操作顺序是__________(填字母)。
a.①⑤④③②⑥⑦⑧ b.①③⑤④②⑦⑥⑧
c.①⑤③④②⑥⑦⑧ d.①③⑤②④⑥⑦⑧
ⅱ.尾气处理的方法是____________。若测得碱石灰增重b g,则x:y=______(用含有a、b的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、R、D都是周期表中前四周期的元素,它们的原子系数依次增大。其中A元素基态原子第一电离能比B元素基态原子的第一电离能大,B的基态原子的L层、R基态原子的M层均有2个单电子,D是第Ⅷ族中原子序数最小的元素。
(1)写出基态D原子的电子排布式__________。
(2)已知高纯度R的单质在现代信息技术与新能源开发中具有极为重要的地位。工业上生产高纯度R的单质过程如下:
![]()
写出过程③的反应方程式___________,已知RHCl3的沸点是31.5oC,则该物质的晶体类型是__________,中心原子的轨道杂化类型为__________,该物质的空间构型是______。
(3)A的第一电离能比B的第一电离能大的原因是_________,A、B两元素分别与R形成的共价键中,极性较强的是________。A、B两元素间能形成多种二元化合物,其中与A3-互为等电子体的物质的化学式为_______。
(4)已知D单质的晶胞如图所示,则晶体中D原子的配位数为______,一个D的晶胞质量为____,已知D原子半径为r pm,则该晶胞的空间利用率为_____________ (写出计算过程)。
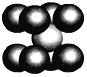
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2和CH4是两种主要的温室气体,通过CH4和CO2反应制造更高价值的化学品是目前的研究目标。
(1)250℃时,以镍合金为催化剂,向4L容器中通入6mol CO2、6mol CH4,发生如下反应:
CO2(g) + CH4(g)![]() 2CO(g) + 2H2(g)。平衡体系中各组分的体积分数如下表:
2CO(g) + 2H2(g)。平衡体系中各组分的体积分数如下表:
物质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
①此温度下该反应的平衡常数K=________________。
②已知:CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) △H=-890.3kJmol-1,CO(g) + H2O(g) = CO2(g) + H2(g) △H=+2.8kJmol-1,2CO(g) + O2(g) = 2CO2(g) △H=-566.0kJmol-1,反应CO2(g) + CH4(g)![]() 2CO(g) + 2H2(g)的△H=_______。
2CO(g) + 2H2(g)的△H=_______。
(2)以二氧化钛表面覆盖的Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成为乙酸。
①在不同温度下,催化剂的催化效率与乙酸的生成速率的变化关系如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是_________。
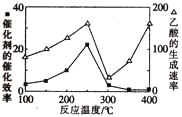
②为了提高该反应中CH4的转化率,可以采取的措施是__________________。
③将Cu2Al2O4溶解在稀硝酸中的离子方程式为___________________。
(3)以CO2为原料可以合成多种物质。
①聚碳酸酯是一种易降解的新型合成材料,它是由CO2加聚而成的。写出聚碳酸酯的结构简式:__________。
②以氢氧化钾水溶液作为电解质进行电解,CO2在铜电极上可转化为甲烷,电极反应式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】MnO2又名黑锰矿,主要用于生产优质软磁铁氧体。MnO2的合成方法按制备工艺中所用原料的不同,分为固相合成和液相合成。已知:MnO2不溶于水,其中锰的价态有+2价,也可能有+3价和+4价。请回答下列问题:
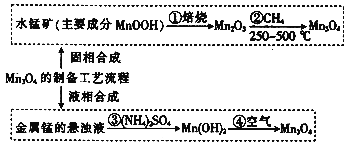
(1)若Mn3O4中锰的价态看作由+2和+4价组成,写出它由氧化物形成的表达式:_____
(2)MnOOH中锰的价态为________价,写出②的化学方程式:____;碱性锌锰干电池的电池反应为:Zn+2MnO2 + 2H2O=Zn(OH)2 + 2MnOOH,写出该电池正极的电极反应式______
(3)将(NH4)2SO4溶于水使锰的悬浊液显酸性,随即缓慢地产生气泡,试用相应的离子方程式解释原因____________。过滤出的Mn(OH)2需要洗涤,简要说明洗涤沉淀的操作过程:________。
(4)若③中收集到672mL(标准状况下)的H2,则理论上可以得到_________g Mn3O4。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了研究有机物A的组成与结构,某同学进行如下实验。
i.将9.0gA 在足量氧气中充分燃烧,并使其产物依次缓缓通过足量的浓硫酸和碱石灰,发现两者分别增重5.4g和13.2g。
ii.通过质谱法测得其相对分子质量为90。
ili.通过红外光谱法测得A中含有—OH和—COOH。
请回答下列问题。
(1)9.0gA完全燃烧生成水的物质的量是____________mol。
(2)A的实验式是____________。
(3)A的分子式是____________。
(4)在一定条件下,若两个A分子可以反应得到一个六元环的分子,则A的结构简式是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】肉桂酸是合成香料、化妆品、医药、浆料和感光树脂等的重要原料,其结构简式是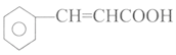 。
。
I.写出肉桂酸的反式结构: __________。
II.实验室可用下列反应制取肉桂酸。
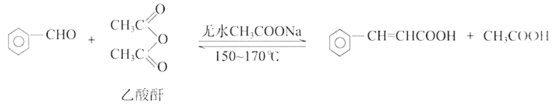
已知药品的相关数据如下:
苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
溶解度(25℃,g/100g 水) | 0.3 | 遇水水解 | 0.04 | 互溶 |
相对分子质量 | 106 | 102 | 148 | 60 |
实验步骤如下:
第一步合成:向烧瓶中依次加入研细的无水醋酸钠、5.3g 苯甲醛和6.0g乙酸酐,振荡使之混合均匀。在150~ 170℃加热1小时,保持微沸状态。第二步粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,并进行下列操作:
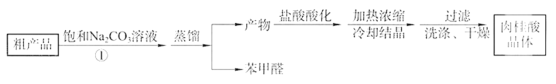
请回答下列问题。
(1)检验粗产品中含有苯甲醛的实验方案是:取粗产品于试管中,加水溶解,滴入NaOH溶液,将溶液调至碱性, _________。
(2)步骤①中肉桂酸与Na2CO3溶液反应的化学方程式是_________。
(3)若最后得到4.81g纯净的肉桂酸,则该反应中肉桂酸的产率是_________。
(4)符合下列条件的肉桂酸的同分异构体有_________种。
i.苯环上含有三个取代基;
ii.该同分异构体遇FeCl3显色且能发生银镜反应。
写出其中任意一种同分异构体的结构简式: _________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com