
科目: 来源: 题型:解答题
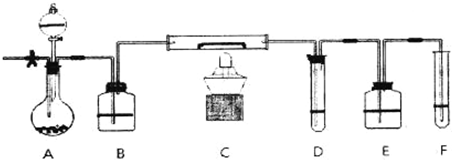
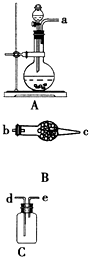 下列为实验室制取、干燥和收集氨气的装置.
下列为实验室制取、干燥和收集氨气的装置.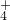 +OH-,NaOH使平衡向左移动
+OH-,NaOH使平衡向左移动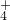 +OH-,NH4Cl使平衡向左移动
+OH-,NH4Cl使平衡向左移动 +OH-
+OH- NH3↑+H2O.
NH3↑+H2O.查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:单选题
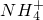 在一定条件下可被O2氧化,反应过程如下:下列叙述正确的是
在一定条件下可被O2氧化,反应过程如下:下列叙述正确的是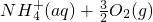 ═
═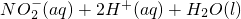 △H=-273kJ/mol
△H=-273kJ/mol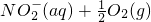 ═
═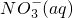 △H=-73kJ/mol.
△H=-73kJ/mol.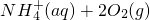 ═
═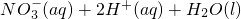 △H=-346 kJ/mol
△H=-346 kJ/mol查看答案和解析>>
科目: 来源: 题型:解答题
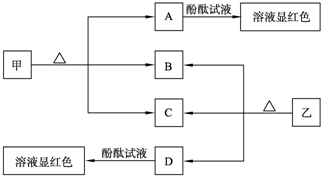
查看答案和解析>>
科目: 来源: 题型:单选题
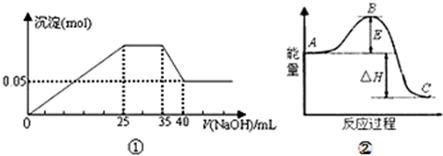
查看答案和解析>>
科目: 来源: 题型:解答题
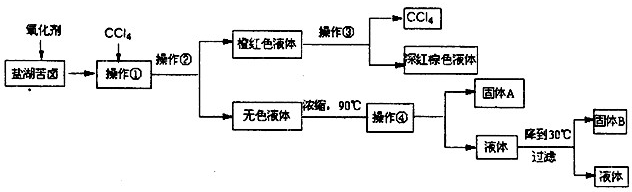
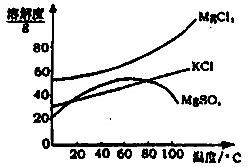
| 化学式 | BaCO3 | BaSO4 | Ca(OH)2 | MgCO3 | Mg(OH)2 |
| Ksp | 8.1×10一9 | 1.08×10一10 | 1.0×10一4 | 3.5×10一5 | 1.6×10一11 |
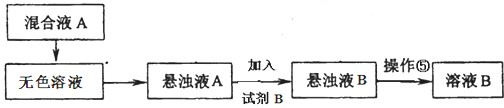
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 4NO+6H20;4NO+3O2+2H2O=4HNO3 设原混合气体中有x mol O2,最后容器中生成y mol HNO3,再向容器中注入一定量的H2O,得到溶液.
4NO+6H20;4NO+3O2+2H2O=4HNO3 设原混合气体中有x mol O2,最后容器中生成y mol HNO3,再向容器中注入一定量的H2O,得到溶液.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com