
科目:gzhx 来源: 题型:阅读理解
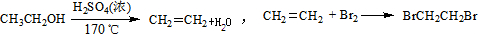
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
科目:gzhx 来源: 题型:阅读理解
 (2012•海南)实验室制备1,2-二溴乙烷的反应原理如下:
(2012•海南)实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
科目:gzhx 来源: 题型:阅读理解
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 浓硫酸 |
| 170摄氏度 |
| 加热 |
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
| 加热 |
| 加热 |
科目:gzhx 来源:2014届山西省晋中市高二下学期期末考试化学试卷(解析版) 题型:实验题
实验室制备1,2-二溴乙烷的反应原理如下:

可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
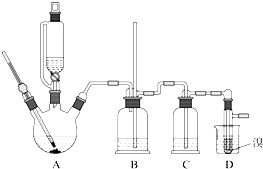
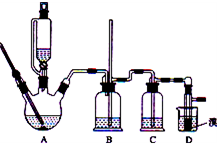
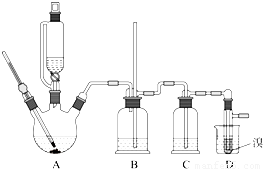
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:
|
|
乙醇 |
1,2-二溴乙烷 |
乙醚 |
|
状态 |
无色液体 |
无色液体 |
无色液体 |
|
密度/g · cm-3 |
0.79 |
2.2 |
0.71 |
|
沸点/℃ |
78.5 |
132 |
34.6 |
|
熔点/℃ |
一l30 |
9 |
-1l6 |
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是 ;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用 洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用 的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 。
科目:gzhx 来源:2015届江苏省徐州市高二上学期期末考试化学试卷(选修)(解析版) 题型:实验题
已知① CH3CH2OH CH2=CH2↑+H20
CH2=CH2↑+H20
CH2=CH2+Br2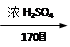 BrCH2—CH2Br
BrCH2—CH2Br
②乙醇、1,2-二溴乙烷、乙醚的有关物理性质如下表所示。
|
|
乙醇 |
1,2-二溴乙烷 |
乙醚 |
|
通常状况下的状态 |
无色液体 |
无色液体 |
无色液体 |
|
密度/g·cm-3 |
0.79 |
2.2 |
0.71 |
|
熔点/℃ |
-130 |
9 |
-116 |
|
沸点/℃ |
78.5 |
132 |
34.6 |
某化学小组拟用乙醇、溴等为原料在实验室制备少量的1,2一二溴乙烷,实验装置如右图所示(装置A中的加热部分的仪器装置省略没有画出)。

(1)仪器E的名称是 。
(2)仪器Ⅰ是漏斗,其左部的玻璃管的作 用是 (填字母)。
a.使漏斗中液体容易滴下
b.有利于吸收气体杂质
c.防止A中三颈烧瓶里的液体爆沸
(3)实验时,A中三颈烧瓶里放入几片碎瓷片的目的是 。加热反应过程中,三颈烧瓶里除生成乙烯外,还可能生成的有机副产物主要是 。
(4)反应过程中,若B中长玻璃导管(Ⅱ)里的液面上升,则说明可能是由于 (填“D中出现堵塞”或“C中杂质已除尽”)造成的。
(5)反应过程中,D中需用冷水冷却盛有液溴的试管,其主要目的是 。说明制备1,2-二溴乙烷的反应已经结束的实验现象是 。
科目:gzhx 来源:2014届江西省高二上学期期末考试化学试卷(解析版) 题型:实验题
(共16分)
Ⅰ实验室制备1,2-二溴乙烷的反应原理如下:
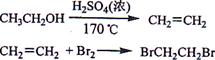
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
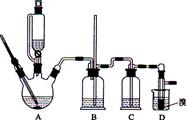
有关数据列表如下:
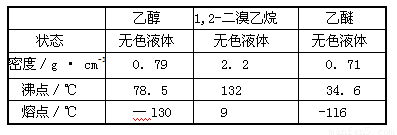
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)若产物中有少量副产物乙醚.可用 的方法除去;
(4)反应过程中应用冷水冷却装置D,其主要目的是避免溴大量挥发,但又不能过度冷却(如用冰水),其原因是 。
Ⅱ.已知烯烃与苯在一定条件下反应生成芳香烃。如:

丙烯是三大合成材料的基本原料,可用于合成应用广泛的DAP树脂单体和双酚等有机物,具有重要的工业用途。
(1)写出丙烯在一定条件下发生聚合反应的化学方程式 。
(2)丙烯在乙酸作用下与O2反应生成有机物A,其蒸气密度是相同状况下甲烷密度的6.25倍,元素的质量分数为:碳60%、氧32%。A的分子式为 。
(3)丙烯与苯在一定条件下反应可生成D、E、F等多种芳香烃。红外光谱、核磁共振是研究有机物结构的重要方法,根据下列数据,画出D、E的结构。
D:元素组成:C89.94%、H10.06%;1H核磁共振有5个信号。
E:元素组成:C88.82%、H11.18%;1H核磁共振有3个信号。
F:元素组成:C88.82%、H11.18%;1H核磁共振有4个信号。
D: 。 E: 。
科目:gzhx 来源:2012-2013学年江西省高安中学高二上学期期末考试化学试卷(带解析) 题型:实验题
(共16分)
Ⅰ实验室制备1,2-二溴乙烷的反应原理如下:
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示: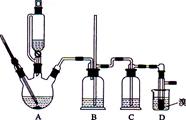
有关数据列表如下:
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)若产物中有少量副产物乙醚.可用 的方法除去;
(4)反应过程中应用冷水冷却装置D,其主要目的是避免溴大量挥发,但又不能过度冷却(如用冰水),其原因是 。
Ⅱ.已知烯烃与苯在一定条件下反应生成芳香烃。如:
丙烯是三大合成材料的基本原料,可用于合成应用广泛的DAP树脂单体和双酚等有机物,具有重要的工业用途。
(1)写出丙烯在一定条件下发生聚合反应的化学方程式 。
(2)丙烯在乙酸作用下与O2反应生成有机物A,其蒸气密度是相同状况下甲烷密度的6.25倍,元素的质量分数为:碳60%、氧32%。A的分子式为 。
(3)丙烯与苯在一定条件下反应可生成D、E、F等多种芳香烃。红外光谱、核磁共振是研究有机物结构的重要方法,根据下列数据,画出D、E的结构。
D:元素组成:C89.94%、H10.06%;1H核磁共振有5个信号。
E:元素组成:C88.82%、H11.18%;1H核磁共振有3个信号。
F:元素组成:C88.82%、H11.18%;1H核磁共振有4个信号。
D: 。 E: 。
科目:gzhx 来源:2012-2013学年陕西省西安市长安一中高二(上)期中化学试卷(解析版) 题型:解答题
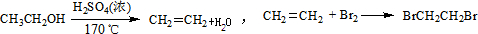
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
科目:gzhx 来源:海南 题型:问答题
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |

科目:gzhx 来源:2012年海南省高考化学试卷(解析版) 题型:填空题
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
科目:gzhx 来源: 题型:
已知:①CH3CH2OH ![]() CH2=CH2↑+H20
CH2=CH2↑+H20
CH2=CH2+Br2 ![]() BrCH2—CH2Br
BrCH2—CH2Br
②乙醇、1,2-二溴乙烷、乙醚的有关物理性质如下表所示。
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 通常状况下的状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 熔点/℃ | -130 | 9 | -116 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
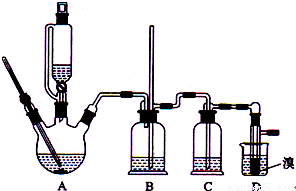
某化学小组拟用乙醇、溴等为原料在实验室制备少量的1,2一二溴乙烷,实验装置如右图所示(装置A中的加热部分的仪器装置省略没有画出)。
(1)仪器E的名称是 。
(2)仪器Ⅰ是漏斗,其左部的玻璃管的作 用是 (填字母)。
a.使漏斗中液体容易滴下
b.有利于吸收气体杂质
c.防止A中三颈烧瓶里的液体爆沸
(3)实验时,A中三颈烧瓶里放入几片碎瓷片的目的是 。加热反应过程中,三颈烧瓶里除生成乙烯外,还可能生成的有机副产物主要是 。
(4)反应过程中,若B中长玻璃导管(Ⅱ)里的液面上升,则说明可能是由于 (填“D中出现堵塞”或“C中杂质已除尽”)造成的。
(5)反应过程中,D中需用冷水冷却盛有液溴的试管,其主要目的是 。
说明制备1,2-二溴乙烷的反应已经结束的实验现象是 。
科目:gzhx 来源: 题型:
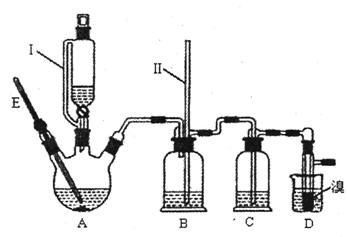
(10分)1,2 — 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2- 二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).
填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
___________________________________________________________
___________________________________________________________
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请
写出发生堵塞时瓶b中的现象._________________________________.
(3)容器c中NaOH溶液的作用是:__________________________________.
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因:_______________________________________________________
________________________________________________________
科目:gzhx 来源:2012届重庆市高二下学期期中考试化学试卷 题型:实验题
(8分)1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2- 二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:
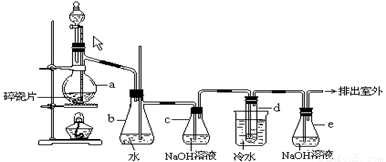
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式.
__________________ _______;____________________ __________ ______;
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象._______________________________________________________;
(3)容器c中NaOH溶液的作用是:__________________________________;
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超过许多,如果装置的气密性没有问题,试分析其可能的原因:________ _______________________;_______________________ 。
科目:gzhx 来源:2012-2013学年甘肃省甘谷县甘谷一中高二下学期期中考试化学试卷(带解析) 题型:实验题
已知实验室制备1,2-二溴乙烷可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:
有关数据列表如下:
| | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g · cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
科目:gzhx 来源: 题型:
1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2- 二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。填写下列空白:
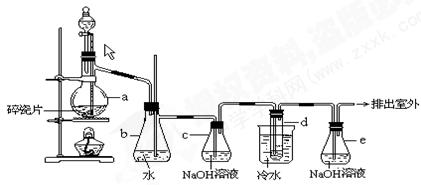
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式._____________________;________________________________;
(2)瓶b的作用是___________________;
(3)容器c中NaOH溶液的作用是:__________________________________;
(4)瓶e的作用是 。
科目:gzhx 来源:2014届甘肃省高二下学期期中考试化学试卷(解析版) 题型:实验题
已知实验室制备1,2-二溴乙烷可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:
|
|
乙醇 |
1,2-二溴乙烷 |
乙醚 |
|
状态 |
无色液体 |
无色液体 |
无色液体 |
|
密度/g · cm-3 |
0.79 |
2.2 |
0.71 |
|
沸点/℃ |
78.5 |
132 |
34.6 |
|
熔点/℃ |
一l30 |
9 |
-1l6 |
回答下列问题:
(1)反应原理是___________________________________________________________
(2)在装置C中应加入 ,(填正确选项前的字母)其目的是_______________
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制各反应已经结束的最简单方法是 ;
(4)若产物中有少量副产物乙醚.可用 的方法除去;
(5)反应过程中应用冷水冷却装置D,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 。
科目:gzhx 来源:2011-2012学年陕西省西安市庆安中学高二下学期阶段考试化学试卷(带解析) 题型:实验题
1,2—二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂在实验室中可以用下图所示装置制备1,2—二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。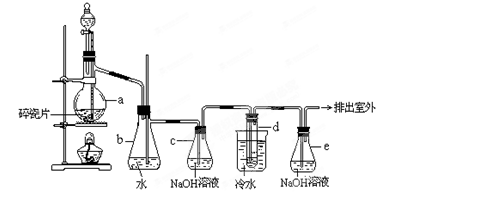
填写下列空白:
(1) 写出本题中制备1,2—二溴乙烷的两个化学反应方程式:
_________________________________;_________________________________
(2) 安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象______________________________。
(3) 容器c中NaOH溶液的作用是________________________________。
(4) 某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因:
① ___________________________________________________________;
② ___________________________________________________________
科目:gzhx 来源:2012届河北省高二上学期期末考试化学试卷 题型:实验题
(8分)1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水). 填写下列空白:

(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式
_____________________________________、
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象._________________________________.
(3)容器c中NaOH溶液的作用是:__________________________________.
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因(写出一条既可)
___________________________________________________________
科目:gzhx 来源: 题型:
1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4 ℃,熔点9.79 ℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在实验室中可以用下图所示装置制备1,2-二溴乙烷,其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水) 。
填写下列空白:
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式:
__________________________________________________________,
___________________________________________________________。
(2)配制乙醇和浓硫酸混合液的要求和操作要点
。
(3)反应后期a中反应物混合液的颜色逐渐变黑,请用简要文字和化学方程式说明原因__________________________________________________________________。
(4)瓶b的作用为: ___________________________________________。
(5)容器c、e中NaOH溶液的作用分别是:______________________
___________________________。
(6)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,如果装置的气密性没有问题,试分析其可能的原因:_______________________________________________。
科目:gzhx 来源:2013届陕西省西安市高二下学期阶段考试化学试卷(解析版) 题型:实验题
1,2—二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂在实验室中可以用下图所示装置制备1,2—二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。
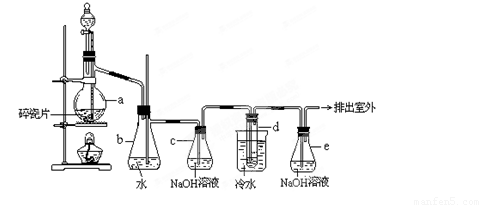
填写下列空白:
(1) 写出本题中制备1,2—二溴乙烷的两个化学反应方程式:
_________________________________;_________________________________
(2) 安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象______________________________。
(3) 容器c中NaOH溶液的作用是________________________________。
(4) 某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因:
① ___________________________________________________________;
② ___________________________________________________________