
科目:gzhx 来源: 题型:
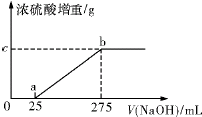 现有铵盐样品A,是(NH4)2SO4、NH4HSO4的混合物.为确定A中 各成分的含量,某研究性学习小组的同学取了数份相同质量的样品A溶于水,然后分别加入不同体积的1mol/L的NaOH溶液,水浴加热至气体 全部逸出(此温度下,铵盐不分解).该气体干燥后用足量的浓硫酸完全吸 收.浓硫酸增重的质量与加人NaOH溶液的体积的关系如图.分析该图象并回答下列问题:
现有铵盐样品A,是(NH4)2SO4、NH4HSO4的混合物.为确定A中 各成分的含量,某研究性学习小组的同学取了数份相同质量的样品A溶于水,然后分别加入不同体积的1mol/L的NaOH溶液,水浴加热至气体 全部逸出(此温度下,铵盐不分解).该气体干燥后用足量的浓硫酸完全吸 收.浓硫酸增重的质量与加人NaOH溶液的体积的关系如图.分析该图象并回答下列问题:科目:gzhx 来源: 题型:阅读理解
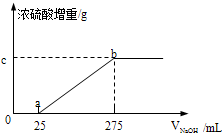 (2013•崇明县一模)现有两份铵盐样品A、B,其成分都是(NH4)2SO4、NH4HSO4的混合物.甲、乙两个研究性学习小组的同学想要确定A和B中各成分的含量.
(2013•崇明县一模)现有两份铵盐样品A、B,其成分都是(NH4)2SO4、NH4HSO4的混合物.甲、乙两个研究性学习小组的同学想要确定A和B中各成分的含量.
| ||
| ||
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 铵盐的质量(g) | 9.88 | 19.76 | 29.64 | 49.40 |
| 浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
科目:gzhx 来源:2012-2013学年上海市崇明县高三上学期期末考试化学试卷(解析版) 题型:计算题
现有两份铵盐样品A、B,其成分都是(NH4)2SO4、NH4HSO4的混合物。甲、乙两个研究性学习小组的同学想要确定A和B中各成分的含量。
甲组同学取了数分相同质量的样品A溶于水,然后分别加入不同体积的1mol/L的NaOH溶液,水浴加热至气体全部逸出。(此温度下,铵盐不分解)。该气体干燥后用足量的浓硫酸完全吸收。浓硫酸增重的质量与加入NaOH溶液的体积的关系如图。分析该图像,并回答下列问题:
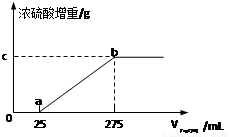
(1)写出ab段涉及的离子方程式: 。
(2)c点对应的数值是 ;样品A中(NH4)2SO4、NH4HSO4的物质的量之比为 。乙组同学取了数份不同质量的样品B,分别加入到200mL 1mol/L的NaOH溶液中,同样用水浴加热,将逸出气体干燥后再用浓H2SO4吸收。测定结果如下表:
|
实验编号 |
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
|
铵盐的质量(g) |
9.88 |
19.76 |
29.64 |
49.40 |
|
浓硫酸增加的质量(g) |
m |
m |
1.36 |
0 |
分析该表,并回答下列问题:
(3)①分析实验数据可知,实验编号为 的实验中,氢氧化钠足量,铵盐中的铵根离
子完全转化成气体;m的值为 。
②计算样品B中氮元素的质量分数。(用小数表示,保留两位小数)
(1)乙组同学在研究时发现,浓硫酸增重的质量与样品B的质量之间满足一定的函数关系。假设样品的质量为x(g),浓硫酸增重的质量为y(g)。求:当x在不同范围时y与x的函数关系。
科目:gzhx 来源: 题型:解答题
 现有两份铵盐样品A、B,其成分都是(NH4)2SO4、NH4HSO4的混合物.甲、乙两个研究性学习小组的同学想要确定A和B中各成分的含量.
现有两份铵盐样品A、B,其成分都是(NH4)2SO4、NH4HSO4的混合物.甲、乙两个研究性学习小组的同学想要确定A和B中各成分的含量.| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 铵盐的质量(g) | 9.88 | 19.76 | 29.64 | 49.40 |
| 浓硫酸增加的质量(g) | m | m | 1.36 | 0 |
科目:gzhx 来源:2014届四川省资阳市高二下学期期末检测化学试卷(解析版) 题型:选择题
已知NH4+与HCHO在水溶液中发生如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O。现有某一铵盐,为测定其氮的质量分数,称取铵盐样品m g,溶于水后,再加入足量HCHO溶液配成100 mL溶液。充分反应后,从中取出V1 mL溶液,用c mol·L-1的NaOH溶液进行中和滴定,恰好用去V2 mL。试求该铵盐中氮元素的质量分数为:
A. B.
B. C.
C.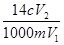 D.
D.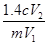
科目:gzhx 来源: 题型:
| A、①④⑥ | B、②⑤⑥ | C、②⑥ | D、④⑤⑥ |
科目:gzhx 来源: 题型:阅读理解
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ |
| FeSO4•7H2O | 15.6 | 20.5 | 26.5 | 32.9 | 40.2 | 48.6 | - |
| (NH4)2SO4 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | - | 88.0 |
| (NH4)2SO4•FeSO4•6H2O | 12.5 | 17.2 | 21.0 | 28.1 | 33.0 | 40.0 | 44.6 |
科目:gzhx 来源: 题型:单选题
科目:gzhx 来源:2007届高三化学氮族单元测试(人教版) 人教版 题型:013
|
已知NH4+与HCHO在水溶液中有如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O.现有一失去标签的铵盐氮肥.为测定其含氮量,今称取2.00g样品溶于水,加入足量的HCHO溶液,共配得100mL溶液,从中取出10mL,滴入酚酞后,再逐滴加入0.100mol/LNaOH溶液,当滴至25.00mL时溶液呈现出了粉红色,且在半分钟内未褪色,该铵盐中氮的质量分数为 | |
| [ ] | |
A. |
0.175 |
B. |
0.177 |
C. |
0.350 |
D. |
无法计算 |
科目:gzhx 来源:平阳三中2006-2007学年高二年级上学期期中考试 化学试卷 题型:013
|
已知NH4+与HCHO在水溶液中有如下反应:
现有一失去标签的铵态氮肥,为了测定其含氮量,称取2.00克样品溶于水,加入足量HCHO溶液配成100毫升溶液,再取出10.0毫升,滴入0.100 mol·L—1 NaOH溶液25.0毫升时恰好完全反应.则该铵盐中氮元素的质量分数为 | |
| [ ] | |
A. |
35.0% |
B. |
17.8% |
C. |
21.2 % |
D. |
17.5 % |
科目:gzhx 来源:2007届深圳一重点中学第一轮复习高三化学氮族单元测试(人教) 人教 题型:013
|
已知NH4+与HCHO在水溶液中有如下反应:4NH4++6HCHO→(CH2)6N4+4H++6H2O. 现有一失去标签的铵盐氮肥.为测定其含氮量,今称取2.00g样品溶于水,加入足量的HCHO溶液,共配得100mL溶液,从中取出10mL,滴入酚酞后,再逐滴加入0.100mol/LNaOH溶液,当滴至25.00mL时溶液呈现出了粉红色,且在半分钟内未褪色,该铵盐中氮的质量分数为 | |
| [ ] | |
A. |
0.175 |
B. |
0.177 |
C. |
0.350 |
D. |
无法计算 |
科目:gzhx 来源:2008届高三化学氮族单元测试题 题型:013
|
已知NH4+与HCHO在水溶液中有如下反应:4NH4++6HCHO(CH2)6N4+4H++6H2O.现有一失去标签的铵盐氮肥.为测定其含氮量,今称取2.00 g样品溶于水,加入足量的HCHO溶液,共配得100 mL溶液,从中取出10 mL,滴入酚酞后,再逐滴加入0.100 mol/LNAOH溶液,当滴至25.00 mL时溶液呈现出了粉红色,且在半分钟内未褪色,该铵盐中氮的质量分数为 | |
| [ ] | |
A. |
0.175 |
B. |
0.177 |
C. |
0.350 |
D. |
无法计算 |
科目:gzhx 来源: 题型:

| 41(z-y) |
| 17x |
| 41(z-y) |
| 17x |
| 0.048(a-b) |
| Vmx |
| 0.048(a-b) |
| Vmx |
科目:gzhx 来源: 题型:阅读理解

 HCO3-+OH-
HCO3-+OH- HCO3-+OH-
HCO3-+OH-科目:gzhx 来源: 题型:阅读理解

科目:gzhx 来源: 题型:
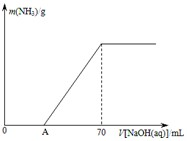 某氮肥NH4HCO3中混有少量(NH4)2CO3,现采用下列方案测定该氮肥中(NH4)2CO3的质量分数:称取5.7g上述样品与2.0mol/L NaOH溶液混合,完全溶解后,低温加热使其充分反应(该温度下铵盐不分解),并使生成的氨气全部被硫酸吸收,测得氨气的质量与所用NaOH溶液体积的关系如图所示:
某氮肥NH4HCO3中混有少量(NH4)2CO3,现采用下列方案测定该氮肥中(NH4)2CO3的质量分数:称取5.7g上述样品与2.0mol/L NaOH溶液混合,完全溶解后,低温加热使其充分反应(该温度下铵盐不分解),并使生成的氨气全部被硫酸吸收,测得氨气的质量与所用NaOH溶液体积的关系如图所示:
科目:gzhx 来源: 题型:
科目:gzhx 来源:2010-2011学年河南省高三模拟考试(理综)化学部分 题型:实验题
(14分)农民使用的氮肥主要是“氢铵”和尿素。某化学兴趣小组对某“氢铵”化肥进行了专项研究:
(1)[预测]根据已有知识预测该“氢铵”是碳酸或亚硫酸或硫酸的铵盐。
(2)[验证和探究]①NH+4的验证:取少量固体药品于试管中,然后 。(填写试剂和操作)
②阴离子的探究:a.取少量固体药品于试管中,然后向试管中滴加稀盐酸,固体全部溶解,将产生的气体通人下图装置。观察到的现象是:溴水无明显变化,澄清石灰水变浑浊。再向滴加稀盐酸反应后的试管中,加Ba(OH)2溶液,无明显现象。

初步结论:“氢铵”是 的铵盐。
b.要进一步确定“氢铵”的成分还需要补做如下实验:取适量“氢铵”配制成溶液,取试液于一支洁净的试管中,加入 。(填写试剂和操作)
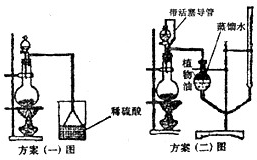
(3)[解释与评价]该实验小组设计了以下两个实验方案测定该化肥的含氮量,请你阅读后解释方案中提出的问题并进行评价方案(一):准确称取一定质量的样品mg,放入图案(一)的烧瓶中,滴加过量NaOH浓溶液,充分微热,通过实验测定烧杯增加的质量为m1g。
方案(二):准确称取一定质量的样品mg,放入图方案(二)的烧瓶中,滴加过量NaOH浓溶液,充分微热,按如图装置测量生成的氨气体积为VL(标况)。

①方案(二)图中导管a的作用是 。
②请你评价上述两套方案是否合理。若合理写出计算式;若不合理,请简要说明原因。
方案(一): 。
方案(二): 。
科目:gzhx 来源: 题型:阅读理解
(16分)已知硫酸亚铁铵晶体为浅绿色,易溶于水、不溶于乙醇,在水中的溶解度比FeSO4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。
以下是将绿矾(FeSO4•7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。根据下图回答:
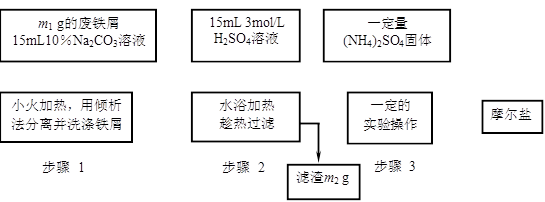
(1)为处理废铁屑表面的油污,用10%Na2CO3溶液清洗,请用离子方程式表示Na2CO3溶液呈碱性的原因: ▲ 。
(2)步骤1中采用倾析法分离出铁屑,下列适合用倾析法的有 ▲ :
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)步骤2中铁屑过量的目的是(用离子方程式表示): ▲ 。步骤2中溶液趁热过滤的原因是 ▲ 。
(4)步骤3中,加入(NH4)2SO4固体后,应加热到 ▲ 时,停止加热。需经过的实验操作包括: ▲ 、 ▲ 、减压过滤(或抽滤)等得到较为 ▲ 的晶体。
(5)抽滤装置的仪器有: ▲ 、 ▲ 、安全瓶、抽气泵组成。
(6)产品中Fe2+的定量分析:
制得的摩尔盐样品中往往含有极少量的Fe3+。为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性下用KMnO4标准液滴定的方法。
称取4.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸。用0.2 mo1/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液体积 10.00 mL。
①请完成滴定过程中发生的离子方程式:
Fe2+ + MnO4-+( )= Mn2+ + Fe3+ + H2O
②本实验的指示剂 ▲ 。
A.酚酞 B.甲基橙 C.石蕊 D.不需要
③KMnO4溶液置于 ▲ (酸式、碱式)滴定管中
④终点颜色的变化: ▲ 。
⑤产品中Fe2+的质量分数为 ▲ 。
(7)在25℃时,相同物质的量浓度的(NH4)2CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为: ▲ 。(用a,b,c回答)
科目:gzhx 来源:2011届浙江省金华一中高三高考模拟考试(理综)化学部分 题型:实验题
(16分)已知硫酸亚铁铵晶体为浅绿色,易溶于水、不溶于乙醇,在水中的溶解度比FeSO4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。
以下是将绿矾(FeSO4•7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。根据下图回答: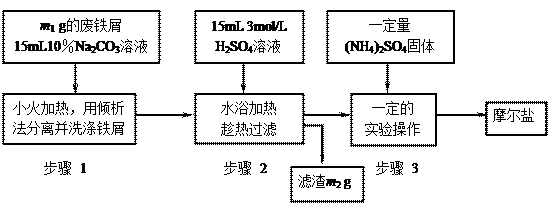
(1)为处理废铁屑表面的油污,用10%Na2CO3溶液清洗,请用离子方程式表示Na2CO3溶液呈碱性的原因: ▲ 。
(2)步骤1中采用倾析法分离出铁屑,下列适合用倾析法的有 ▲ :
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)步骤2 中铁屑过量的目的是(用离子方程式表示): ▲ 。步骤2中溶液趁热过滤的原因是 ▲ 。
中铁屑过量的目的是(用离子方程式表示): ▲ 。步骤2中溶液趁热过滤的原因是 ▲ 。
(4)步骤3中,加入(NH4)2SO4固体后,应 加热到 ▲ 时,停止加热。需经过的实验操作包括: ▲ 、 ▲ 、减压过滤(或抽滤)等得到较为 ▲ 的晶体。
加热到 ▲ 时,停止加热。需经过的实验操作包括: ▲ 、 ▲ 、减压过滤(或抽滤)等得到较为 ▲ 的晶体。
(5)抽滤装置的仪器有: ▲ 、 ▲ 、安全瓶、抽气泵组成。
(6)产品中Fe2+的定量分析:
制得的摩尔盐样品中往往含有极少量的Fe3+。为了测定摩尔盐产品中Fe2+的含 量,一般采用在酸性下用KMnO4标准液滴定的方法。
量,一般采用在酸性下用KMnO4标准液滴定的方法。
称取4.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸。用0.2 mo1/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液体积 10.00 mL。
①请完成滴定过程中发生的离子方程式:
Fe2++ MnO4-+( )=" " Mn2++ Fe3++ H2O
②本实验的指示剂 ▲ 。
A.酚酞 B.甲基橙 C.石蕊 D.不需要
③KMnO4溶液置于 ▲ (酸式、碱式)滴定管中
④终点颜色的变化: ▲ 。
⑤产品中Fe2+的质量分数为 ▲ 。 (7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为: ▲ 。(用a,b,c回答)
(7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为: ▲ 。(用a,b,c回答)