
题目列表(包括答案和解析)


| ||
| ||
(14分)近年来,在超临界CO2(临界温度Tc = 304.3K;临界压力pc = 72.8×105Pa)中的反应引起广泛关注。该流体的密度在临界点附近很容易调制,可认为是一种替代有机溶剂的绿色溶剂,该溶剂早已用于萃取咖啡因。然而,利用超临界CO2的缺点之一是CO2必须压缩。
10-1 计算将CO2从1bar压缩到50bar所需的能量,其最终体积为50ml,温度为298K,设为理想气体。
10-2 实际气体用如下方程描述(近似的):
[p+a(n/V)2](V-nb) = nRT
对于CO2:a =3.59×105 Padm6mol-2 b = 0.0427dm3mol-1
分别计算在温度为305K和350K下为达到密度220gdm-3,330 gdm-3,440 gdm-3所需的压力。
10-3 超临界流体的性质,如二氧化碳的溶解能力和反应物的扩散性与液体的密度关系密切,上问的计算表明,在哪一区域――近临界点还是在较高压力或温度下更容易调制流体的密度?
10-4 在超临界二氧化碳中氧化醇类,如将苄醇氧化为苯甲醛,是一种超临界工艺,反应在催化选择性效率为95%的Pd/Al2O3催化剂作用下进行。
(1)写出主要反应过程的配平的反应式。
(2)除完全氧化外,进一步氧化时还发生哪些反应?
10-5 在另一超流体工艺合成有机碳酸酯和甲酰胺的例子中,二氧化碳既是溶剂又可作为反应物替代光气或一氧化碳。
(1)写出甲醇和二氧化碳反应得到碳酸二甲酯的配平的化学反应方程式,如以光气为反应物如何得到碳酸二甲酯?
(2)用适当的催化剂可用吗啉和二氧化碳合成甲酰基吗啉。该反应还需添加什么反应物?写出反应式;若用一氧化碳替代,反应式如何?
10-6 用绿色化学的观念给出用二氧化碳代替一氧化碳和光气的两个理由。与以CO或COCl2为反应物对比,再给出用CO2为反应物的1个主要障碍(除必须对二氧化碳进行压缩外)
注:吗啉的分子式为C4H9NO;结构式为:![]()
雄黄(AS4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
⑴As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,该反应的化学方程式为 。
⑵上述反应中的氧化剂是 ,反应产生的气体可用 吸收。
⑶As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O,若生成2mol H3AsO4,则反应中转移电子的物质的量为 。若将该反应设计成一原电池,则NO2应该在 极附近逸出。
⑷将⑶中反应产物NO2充满干燥的烧瓶,然后将烧瓶倒立于少水槽中,向烧瓶中通入一定量的氧气,气体恰好完全溶于水(假设溶液没有扩散),则烧瓶中溶液溶质的物质的量浓度为 (设该条件下的气体摩尔体积为23.8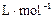 ,结果保留到小数点后三位)。
,结果保留到小数点后三位)。
雄黄(AS4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生.根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体.若As2S3和SnCl2正好完全反应,该反应的化学方程式为________.
(2)上述反应中的氧化剂是________,反应产生的气体可用________吸收.
(3)As2S3和HNO3有如下反应:As2S3+10H++10NO![]() =2H3AsO4+3S+10NO2↑+2H2O,若生成2 mol H3AsO4,则反应中转移电子的物质的量为________.若将该反应设计成一原电池,则NO2应该在________极附近逸出.
=2H3AsO4+3S+10NO2↑+2H2O,若生成2 mol H3AsO4,则反应中转移电子的物质的量为________.若将该反应设计成一原电池,则NO2应该在________极附近逸出.
(4)将(3)中反应产物NO2充满干燥的烧瓶,然后将烧瓶倒立于少水槽中,向烧瓶中通入一定量的氧气,气体恰好完全溶于水(假设溶液没有扩散),则烧瓶中溶液溶质的物质的量浓度为________(设该条件下的气体摩尔体积为23.8 L·mol-1,结果保留到小数点后三位).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com