
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
 P(g)+Q(g) ЁїH>0ЃЌЧыЛиД№ЯТСаЮЪЬтЃК
P(g)+Q(g) ЁїH>0ЃЌЧыЛиД№ЯТСаЮЪЬтЃК 
ЃЈ9ЗжЃЉЫцзХЛЗБЃвтЪЖдіЧПЃЌЧхНрФмдДдНРДдНЪмЕНШЫУЧЙизЂЁЃ
ЃЈ1ЃЉМзЭщЪЧвЛжжРэЯыЕФНрОЛШМСЯЁЃвбжЊЃК
CH4ЃЈgЃЉ+2O2ЃЈgЃЉ= CO2ЃЈgЃЉ+2H2OЃЈgЃЉЃЛЁїH= ЁЊ802ЃЎ3kJЁЄmol-1
H2OЃЈ1ЃЉ =H2OЃЈgЃЉЃЌЁїH =+44ЃЎ0kJЁЄmol-l
дђ4ЃЎ8gМзЭщЦјЬхЭъШЋАДШМЩеЩњГЩвКЬЌЫЎЃЌЗХГіШШСПЮЊ ЁЃ
ЃЈ2ЃЉРћгУМзЭщгыЫЎЗДгІжЦБИЧтЦјЃЌвђдСЯСЎМлЃЌОпгаЭЦЙуМлжЕЁЃ
ИУЗДгІЮЊCH4ЃЈgЃЉ+H2OЃЈgЃЉ COЃЈgЃЉ+3H2ЃЈgЃЉ;ЁїH=+206ЃЎlkJЁЄmol-lЁЃ
COЃЈgЃЉ+3H2ЃЈgЃЉ;ЁїH=+206ЃЎlkJЁЄmol-lЁЃ
ЂйШє800ЁцЪБЃЌЗДгІЕФЛЏбЇЦНКтГЃЪ§K=lЃЎ0ЃЌФГЪБПЬВтЕУИУЮТЖШЯТУмБеШнЦїжаИїЮяжЪЕФЮяжЪЕФСПХЈЖШШчЯТБэЁЃ
дђДЫЪБе§ЁЂФцЗДгІЫйТЪЕФЙиЯЕЪЧ ЁЃЃЈЬюБъКХЃЉ
| AЃЎvЃЈе§ЃЉ>vЃЈФцЃЉ | BЃЎvЃЈе§ЃЉ<vЃЈФцЃЉ |
| CЃЎvЃЈе§ЃЉ=vЃЈФцЃЉ | DЃЎЮоЗЈХаЖЯ |
 COЃЈgЃЉ+3H2ЃЈgЃЉ;ЁїH=+206ЃЎlkJЁЄmol-lЁЃ
COЃЈgЃЉ+3H2ЃЈgЃЉ;ЁїH=+206ЃЎlkJЁЄmol-lЁЃ
| AЃЎvЃЈе§ЃЉ>vЃЈФцЃЉ | BЃЎvЃЈе§ЃЉ<vЃЈФцЃЉ |
| CЃЎvЃЈе§ЃЉ=vЃЈФцЃЉ | DЃЎЮоЗЈХаЖЯ |
ЃЈ9ЗжЃЉЫцзХЛЗБЃвтЪЖдіЧПЃЌЧхНрФмдДдНРДдНЪмЕНШЫУЧЙизЂЁЃ
ЃЈ1ЃЉМзЭщЪЧвЛжжРэЯыЕФНрОЛШМСЯЁЃвбжЊЃК
CH4ЃЈgЃЉ+2O2ЃЈgЃЉ=CO2ЃЈgЃЉ+2H2OЃЈgЃЉЃЛЁїH=ЁЊ802ЃЎ3kJЁЄmol-1
H2OЃЈ1ЃЉ=H2OЃЈgЃЉЃЌЁїH =+44ЃЎ0kJЁЄmol-l
дђ4ЃЎ8gМзЭщЦјЬхЭъШЋАДШМЩеЩњГЩвКЬЌЫЎЃЌЗХГіШШСПЮЊ ЁЃ
ЃЈ2ЃЉРћгУМзЭщгыЫЎЗДгІжЦБИЧтЦјЃЌвђдСЯСЎМлЃЌОпгаЭЦЙуМлжЕЁЃ
ИУЗДгІЮЊCH4ЃЈgЃЉ+H2OЃЈgЃЉ![]() COЃЈgЃЉ+3H2ЃЈgЃЉ;ЁїH=+206ЃЎlkJЁЄmol-lЁЃ
COЃЈgЃЉ+3H2ЃЈgЃЉ;ЁїH=+206ЃЎlkJЁЄmol-lЁЃ
ЂйШє800ЁцЪБЃЌЗДгІЕФЛЏбЇЦНКтГЃЪ§K=lЃЎ0ЃЌФГЪБПЬВтЕУИУЮТЖШЯТУмБеШнЦїжаИїЮяжЪЕФЮяжЪЕФСПХЈЖШШчЯТБэЁЃ
дђДЫЪБе§ЁЂФцЗДгІЫйТЪЕФЙиЯЕЪЧ ЁЃЃЈЬюБъКХЃЉ
AЃЎvЃЈе§ЃЉ>vЃЈФцЃЉ BЃЎvЃЈе§ЃЉ<vЃЈФцЃЉ
CЃЎvЃЈе§ЃЉ=vЃЈФцЃЉ DЃЎЮоЗЈХаЖЯ
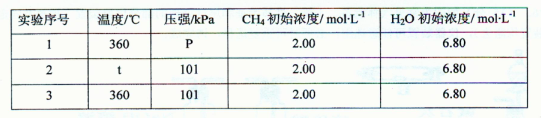
ЂкЮЊСЫЬНОПЮТЖШЁЂбЙЧПЖдЩЯЪіЛЏбЇЗДгІЫйТЪЕФгАЯьЃЌФГЭЌбЇЩшМЦСЫвдЯТШ§зщЖдБШЪЕбщЃЈЮТЖШЮЊ360ЁцЛђ480ЁцЁЂбЙЧПЮЊ101 kPaЛђ303 kPaЃЌЦфгрЪЕбщЬѕМўМћЯТБэЃЉЁЃ
Бэжаt= ЃЌP= ЃЛ
ЩшМЦЪЕбщ2ЁЂ3ЕФФПЕФЪЧ
ЪЕбщlЁЂ2ЁЂ3жаЗДгІЕФЛЏбЇЦНКтГЃЪ§ЕФДѓаЁЙиЯЕЪЧ ЃЈгУK1ЁЂK2ЁЂK3БэЪОЃЉЁЃ
МзДМЪЧвЛжжПЩдйЩњФмдДЃЌОпгаЙуЗКЕФПЊЗЂКЭгІгУЧАОАЁЃ

ЃЈ1ЃЉЙЄвЕЩЯвЛАуВЩгУШчЯТЗДгІКЯГЩМзДМЃК
COЃЈgЃЉ+2H2ЃЈgЃЉ CH2O
HЃЈgЃЉЁїH= xkJЃЏmoЂйгвЭМЪЧЗДгІЪБCOКЭCH3 0HЕФХЈЖШЫцЪБМфЕФБфЛЏЧщПіЁЃДгЗДгІПЊЪМЕНЦНКтЃЌгУCOХЈЖШБфЛЏБэЪОЦНОљЗДгІЫйТЪvЃЈCOЃЉ=__ __ЁЃ
ЂкЯТБэЫљСаЪ§ОнЪЧИУЗДгІдкВЛЭЌЮТЖШЯТЕФЛЏбЇЦНКт
ГЃЪ§ЃЈKЃЉ
|
ЮТЖШ |
250Ёц |
300Ёц |
350Ёц |
|
K |
2.041 |
0.270 |
0.012 |
гЩБэжаЪ§ОнХаЖЯx 0ЃЈЬюЁА<ЁБЁЂЁА<ЁБЬюЁА=ЁБЃЉ
ЂлФГЮТЖШЯТЃЌНЋ2molCOКЭ6molH2ГфШы2LЕФУмБеШнЦїжаЃЌГфЗжЗДгІЃЌДяЕНЦНКтКѓЃЌВтЕУ
cЃЈCOЃЉ=0.2mol/LЃЌдђCOЕФзЊЛЏТЪЮЊ____ЁЃ
ЃЈ2ЃЉвбжЊдкГЃЮТГЃбЙЯТ
Ђй2CH3OHЃЈ1ЃЉ+3O2ЃЈgЃЉ 2CO2ЃЈgЃЉ+4H2OЃЈgЃЉ ЁїH=ЁЊ1275.6kJ/mol
Ђк2COЃЈgЃЉ+O2ЃЈgЃЉ 2CO2ЃЈgЃЉЁїH=ЁЊ566.0kJ/mol
ЂлH2OЃЈgЃЉ H2OЃЈ1ЃЉ
ЁїH=ЁЊ44.0kJ/mol
ЧыМЦЫу1molМзДМВЛЭъШЋШМЩеЩњГЩlmolCOКЭвКЬЌЫЎЗХГіЕФШШСПЮЊ____ЁЃ
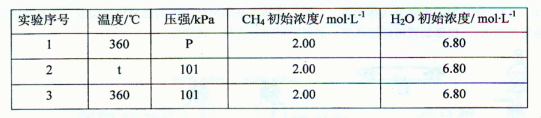
ЃЈ3ЃЉРћгУМзДМШМСЯЕчГиЩшМЦШчгвЭМЫљЪОЕФзАжУЃК
дђИУзАжУжаbЮЊ____МЋЃЛCuМЋЕФЕчМЋЗДгІЪНЮЊ____ЁЃ
ЕБЭЦЌЕФжЪСПБфЛЏЮЊ25ЃЎ6gЪБЃЌaМЋЩЯЯћКФЕФO2дкБъзМзДПіЯТЕФЬхЛ§ЮЊ_ __LЁЃ

ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com