
题目列表(包括答案和解析)
|
一种大型蓄电系统的电池总反应为:2Na2S2+NaBr3 中的左右两侧为电极,中间为离子选择性膜(在电池放电和充电时该膜允许钠离 子通过);放电前,被膜隔开的电解质为Na2S2和NaBr3,放电后,分别变为Na2S4 和NaBr.下列说法正确的是
| |
| [ ] | |
A. |
充电过程中,Na+离子的流向为从右到左 |
B. |
充电过程中,阳极的电极反应为:3NaBr-2e-=NaBr3+2Na+ |
C. |
放电前,左侧电解质为Na2S2,右侧电解质为NaBr3 |
D. |
放电过程中,电子由负极通过外电路流向正极 |
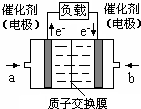 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路.质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路.质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法正确的是( )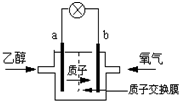 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )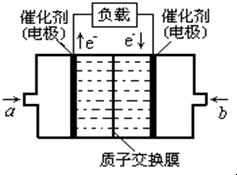 甲醇燃料电池已经面世,其结构示意图如图.甲醇在催化作用下提供质子(H+)和电子,电子经外电路、质子(H+)经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2═2CO2+4H2O,下列说法不正确的是( )
甲醇燃料电池已经面世,其结构示意图如图.甲醇在催化作用下提供质子(H+)和电子,电子经外电路、质子(H+)经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2═2CO2+4H2O,下列说法不正确的是( )湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com