
题目列表(包括答案和解析)
6. 钾肥能使农作物生长茁壮,茎秆粗硬,增强抗倒伏能力。下列物质能作钾肥的是
A.NH4NO3 B.Ca(H2PO4)2 C.K2CO3 D.FeSO4
5. 与元素的化学性质密切相关的是
A.质子数 B.电子总数 C.最外层电子数 D.中子数
4. 冬天用煤火取暖时造成煤气中毒的气体是
A.H2 B.O2 C.N2 D. CO
3. 下列物质都是我们日常生活所接触到的,其中属于纯净物的是
A.碘酒 B.雪碧 C.天然气 D.蒸馏水
2. 生活中的下列现象,属于化学变化的是
A.水分蒸发 B.菜刀生锈 C.冰雪融化 D.轮胎爆炸
(每小题1分,共25分)
1. 空气的成分中,体积分数约占78%的是
A.氧气 B.氮气 C.稀有气体 D.二氧化碳
29.(5分)初三(1)班学生将采集到的块状石灰石样品用水冲洗后晾干,称得样品质量为25.0g。该班甲、乙两组同学共利用这25.0g石灰石样品分别进行了如下实验。(假设样品中其他杂质不参加反应,不考虑水、氯化氢逸出)
[实验过程]甲组:取一定质量的块状石灰石样品于锥形瓶内,加入过量的10%的稀盐酸M g,测定反应过程中锥形瓶中的药品质量变化。(如图a)
乙组:把剩余的块状石灰石样品研碎成粉末状,然后全部置于另一锥形瓶内,加入10%的稀盐酸N g,测定反应过程中锥形瓶中药品的质量变化。(如图b)
两组同学经数据处理得到释放出二氧化碳的质量与反应时间的关系如图c。
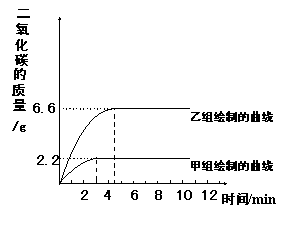
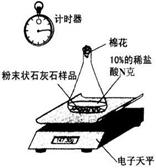
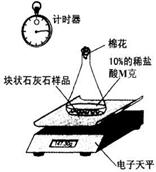
图a 图b 图c
[问题讨论]
(1)甲、乙两组同学的实验中, 组实验消耗的时间更短。
(2)两次实验中消耗的稀盐酸质量比甲: 乙=__________。
(3)求石灰石样品中碳酸钙的质量分数。
28.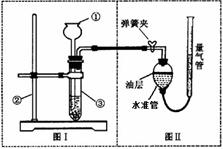 (9分)小明设计了如下图所示的实验装置来证明氧化铜能加快过氧化氢溶液的分解,并与相同条件下MnO2的催化效果做比较,实验时间均以生成30 mL气体为准(即比较反应速率)。用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
(9分)小明设计了如下图所示的实验装置来证明氧化铜能加快过氧化氢溶液的分解,并与相同条件下MnO2的催化效果做比较,实验时间均以生成30 mL气体为准(即比较反应速率)。用图示装置测量产生气体的体积,其它可能影响实验因素均已忽略,相关数据如下:
|
实验序号 |
过氧化氢溶液体积 |
催化剂 |
待测数据 |
|
① |
15mL |
无 |
|
|
② |
15mL |
CuO(0.5g) |
|
|
③ |
15mL |
MnO2(0.5g) |
|
(1) 检查图(I)装置气密性的方法是: ;
检查图(Ⅱ)装置气密性的方法是: ;
(2) 图(Ⅱ)装置中油层的作用是 。
(3)从设计原理看,实验中的“待测数据”可以是指 。
(4)为了较准确地测量气体体积,在读取反应前后量气管中液面的读数的过程中,应注意 (填字母编号)。
a.视线与凹液面最低处相平 b.读数前不能移动量气管和水准管
c.保持水准管静止,待水准管中液面不再上升时,立刻读数
d.读数前应上下移动水准管,待两管液面相平再读数
(5)如果要进一步探究CuO是否是该反应的催化剂,请完成下列实验。
|
实验步骤和现象 |
设计这一步骤的目的 |
|
(1)取15mL过氧化氢溶液,加入0.5g
CuO后,产生O2的速率比未加入时快得多 |
CuO能加快过氧化氢溶液的分解 |
|
|
|
|
|
|
(三)温度对金属与盐酸反应速率也有影响
取两个烧杯,分别加入等质量的 (“同种”、 “不同种”)金属,再分别加入足量的质量分数 (“相同”、 “不相同”)的稀盐酸……实验表明,温度越高,盐酸与金属反应的速率越快。
27.(5分)实验室有一包白色固体,可能含有无水硫酸铜、硫酸钠、碳酸钙、氯化钡、氯化钾中的一种或几种。现做如下实验:
a.取少量白色固体加足量的水溶解,过滤得沉淀和无色溶液。
b.向所得的沉淀中加入足量的稀硝酸,沉淀有部分溶解,并有气体产生,再过滤,滤液无色。
回答下列问题:
⑴.仅根据第一步实验现象的描述,你认为白色固体中无水硫酸铜______________。(选填“存在”、“不存在”或“不能确定”) 。
⑵.根据两步实验的现象,你认为该白色固体中一定不含有的物质是_________________,不能确定是否含有的物质是_________________,沉淀有部分溶解的化学反应方程式是_____________ 。
(二)金属与不同质量分数的盐酸反应的快慢不同
 取质量相等的锌片,分别放入5%、20%的足量稀盐酸中。
取质量相等的锌片,分别放入5%、20%的足量稀盐酸中。
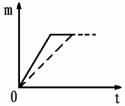 生成氢气的质量为m,反应时间为t。5%的盐酸与锌片反应m与t的关系曲线如图2所示。请在该图上补画出20%的盐酸与锌片反应m与 t的关系曲线。
生成氢气的质量为m,反应时间为t。5%的盐酸与锌片反应m与t的关系曲线如图2所示。请在该图上补画出20%的盐酸与锌片反应m与 t的关系曲线。
实验表明,盐酸质量分数越大,与金属反应的速率越快。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com