
题目列表(包括答案和解析)
25.(10分)
 感光性高分子又称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料。其结构简式为:
感光性高分子又称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料。其结构简式为:
(1)在一定条件下,该高聚物可发生的反应有 (填代号)
① 加成反应 ② 氧化反应 ③ 消去反应
④ 酯化反应 ⑤ 卤代反应
(2)该高聚物在催化剂的作用下,水解后的产物中有一种相对分子质量较小的R,其分子式为 。
(3)写出R在一定条件下与乙醇反应的化学方程式:
。
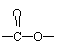

(4) R的同分异构体有多种,其中含有苯环、 和 ,且苯环上有两个对位取代基的结构简式是
R的同分异构体有多种,其中含有苯环、 和 ,且苯环上有两个对位取代基的结构简式是
。
24.(8分)
有机物A(C6H8O4)为食品包装纸的常用防腐剂。A可以使溴水褪色,A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状态下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)B分子所含官能团的名称是 。
(2)B分子中没有支链,其结构简式是 。
(3)A的结构简式是 。
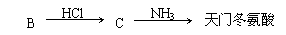 (4)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
(4)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
天门冬氨酸的结构简式是 。
23.(12分)
 在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:
(1)碘位于元素周期表中的第 族,第 周期。
(2)步骤①加Fe的目的是 。
(3)写出步骤②的化学方程式 。
(4)上述生产流程中,可以利用的副产物是 ,考虑原料循环利用,若将该副产物制成生产所需的试剂,先后还需加入 来进行处理。
(5)甲物质见光易变黑,其原因是(用化学方程式表示): 。
(6)分离I2和丁的方法是 。
22.(9分)
(1)航天飞机曾用金属铝粉和高氯酸铵混合物作为固体燃料。加热铝粉使其氧化并放出大量热量,促使混合物中另一种燃料分解。m mol高氯酸铵分解时除产生2m mol水蒸气和m mol氧气外,其他组成元素均以单质形式放出,因而产生巨大的推动力。
写出其中涉及到的化学方程式:
;
。
(2)高氯酸铵作为火箭燃料的重要氧载体。高氯酸铵在高压、450℃的条件下迅速分解生成水蒸气、氮气、氯化氢和氧气。
①写出此反应的化学方程式 。
②反应中生成的氧化产物与还原产物的物质的量之比是 ,
每分解1mol高氯酸铵,转移的电子数目是 。
21.(12分)
测定硫酸铜晶体(CuSO4·xH2O)里结晶水的含量,实验步骤为: ①研磨;②用坩埚准确称取2.0g已经研碎的硫酸铜晶体;③加热;④冷却;⑤称量;⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g 为止;⑦根据实验数据计算硫酸铜晶体里结晶水的含量。
请回答相关问题:
(1)步骤①需要的实验仪器是: 。
(2)步骤 (填编号)需要使用干燥器,使用干燥器的目的是
。
(3)步骤③具体的操作是:将盛有硫酸铜晶体的坩埚放在三角架上面的泥三角上,用酒精灯缓慢加热,同时用玻璃棒轻轻搅拌硫酸铜晶体。加热一段时间后,若晶体显蓝色,此时应当 ;若晶体变为黑色,此时应当 。
(4)步骤⑥的目的是 。
(5)若操作正确而实验测得的硫酸铜晶体里结晶水的含量偏低,其原因可能有 。(填编号)
A.被测样品中含有加热不挥发的杂质
B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水
D.加热前所用的坩埚未完全干燥
20.(12分)
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:
2FeSO4  Fe2O3+SO2↑+SO3↑。某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量。
Fe2O3+SO2↑+SO3↑。某研究性学习小组用下图所示装置检验该反应所产生的气态物质,然后用装置中A瓶内的混合物来测定已分解的FeSO4的质量。
(SO2沸点为-10.02℃)

请回答相关问题:
(1)A瓶所盛试剂的作用是 ;B瓶所盛的试剂是 ;C瓶所盛试剂的作用是 。
(2)A瓶要用冷水冷却的原因是 。
(3)将此反应生成的气体通入A瓶BaCl2溶液中,则 。(填编号)
A.析出BaSO3沉淀 B.析出BaSO4沉淀
C.逸出SO3气体 D.逸出SO2气体
理由是 。
(4)反应后若用A瓶内的混合物来测定已分解的FeSO4的质量,其实验操作的第一步是(简述操作步骤) 。
19. 单质钛(Ti)的机械强度高,抗蚀能力强,有“未来金属”之称。工业上常用硫酸分解钛铁矿(FeTiO3)的方法来制取TiO2,再由TiO2制金属钛,主要反应有:
① FeTiO3 +2H2SO4=TiOSO4+ FeSO4 +2H2O
② TiOSO4 +2H2O=H2TiO3↓+H2SO4
③
H2TiO3 TiO2+H2O
TiO2+H2O
④
TiO2 +2C +2Cl2 TiCl4+2CO
TiCl4+2CO
⑤ TiCl4 +2Mg=2MgCl2 +Ti
下列叙述不正确的是
A. 反应①不是氧化还原反应
B. 反应②是水解反应
C. 反应④中TiO2是氧化剂
D. 反应⑤表现了金属镁还原性比金属钛强
18. 对可逆反应2SO2(g) + O2(g) 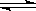 2SO3(g),下列判断正确的是
2SO3(g),下列判断正确的是
A. 若单位时间内生成x molSO3的同时,消耗x mol SO2,则反应达到平衡状态
B. 达到化学平衡时,2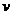 正(O2)=
正(O2)=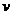 逆(SO3)
逆(SO3)
C. 平衡时,SO2的浓度必定等于O2浓度的2倍
D. 达到化学平衡时,若增大容器体积,则正反应速率减小,逆反应速率增大
17. AB3是短周期两种元素形成的化合物,已知B原子比A原子多一个电子层,且AB3分子中所有原子的最外层都满足8电子结构,则下列说法正确的是
A. A是IIIA族元素
B. AB3是三氧化硫
C. B的氢化物和A的氢化物都极易溶于水
D. B原子比A原子多10个电子
16. 常温下将NaOH稀溶液与CH3COOH稀溶液混合,不可能出现的结果是
A. pH>7,且c(OH-)>c(Na+)>c(H+)>c(CH3COO-)
B. pH>7,且c(Na+)+c(H+)=c(OH-)+c(CH3COO-)
C. pH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D. pH=7,且c(CH3COO-)>c(Na+)>c(H+)=c(OH-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com