
题目列表(包括答案和解析)
7.已知下列几种烷烃的燃烧热数据如下:
|
烷烃 |
甲烷 |
乙烷 |
丙烷 |
丁烷 |
|
燃烧热/(kJ/mol-1) |
890 |
1560 |
2220 |
2880 |
据此判断,表示戊烷燃烧的热化学方程式正确的是
A.C5H12(l) + 8O2(g) = 5CO2(g) + 6H2O(l);△H = - 3540 kJ/mol
B.C5H12(l) + 8O2(g) = 5CO2(g) + 6H2O(g);△H = - 3540 kJ/mol
C.C5H12(l) + 8O2(g) = 5CO2(g) + 6H2O(g);△H = + 3540 kJ/mol
D.C5H12(l) + 8O2(g) = 5CO2(g) + 6H2O(l);△H = + 3540 kJ/mol
6.下图分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图

在上述实验过程中,所涉及的三次分离操作分别是
A.① 蒸馏 ② 过滤 ③ 分液 B.① 分液 ② 蒸馏 ③ 蒸馏
C.① 蒸馏 ② 分液 ③ 分液 D.① 分液 ② 蒸馏 ③ 结晶、过滤
5.下列有关物质性质的比较中,正确的是
....
A.酸性:H2SO4 < HClO4
B.水溶性: CH3CH2OH < CH3COOCH2CH3
C.稳定性: HF < HBr
D.碱性 RbOH < Mg(OH)2
4.下列做法符合实验操作或事故处理规范的是
A.做氢气还原氧化铜的实验时,先加热氧化铜再通氢气
B.蒸馏石油时,将温度计插入到石油液面以下
C.皮肤上不慎沾有少量浓硫酸时,立刻用大量水冲洗
D.配制浓硫酸与酒精的混合液时,将酒精加入盛有浓硫酸的烧杯中
3.氧可与许多元素形成化合物,下列有关叙述错误的是
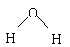
A.水分子的结构式为
B.氧与氟形成的化合物(OF2)中,氧元素的化合价为-2价
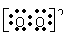
 C.Na2O2的电子式为Na+
Na+
C.Na2O2的电子式为Na+
Na+
D.在MgO晶体中,O2-的结构示意图可表示为
2.一定量的锎(252 98Cf)是有用的中子源,1 mg (252 98Cf)每秒约放出2.34×199个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关锎的说法错误的是
A.(252 98Cf)原子中,中子数为154 B.(252 98Cf)原子中,质子数为98
C.(252 98Cf)原子中,电子数为98 D.锎元素的相对原子质量为252
1.“抓好资源节约,建设环境友好型社会”,是我国社会和经济长期发展的重要保证。你认为下列做法与之不相符的是
A.推广使用乙醇汽油作汽车燃料
B.研制开发以水代替有机溶剂的化工涂料
C.农村大力发展沼气,将废弃的秸杆转化为清洁高效的能源。
D.包装盒、快餐盒等全部用聚苯乙烯生产,以减少木材的使用
29、(10分)A、B、C、D、E都是元素周期表中前20号元素,其原子序数依次增大。B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族。B、C、D的最高价氧化物的水化物均能互相反应生成盐和水。A和E可形成离子化合物,其晶胞结构如下图所示:
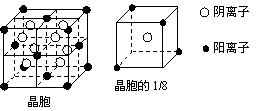 (1)A和E所形成的化合物的电子式是
(1)A和E所形成的化合物的电子式是
(2)A、B、C、D四种元素的原子半径由小到大的
顺序为 (用元素符号表示)
(3)A和D的氢化物中,后者沸点较低,原因是
(4)A和E的化合物晶体中,每个阳离子的周围
与它最近且等距离的阳离子共有 个
(5)已知A和E所形成的化合物晶体的晶胞体积为1.6×10-22cm3,则A和E组成的离子化合物的密度为(结果保留一位小数) 。
(6)现代原子结构理论认为,在同一电子层上有s、p、d、f、g、h……等能级,各能级分别有1、3、5……个轨道。2006年有人预言,126号元素(一种极稳定的超重元素)可能与A能形成稳定的化合物,按照元素周期律,126号元素应位于周期表第 周期;请根据元素原子核外电子填充的顺序预测,该元素的价电子排布式应为 。
28、 (10分)抗禽流感药物达菲是以莽草酸(A)为原料合成制得。莽草酸可以从香料“八角”中提取,其结构简式如下:
(10分)抗禽流感药物达菲是以莽草酸(A)为原料合成制得。莽草酸可以从香料“八角”中提取,其结构简式如下:
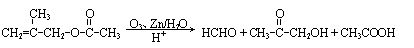
已知:①
②在NaOH稀溶液中,1molB能与2molNaOH反应
③F转化为G时,产物只有一种结构且能使溴水褪色
④各物质之间存在下列所示的转化关系:

(1)写出化合物A中所有官能团的名称
(2)写出F→G的反应类型
(3)写出D的结构简式:
(4)已知B的同分异构体有下列性质:①与FeCl3溶液作用显紫色;②与新制Cu(OH)2浊液作用产生红色沉淀;③苯环上的一卤代物只有2种。写出符合以上要求的B的同分异构体的结构简式
。
(5)在有机物分子中,若碳原子连接四个不同的原子或原子团,该碳原子称为手性碳原子。试设计一步反应使A生成具有2个手性碳原子的物质,其化学方程式为
。
27、 (10分)某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”,以节省石油资源。已知制酒精的方法有三种:
(10分)某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”,以节省石油资源。已知制酒精的方法有三种:

 ①在催化剂作用下乙烯与水反应; ②CH3CH2Br
+ H2O CH3CH2OH
+ HBr
①在催化剂作用下乙烯与水反应; ②CH3CH2Br
+ H2O CH3CH2OH
+ HBr
③ (C6H10O5)n(淀粉) + nH2O nC6H12O6(葡萄糖);C6H12O6(葡萄糖) 2C2H5OH + 2CO2↑
(1)方法①的化学反应方程式是
(2)方法②的化学反应类型是
(3)为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?请简述理由
。
(4)如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是( )
A、① B、③ C、①③ D、①②③
(5)乙醇分子中的氧原子被硫原子取代后的有机物叫乙硫醇,其性质与乙醇相似,但乙硫醇有酸性,它能与NaOH等强碱溶液反应生成无色溶液。石油中因含乙硫醇(无色液体,微溶于水)使汽油有臭味且其燃烧产生的二氧化硫会污染环境,因此要把它除去。
①用化学方法除去石油样品中的乙硫醇,请写出有关反应的化学方程式
②乙硫醇与乙酸在一定条件下可发生酯化反应,写出该反应的化学程式
③在120℃、1.01×105Pa时,将乙醇、乙硫醇的混合蒸气1L和5LO2混合,充分燃烧后,恢复到原状况,气体密度减少为燃烧前混合气的10/11,则乙醇和乙硫醇的体积之比为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com