
题目列表(包括答案和解析)
2、下列热化学方程式中的反应热下划线处表示燃烧热的是B
A.NH3(g)+ O2(g)
O2(g) NO(g)+
NO(g)+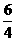 H2O(g); ΔH=-a kJ·mol-1
H2O(g); ΔH=-a kJ·mol-1
B.C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l); ΔH=-b kJ·mol-1
6CO2(g)+6H2O(l); ΔH=-b kJ·mol-1
C.2CO(g)+O2(g) 2CO2(g);
ΔH=-c kJ·mol-1
2CO2(g);
ΔH=-c kJ·mol-1
D.CH3CH2OH(l)+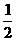 O2(g)
O2(g) CH3CHO(l)+H2O(l);ΔH=-d kJ·mol-1
CH3CHO(l)+H2O(l);ΔH=-d kJ·mol-1
1.已知:①1 mol H2分子中化学键断裂时需要吸收436 kJ的能量,②1 mol I2蒸气中化学键断裂时需要吸收151 kJ的能量,③由H原子和I原子形成1 mol HI气态分子时释放299 kJ的能量。下列热化学方程式正确的是A
A.2HI(g) ===H2(g)+I2(g);∆H=+11 kJ/mol
B. H2(g)+
H2(g)+ I2(g) ===HI(g);∆H=-11 kJ/mol
I2(g) ===HI(g);∆H=-11 kJ/mol
C. H2(g)+I2(g) ===2HI(g);∆H=+288 kJ/mol
D. H2(g)+
H2(g)+ I2(g) ===HI(g);∆H=-144 kJ/mol
I2(g) ===HI(g);∆H=-144 kJ/mol
15.(1) H++OH-=H2O (1分) CO32-+H+=HCO3-(1分)
(2) 224mL (2分)
(3) 42.4% (4分)
本资料由《七彩教育网》 提供!
15. (8分)将2.5克碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶于水制成溶液,然后向该溶液中逐滴加入1mol/L盐酸。所加入的盐酸溶液的体积与产生的二氧化碳气体的体积(标准状况)的关系如图所示:
(1) 写出OA段所反应的离子方程式___________________________________________
(2) 当加入35mL盐酸时,所产生的二氧化碳体积(标准状况)是_______________mL。
(3) 计算原混合物中碳酸钠的质量分数(写出计算过程)。


14.15.6g
14.(6分)铜和镁的合金8.8g完全溶于浓硝酸,若反应中硝酸被还原只产生6.72L的NO2气体和1.12L的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,求生成沉淀的质量。
13.(1)40g (2)24.2%
13.(6分)某温度下的CuSO4溶液200克,蒸发掉31克水,恢复到原温度,或向其中加入25克CuSO4·5H2O晶体,均可使溶液达到饱和。试计算:
(1)该温度下CuSO4·的溶解度。
(2)原溶液中溶质的质量分数。
12.(1)2片小苏打所含NaHCO3的质量为1.008g,
其物质的量为1.008g ÷84g/mol=0.012mol,
由HCO3-+H+=== CO2↑+H2O,可知n(H+)=0.012mol。
(2)6片小苏打的物质的量为:0.036mol,即中和的H+为0.036mol,而每片的Al(OH)3
的物质的量为0.234g÷78g/mol =0.003mol,由Al(OH)3+3H+ ===Al3++3H2O,
中和的H+为0.009mol,所以Al(OH)3的片数为:0.036÷0.009 = 4片。
12.小苏打、胃舒平都是常用的中和胃酸的药物。
(1)小苏打每片含0.504g NaHCO3,2片小苏打片和胃酸完全中和,被中和的H+的物质的量是多少?
(2)胃舒平每片含0.234g Al(OH)3。中和胃酸时,6片小苏打片相当于多少片胃舒平?
(写出计算过程)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com